
- •1. Основные законы химии
- •1.1 Моль. Количество вещества эквивалента (эквивалент) и молярная масса эквивалента (эквивалентная масса) простых и сложных веществ. Закон эквивалентов
- •2. Строение атома и химическая связь
- •2.1 Строение атома
- •2.2 Химическая связь и строение молекул.
- •3. Энергетика химических процессов
- •3.1 Химическое сродство.
- •4. Химическая кинетика и равновесие
- •5. Дисперсные системы
- •5.1 Способы выражения концентрации раствора
- •5.3 Ионно-молекулярные (ионные) реакции обмена
- •5.4 Гидролиз солей
- •6.Окислительно-восстановительные
- •6.1 Электродные потенциалы и электродвижущие силы
- •6.2 Электролиз
- •6.3 Коррозия металлов
- •7. Комплексные соединения
- •8. Жесткость воды и методы ее устранения
- •9.Теория строения органических соединений
- •9.1 Теория а.М. Бутлерова
- •9.2 Углеродные цепи и изомерия
- •9.3 Электронные структуры органических соединений
- •10. Классификация органических соединении.
- •10.1 Радикалы
- •10.2 Функциональные группы
- •10.3 Типы реакций органических соединений
- •11. Реакции полимеризации.
- •11.1 Полимеризация органических соединений
- •11.2 Полимеризация углеводородов с двойной связью
- •11.3 Сополимеризация.
- •11.4 Ионная полимеризация.
- •11.5 Пространственная изомерия
- •12. Кристаллическое состояние
- •12.1 Основные понятия
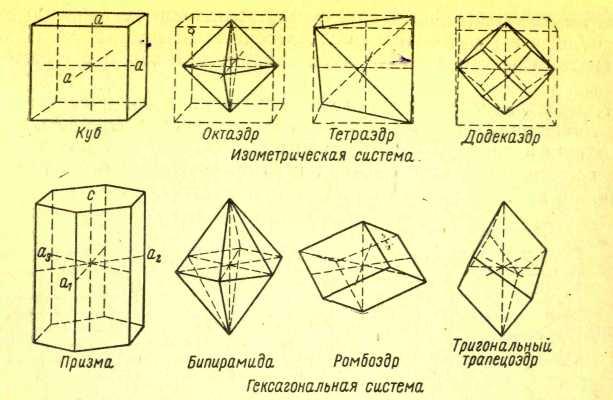
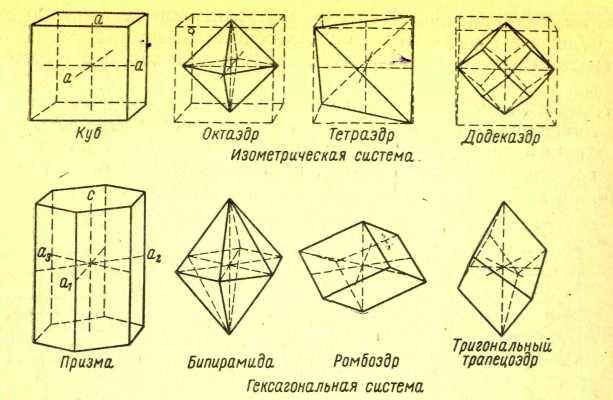
- •12.2 Симметрия кристаллов. Система кристаллов
- •12.3 Кристаллические решетки
- •13. Сплавы
- •13.1 Диаграммы состояния металлических систем.
12.3 Кристаллические решетки
Зонке (1879 г.), Чермак, Шенфлис, Федоров (1891 г.) и другие показали геометрически, что все кристаллические формы можно представить как результат распределения точек (мельчайших вещественных частиц) в пространстве по законам симметрии; получающиеся конфигурации они назвали кристаллическими решетками.
Распределяя согласно элементам симметрии точки в пространстве, они получили 230 комбинаций, 230 кристаллических решеток, которые соответствуют всем встречающимся в природе кристаллическим формам.
Последующее исследование кристаллов с помощью лучей Рентгена немецким ученым Лауэ (1912 г.) подтвердило те предположения и выводы, которые были сделаны косвенным путем. Были получены прямые доказательства существования атомов, ионов и способов их расположения в пространстве.
Кристаллические решетки, как выяснилось, делятся на следующие группы: атомные, ионные, молекулярные и металлические.
Атомные решетки. Каждое узловое место в атомной решетке занято нейтральным атомом. Примером может служить кристаллическая решетка аргона, приведенная на рис. 6.
Ионные решетки. Каждое узловое место в ионной решетке занято ионом. Примеры ионных решеток приведены на рис. 7 и 8. На рис. 7, а показана кристаллическая решетка Na+Cl-, на рис. 7,6 — решетка CsJ; на рис. 8 приведена кристаллическая решетка CaF2.
Кристаллическая решетка Na+Cl- типична для бинарных электролитов, состоит из двух центрированных в гранях решеток, вдвинутых одна в другую на ½ длины ребра куба. Одна решетка — катиона Na+, другая такая же—аниона С1-.
 Кристаллическая
решетка Cs+J-
представляет собой сочетание двух
простых кубических решеток: решетки
иона Cs+
и решетки иона
J-,
вдвинутых одна в другую так, что в центре
куба находится; ион
йода, а в углах — ионы Cs+.
Эта решетка центрирована в пространстве
так, что в центре куба находится анион,
а в углах —катионы.
Кристаллическая
решетка Cs+J-
представляет собой сочетание двух
простых кубических решеток: решетки
иона Cs+
и решетки иона
J-,
вдвинутых одна в другую так, что в центре
куба находится; ион
йода, а в углах — ионы Cs+.
Эта решетка центрирована в пространстве
так, что в центре куба находится анион,
а в углах —катионы.
Кристаллическая решетка Ca2+F2- типична для многих тройных электролитов. Здесь ионы Са2+ образуют кристаллическую, центрированную в гранях, решетку, ионы же F- расположены в серединах восьми маленьких кубов, на которые может быть разложен большой куб.
В ионных кристаллических решетках отдельные места могут занимать сложные и комплексные ионы. Примеры: решетка нитрата натрия Na+NO3- (pис 9, а) и решетка гексахлороплатината калия K+[PtCl6]2- (рис. 9,б). Здесь отдельные места занимают ионы: Na+, К+, NO3-, [PtCl6]2-.
В кристаллической решетке нитрата натрия каждый ион NO3- занимает одно место, причем в центре тетраэдра — атом азота N+5, а в углах — атомы кислорода О; атомы сближены друг с другом и составляют прочную, крепко стянутую группу.






Ионы [PtCl6]2- занимают углы кубической, центрированной в гранях, кристаллической решетки. Ионы К+ составляют куб.
Молекулярные решетки. В молекулярных решетках отдельные места занимают молекулы. Примером молекулярных решеток соединений, которые рассматриваются в неорганической химии, могут служить кристаллические решетки окиси алюминия (рис. 10, а) и двуокиси углерода СО2 (рис. 10,6). В кристаллической решетке окиси алюминия Аl2Оз углы ромба с длиной ребра αo = 5,12А занимают близко расположенные друг к другу группы атомов, образующие нейтральную молекулу.
В кристаллической, центрированной в гранях, решетке двуокиси углерода отдельные места занимают нейтральные молекулы СО2, очень сближенные группы из трех атомов С и 2О, сгруппированные так, как это показано на рис. 10.

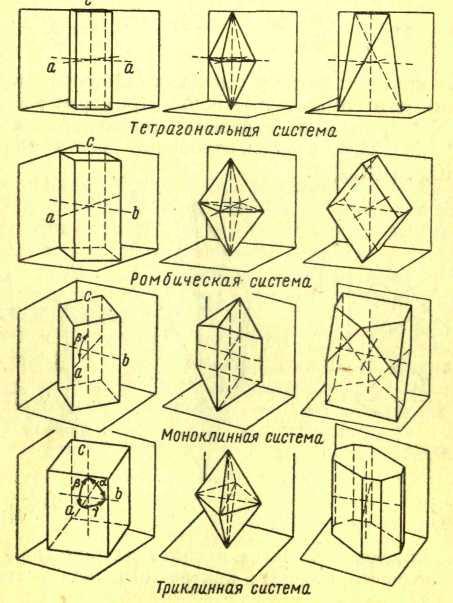
Рис.5
Металлические решетки. Металлические решетки характеризуются особыми свойствами, отличающими их от других типов кристаллических решеток. В узлах металлических решеток находятся не атомы, а положительные ионы. Внешние электроны атомов металлов свободно мигрируют внутри кристаллической решетки, переходя от одного иона к другому, т. е. ведут себя подобно молекулам газа, поэтому всю совокупность электронов в кристаллической решетке металлов называют


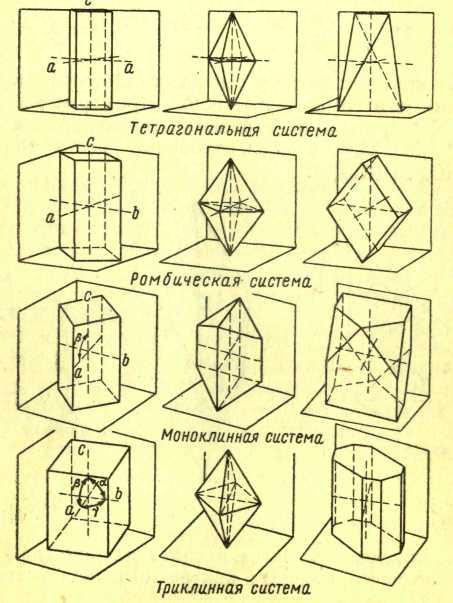


Рис.8 Рис.9



Рис. 10 Рис.11
электронным газом. Таким образом, металлическую решетку можно рассматривать как ионную решетку, находящуюся в «атмосфере» электронного газа из внешних электронов. Такова, например, решетка металлического натрия (рис. 11). Характерные свойства металлов — электропроводность и теплопроводность, в частности, зависят от передвижения электронов внутри решетки. Под воздействием внешнего электрического поля валентные электроны, число которых у атомов металлов невелико (1, 2 или 3), перемещаются в направлении поля, создавая электрическую проводимость.
