
Система: 1 — вода—кварц, 2 — вода—гидрофильная пористая среда, 3 — кварц—сСl; 4— кривая, рассчитанная по формуле (22)
Позднее 3. М. Товбина [61], используя изменения эффективного коэффициента диффузии растворенных веществ, рассчитала вязкость водных растворов в гидрофильных пористых средах и установила резкое возрастание ее по мере уменьшения радиусов капилляров, начиная с r=10-8 м. Затем 3. М. Зорин, В. Д. Соболев и Н. В. Чураев выполнили измерения вязкости воды и неполярного четыреххлористого углерода (ССl4) на кварцевых капиллярах радиусами r=(1— 0,05) ∙10-6 м [26]. Для неполярного четыреххлористого углерода (ССl4) не обнаружено изменения вязкости при уменьшении радиуса капилляров вплоть до 0,05 ∙10-6 м. Для воды отмечено увеличение вязкости на 35 — 40% при снижении х до 0,05∙10-6 м; при этом получена формула для определения изменения вязкости воды в зависимости от радиуса капилляров:
![]()
где hн = 8∙10-9 м—толщина поверхностного слоя, не участвующего в течении жидкости при заданных градиентах давления.
Выражение (24) практически аналогично уравнению (22) при среднем значении n = 2. Сопоставление экспериментальных данных указанных выше авторов с эмпирической кривой, рассчитанной по (22), свидетельствует о их хорошей сходимости (рис. 4). Для расчетов средней эффективной вязкости связанного электролита в пленке может быть принято выражение (23).
Электропровод но ст ь. Попытки теоретически и эксперементально исследовать электропроводность связанной воды в тонких пленках и тонкодисперсных системах делались многими авторами [25, 32, 34, 48]. В результате этих работ получены первые сведения об удельной электропроводности связанной воды связанныx растворов электролитов. Нами впервые предложено аналитическое выражение для электропроводности пленки связанной воды [32].
Аномальная электропроводность связанного раствора электролита χс обусловлена, во-первых, изменением концентрации ионов в его пленке и, во-вторых, уменьшением их подвижности на внешней части двойного электрического слоя. В болыпинстве случаев полагают, что концентрация ионов в указанном …….подчиняется экспоненциальному соотношению Больцмана и показывает решающее влияние на изменение удельной электропроводности связанного раствора в случае малой его минерализации. Подвижность ионов пропорциональна скорости их движения, которая зависит от действующей на ионы движущей силы электрического поля, сопротивления среды, определяющейся ее вязкостью, и электрических сил, зависящих от величины заряда поверхности минеральной частицы и степень взаимодействия между гидратированными ионами.
Зависимость электропроводности связанного раствора электролита от толщины его слоя можно установить, используя закон изменения подвижности ионов по толщине пленки связанной воды.
Пусть
ион
заряда
еzi
движется под действием внешнего
электрического
поля напряженностью Е
в
слое связанной воды,
имеющей
среднюю
вязкость растворителя
![]() и среднюю
диэлектрическую проницаемость εв
св
со скоростью vi.
Вектор
разряженности
внешнего электрического поля составляет
угол с нормалью
к поверхности раздела твердая минеральная
частица – раствор электролита.
Эта поверхность раздела принимается
плоской.
и среднюю
диэлектрическую проницаемость εв
св
со скоростью vi.
Вектор
разряженности
внешнего электрического поля составляет
угол с нормалью
к поверхности раздела твердая минеральная
частица – раствор электролита.
Эта поверхность раздела принимается
плоской.
С![]() огласно,
закону движения частиц уравнение
движения иона
огласно,
закону движения частиц уравнение
движения иона
где
m
- масса
иона;
![]() —
результирующая сила, действующая на
ион; dvi/dτ
— ускорение; τ — время движения иона.
—
результирующая сила, действующая на
ион; dvi/dτ
— ускорение; τ — время движения иона.
При движении иона на него действуют следующие силы.
1. Сила внешнего электрического поля
![]()
2. Тормозящая
сила за счет трения, вызванного
средой с ВЯЗКОСТЬЮ
![]() ,
,
![]()
где
ki=6π![]() r
— коэффициент трения, определяющийся
формулой
Стокса1;
r—радиус
гидратированного иона.
r
— коэффициент трения, определяющийся
формулой
Стокса1;
r—радиус
гидратированного иона.
3![]() . Тормозящие
силы, обусловленные электростатичесим
взаимодействием
между подвижными ионами: сила
релаксацп
онного
эффекта fр
и электрофоретическая сила fa:
. Тормозящие
силы, обусловленные электростатичесим
взаимодействием
между подвижными ионами: сила
релаксацп
онного
эффекта fр
и электрофоретическая сила fa:
В![]() еличина
χ зависит от концентрации электролита
Св,
его типа
(zi),
природы растворителя (εв
cв),
температуры Т
и
определяется
формулой1:
еличина
χ зависит от концентрации электролита
Св,
его типа
(zi),
природы растворителя (εв
cв),
температуры Т
и
определяется
формулой1:
![]()
здесь
г![]() де
де
zk и za - валентности катиона и анниона; lk и la – их эквивалентные электропроводности.
В выражении (29) для релаксационной силы торможения учитывается также и тепловое движение частиц.
4. Электрическая сила ионно-электростатического поля, определяющаяся уравнениями (18) и (19).
Н![]() айдем
результирующую силу
айдем
результирующую силу
![]() .
Для
простоты полагаем, что
все рассмотренные силы действуют в
одной плоскости и по прямой;
тогда
.
Для
простоты полагаем, что
все рассмотренные силы действуют в
одной плоскости и по прямой;
тогда
1 Строго говоря, формула Стокса справедлива для движения шарика, радиус которого велик по сравнению с радиусом молекул среды. В данном случае можно полагать, что и для гидратированного иона, который по размеру больше молекулы воды, скорость движения должна возрастать с увеличением движущей силы и уменьшаться с увеличением радиуса частицы.
Подставив выражения (18), (26), (27), (28), (29) в (30), получим
![]()
Г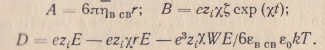 де
де
Умножая и деля на dх левую часть уравнения (31) и считая, что dx/dτ=vx’ с учетом (25) имеем
Это нелинейное дифференциальное уравнение первого порядка. В общем виде оно, по-видимому, не может быть решено в элементарных функциях. X. Лемке исследовал вид решений для подобного типа вблизи точки х = 0 с разложений в ряды [32].
Из уравнения (32) находим максимальное значение функции…..т.е. когда vx’ = 0
![]()
Это условие выполняется для достаточно больших значений и при этом ехр(—χх)→0 ,а скорость иона не зависит от координаты х. Из уравнения (33) находим условие неподвижности иона, т.е. когда v = 0
![]()
Из формулы (34) определяем значение хо, при котором скорость иона равна нулю (в случае α = 0):
![]()
Чтобы
избежать весьма сложных и громоздких
вычислений при
решении уравнения (32), предполагаем
движение иона в щи
связанной воды толщиной h
= х—х0
равномерным,
т. е. ;
п.|,
и на ион действует средняя сила
![]() ионно-электростатического поля,
определяемая по формуле (19).
ионно-электростатического поля,
определяемая по формуле (19).
В соответствии с (19), (32) и (34) выражение для среднего эффективного значения абсолютной скорости иона принимает
в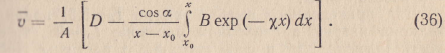 ид
ид
Подвижность иона l равна произведению абсолютной скорости иона vо на число Фарадея F, т. е.
![]()
здесь v0 — скорость иона при Е= 1 В/см.
Средняя
эффективная подвижность
![]() ионов в двойном электрическом
слое толщиной hв
св=х—х0
с
учетом ионно-электростатического
поля на основании (36) будет
ионов в двойном электрическом
слое толщиной hв
св=х—х0
с
учетом ионно-электростатического
поля на основании (36) будет
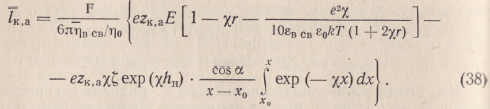
Принимая во внимание выражение (38), после интегрирования (23) при п = 2 получим
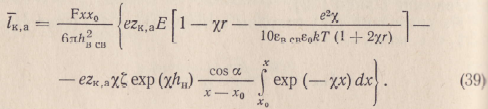
На
рис. 5 приведена зависимость подвижности
катиона Na+
от
его расстояния до поверхности твердой
фазы породы для различных
минерализаций раствора NаС1
при t
= 25° С, рассчитанная по формуле (39). Из
рис. 5 следует, что подвижность катионов
в слое связанной воды при приближении
к поверхности
минерала заметно уменьшается и в слое
прочно связанной
воды ( hв
псв
= 0,07∙10-7
м) в десятки и сотни раз меньше его
подвижности в свободном растворе.
Сравнение средних эффективных
подвижностей катиона Nа+,
рассчитанных по формуле
(39) для случаев α = 0° и α = 90°, показывает,
что существенное
расхождение между ними наблюдается
при х≤0,1∙10-7
м, т. е. на таком расстоянии, где
ионно-электростатическая сила оказывает
заметное влияние на катион (рис. 6). Для
х≤0,1∙10-7
м
значения
![]() практически одинаковы для α = 0° и
α
=90°. В этом случае для расчетов
практически одинаковы для α = 0° и
α
=90°. В этом случае для расчетов
![]() можно
использовать, более
простое выражение
можно
использовать, более
простое выражение
![]()
в котором не учитывается влияние на катион ионно-электростатической силы.
Для
приведенного выше примера
![]() = 5,5; подвижность
же катиона
натрия в свободном растворе lко
= 31, т.е. подвижность
же катиона Nа+ в слое связанного
раствора NаCV
приблизительно в
5,7
раза меньше его подвижности в свободном
растворе. Величина
= 5,5; подвижность
же катиона
натрия в свободном растворе lко
= 31, т.е. подвижность
же катиона Nа+ в слое связанного
раствора NаCV
приблизительно в
5,7
раза меньше его подвижности в свободном
растворе. Величина
![]() в слое прочно связанного раствора
примерно в 30 раз
меньше lко
.
в слое прочно связанного раствора
примерно в 30 раз
меньше lко
.
Исследования Д. А. Фридрихсберга, проведенные на керамических диафрагмах по изучению зависимости между обменной адсорбцией и поверхностной проводимостью, показали, что средняя эффективная подвижность катиона калия в двойном электрическом слое в 100 раз меньше, чем в свободном растворе КСl. В.С. Шаров на основании опытов по электролизу в глинистом тесте установил, что подвижность ионов Са2+ и Сu2+ в двойном электрическом слое примерно в 20 раз меньше, чем в свободном растворе. Б.Ю. Вендельштейн, исходя из опубликованных данных, определяет среднюю эффективную подвижность катиона в двойном электрическом слое равенством
![]()
где lк0 и lа0 - подвижности катиона и аниона в свободном растворе.
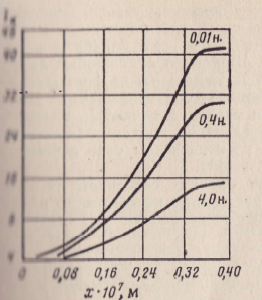
Рис.5. Подвижность tк катиона Na+ на внешней части двойного электрического слоя в зависимости от его расстояния х от твердой фазы породы (Шифр кривых - Св)
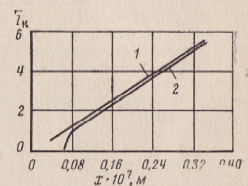
Рис.
6. Средняя эффективная' подвижность
![]() катиона
Nа+
в двойном
электрическом слое в зависимости
от его расстояния х
от
твердой
фазы породы.
катиона
Nа+
в двойном
электрическом слое в зависимости
от его расстояния х
от
твердой
фазы породы.
1 — α=90°: 2 — α = 0. Минерализация раствора электролита Св=0,4 н.
Таким
образом, анализ полученных нами
результатов и опубликованных данных
о подвижности катионов в двойном
злектрическом слое
показывает, что ионы прочно и рыхло
связанного раствора имеют существенно
разные средние эффективные
подвижности,
которые в несколько раз меньше
подвижностей
в свободном растворе, и что величины
установленных подвижностей
в двойном электрическом слое по данным
различных
авторов весьма различаются. Наиболее
близки к нашим результатам
определения В. С. Шарова и обобщенные
данные Б.
Ю. Вендельштейна. Значения
![]() ,
найденные
по формуле (39), примерно
в 3 раза больше величин
,
найденные
по формуле (39), примерно
в 3 раза больше величин
![]() ,
полученных_В. С. Шаровым,
и приблизительно в 3 раза меньше значения
,
полученных_В. С. Шаровым,
и приблизительно в 3 раза меньше значения
![]() ,
вычисленных
по формуле (41). Для определения средней
эффективной подвижности
ионов в двойном электрическом слое
рекомендуется использовать формулы
(39) и (40).
,
вычисленных
по формуле (41). Для определения средней
эффективной подвижности
ионов в двойном электрическом слое
рекомендуется использовать формулы
(39) и (40).
Удельная
электропроводность пленки связанного
раствора электролита
в зависимости от расстояния исследуемого
объема жидкости
от твердой поверхности на основании
(37) выразится с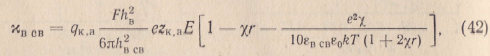 оотношением
оотношением
где qк,а — концентрация катионов или анионов двойного электрического слоя, зависящая от сорбционных свойств твердой минеральной поверхности.
С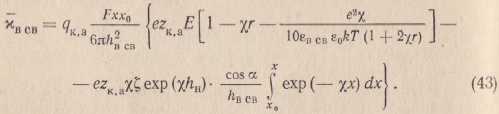 редняя
эффективная электропроводность пленки
связанной воды
толщиной hв
св
= х —
х0
на
основании (39) равна
редняя
эффективная электропроводность пленки
связанной воды
толщиной hв
св
= х —
х0
на
основании (39) равна
В
случае разбавленных растворов (СВ→0)
в соответствии с элекропроводность
связанной воды
![]() превышает проводимость
воды свободной χ0
за счет существенного преобладания
концентрации
ионов в двойном электрическом слое по
сравнению с объемным раствором
(qк.а»Cв),
несмотря на то, что подвижность
ионов двойного электрического слоя
меньше их подвижности
в свободном растворе. Это положение
подтверждается
экспериментально. Д. А. Фридрихсберг
установил, что при
Св→0
превышает проводимость
воды свободной χ0
за счет существенного преобладания
концентрации
ионов в двойном электрическом слое по
сравнению с объемным раствором
(qк.а»Cв),
несмотря на то, что подвижность
ионов двойного электрического слоя
меньше их подвижности
в свободном растворе. Это положение
подтверждается
экспериментально. Д. А. Фридрихсберг
установил, что при
Св→0
![]() составляет 75% всей удельной
электропроводности
капилляров определенного радиуса. В
случае растворов
составляет 75% всей удельной
электропроводности
капилляров определенного радиуса. В
случае растворов
высокой концентрации qк.а<Cв ПОДВИЖНОСТЬ ИОНОВ ДВОЙНого
электрического
слоя меньше их подвижности в свободом
растворе,
поэтому согласно формулам (42) и (43)
электропроводность
связанного раствора меньше электропроводности
свободного,
т. е.
![]() <
χ0.
Следует ожидать, что при каких-то
минерализациях
равновесного раствора средняя эффективная
электропроводность
двойного электрического слоя приблизительно
равна проводимости
объемного электролита, т.е. χв
св
≈ χ0.
Этот
диапазон
<
χ0.
Следует ожидать, что при каких-то
минерализациях
равновесного раствора средняя эффективная
электропроводность
двойного электрического слоя приблизительно
равна проводимости
объемного электролита, т.е. χв
св
≈ χ0.
Этот
диапазон
минерализаций, установленный нами экспериментально для полИМИКТОВЫХ терригенных пород месторождений Западной Сибири, находится в пределах 0,13—0,4 н. [27]. Об изменении электропроводности поверхностной жидкой фазы с расстоянием от поверхности твердой фазы свидетельствуют непосредственные измерения толщин пленок связанной воды
и их проводимостей, выполненные В. Д. Перевертаевым и
М.С. Мециком [55]. Ими установлено экспоненциальное изменение электропроводности поверхностных водных слоев толщиной 1,5∙10-9 - 20∙10-9 м, расположенных между кристаллом слюды и воздушными водными парами (рис. 7). Удельная электропроводность χв св поверхностного слоя толщиной hв св
определяется эмпирической формулой
![]()
где χч электропроводность твердой гидратированной минеральной частицы; β — коэффициент, зависящий от физико-химических свойств твердой и жидкой фаз (для слюды χч = 0,54∙10-5 См/м; β = 0,98∙108 м).
Сравнение теоретической формулы (43) с эмпирической (44) показывает их идентичность в изменении электропроводности связанной воды по экспоненциальному закону в зависисимости от толщины ее пленки.
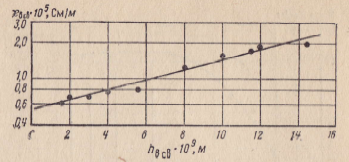
Рис. 7. Зависимость удельной электропроводности связанной воды χв св от толщины ее пленки hв св (по В.Д. Перевертаеву, М.С. Мецику [55] ).
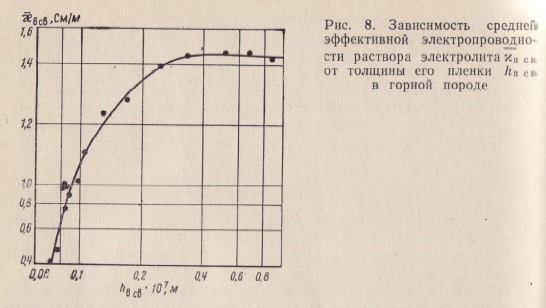
Зависимость электропроводности связанного раствора электролита от толщины его пленки hв св, установленная по измерениям на образцах горных пород, носит более сложный характер (рис.8).
.
Диэле к т р и ч е с к а я проницаемость. Связанная вода обладает значительно меньшей диэлектрической проницаецаемостью по сравнению с водой свободной. Это обусловлено тем, что молекулы воды, находящиеся под действием ван-дер-ваальсовых молекулярных сил притяжения, ионно-электростатической силы твердой поверхности минералов, диффузных ионов и сил водородных связей, лишены свободы переориентации даже в полях сравнительно невысоких частот. По мере утоньшения

пленки связанной воды наблюдается вырождение дипольно-ориентационной поляризации молекул [48, 49].
Экспериментальными данными установлено, что диэлектрическая проницаемость εв св связанной воды при малых влажностях составляет 2—2,5, т. е. отличается от ε0 воды свободной приблизительно в 32—40 раз. По опытным данным И. В. Жиленкова при количестве связанной воды в дисперсной системе не более 0,08% εв св = 6÷8.
Непосредственные измерения диэлектрической проницаемости водных пленок известной толщины осуществлены М. С. Мециком и др. [48, 49]. Толщина пленок, заключенных между двумя объемными фазами, состоящими из кристаллов слюды, изменялась от 0,7∙10-7 до 37∙10-7 м. При hв св =0,7∙10-7 м диэлектрическая проницаемость εв св пленки составляет 4,5; при hв св ≥ 15∙10-7 м она приблизительно равна 80, т. е. не отличается от диэлектрической проницаемости воды в объеме (рис. 9).
На основании экспериментальных данных М. С. Мецика нами установлены формулы изменения диэлектрической проницаемости в зависимости от расстояния х и толщины пленки hв св. Диэлектрическая проницаемость связанной воды в зависимости от расстояния х определяется эмпирическим уравнением
![]()
здесь ε0≈80 диэлектрическая проницаемость объемной воды при температуре опыта; А — постоянная, численно равная отношению hв св /х, при котором диэлектрическая проницаемость εв св поверхностной фазы практически не отличается от ε0 объемам водной фазы; в данном случае А= 6,9; hв св — вероятно максимальная толщина пленки связанной воды; х — толщина пленки связанной воды при данном водонасыщении; n — показатель степени, равный для условий опыта 1,38.
Формула (45) справедлива для диапазона изменения отношения hв св /х от 6,9 до 60 (рис. 10).
К![]() оэффи
ц и е н т диффузии. Аномальные
физико-химические свойства
поверхностных фаз оказывают также
существенное влияние на величину
диффузии в них ионов и молекул. На
основании
экспериментальных
данных 3. М. Товбиной [61] по изучению
эффективного
коэффициента диффузии
оэффи
ц и е н т диффузии. Аномальные
физико-химические свойства
поверхностных фаз оказывают также
существенное влияние на величину
диффузии в них ионов и молекул. На
основании
экспериментальных
данных 3. М. Товбиной [61] по изучению
эффективного
коэффициента диффузии
![]() веществ в пористых средах с глобулярной
структурой и наших исследований по
определению
вязкости связанной воды получено
уравнение для среднего
эффективного коэффициента диффузии
вещества D
в пленке
связанной воды
веществ в пористых средах с глобулярной
структурой и наших исследований по
определению
вязкости связанной воды получено
уравнение для среднего
эффективного коэффициента диффузии
вещества D
в пленке
связанной воды
Г![]() де
D0
– коэффициент свободной диффузии
вещества в объемной фазе;
В – коэффициент, определяемый
пористостью среди kп:
де
D0
– коэффициент свободной диффузии
вещества в объемной фазе;
В – коэффициент, определяемый
пористостью среди kп:
С – коэффициент, зависящий от отношения размеров гидратированных ионов или молекул диффундирующего вещества r и радиусов поровых каналов rк или толщин водных пленок:
![]()
29
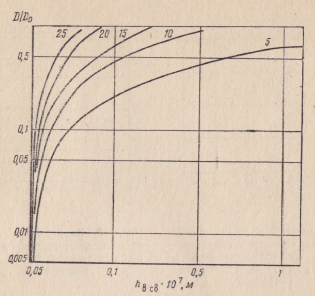
Рис. 11. Зависимость отношения коэффициентов диффузии вещества D/D0 от толщины пленки связанной воды
hв св. Шифр кривых — кп горной породы в %.
Из формулы (46) следует, что с уменьшением толщины водного слоя или же с увеличением отношения r/rк коэффициент диффузии уменьшается (рис. 11).
Теплопроводность. Аномальная теплопроводность поверхностных водных пленок между двумя объемными фазами слюды изучена экспериментально М. С. Мециком [48] и Г.Т. Тимощенко. Ими установлено, что теплопроводность λв св воды в тонких пленках увеличивается от 0,6 до 60 Вт/(моль °С) в зависимости от уменьшения толщины водных слоев от 10- 6 до 0,05∙10-6 м. При этом теплопроводность связанной воды на два порядка превышает теплопроводность свободной воды и оказывается близкой к теплопроводности металлов. Выяснено, что теплопроводность пленок связанной воды резко падает до ее объемной теплопроводности с увеличением температуры в интервале 50—60° С. Для неполяриых жидкостей (четыреххлористый углерод, трансформаторное масло) аномальной теплопроводности в тонких пленках не отмечено; также не зафиксировано аномальной теплопроводности в тонких пленках, расположенных между гидрофобными объемными фазами полиэтиленовые пластинки (рис. 12).
Нами на основе экспериментальных данных М. С. Мецика и Г.Т. Тимощенко получены эмпирические формулы, характеризующие изменение теплопроводности λв св связанной воды с изменением толщины водных пленок:
![]()
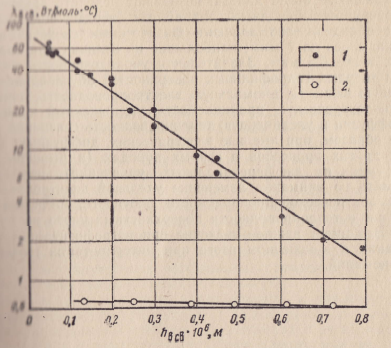
Рис. 12. Зависимость теплопроводности связанной воды λв св от толщины пленки hв св (по М. С. Мецику и Г. Т. Тимощенко).
1 - вода—слюда; 2 — вода—полиэтиленовые пластинки
где λ0 – теплопроводность свободной воды, равная при t = 20° С ..Вт/(моль °С); hв св — вероятно максимальная толщина пленки связанной воды, при которой наблюдается аномальная тепплопроводность (координата внешней границы пленки); А =, k =5,1.
Средняя
эффективная теплопроводность
![]() пленки связанной воды
толщиной hв
св
= х—х0
на основании (47) выразится отношением
пленки связанной воды
толщиной hв
св
= х—х0
на основании (47) выразится отношением
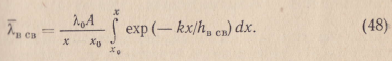
После интегрирования (48)
![]()
где х0=7,5∙10-10 м — расстояние, на котором расположен от жидкой поверхности минерала мономолекулярный слой прочно связанной воды.
Изложенные выше данные позволяют сделать заключение, что поверхностные водные слои вблизи твердых минеральных частиц обладают аномальными физическими свойствами при толщине слоев до 1 мкм; наибольшие их отличия при толщине пленок менее 0,5 мкм. Значительная упорядоченность молекул вблизи твердых гидрофильных поверхностей обусловливает повышенную вязкость, аномальную электропроводность, пониженную диэлектрическую проницаемость, уменьшенный коэффициент диффузии и увеличенную теплопроводность связанной воды. Таким образом, при анализе электрических, диффузных, тепловых и других процессов в горных породах (и решении соответствующих им дифференциальных уравнений) необходимо принимать во внимание изменение удельной электропроводности, диэлектрической проницаемости, плотности, коэффициентов диффузии и теплопроводности поверхностных слоев по их толщине. Это имеет важное значение при петрофизическом моделировании и в конечном итоге при интерпретации геофизических аномалий.
