
- •Кинетика гидролиза сахарозы
- •Общие сведения
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Определение порядка и константы скорости реакции
- •Зависимость скорости реакции от температуры
- •Зависимость скорости реакции от присутствия катализатора
- •Поляриметрический метод
- •Полутеневой поляриметр
- •Реакция гидролиза сахарозы
- •Методика выполнения работы Порядок проведения эксперимента
- •Обработка результатов эксперимента
- •Вопросы к лабораторной работе №1
- •Перегонка
- •Общие сведения
- •Давление пара над бинарными жидкими смесями
- •Температуры кипения бинарных жидких смесей
- •Рефрактометрический метод
- •Рефрактометр Аббе
- •Методика измерения показателей преломления
- •Методика проведения работы Порядок проведения эксперимента
- •Обработка результатов эксперимента
- •Вопросы к лабораторной работе №2
- •Коэффициент распределения
- •Общие сведения
- •Распределение растворённого вещества между двумя несмешивающимися растворителями
- •Экстракция
- •Титриметрический метод
- •Методика проведения работы Порядок проведения эксперимента
- •Обработка результатов эксперимента
- •Вопросы к семинарскому занятию №3
Реакция гидролиза сахарозы
Сахароза представляет собой дисахарид, при гидролизе молекулы которого образуется молекула глюкозы и фруктозы:
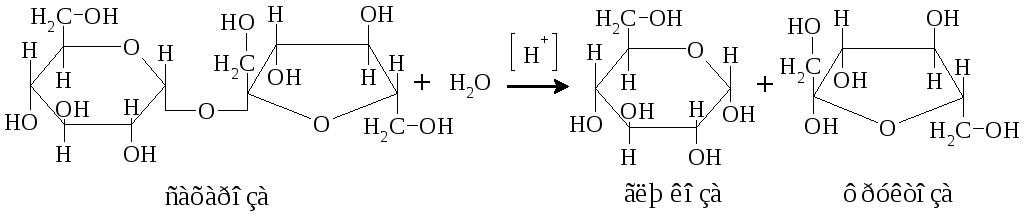
Реакция гидролиза катализируется кислотами и ферментами. В присутствии фермента b-фруктофуранозидазы энергия активации реакции снижается с 134кДж до 39кДж.
Сахароза является правовращающим веществом, т.е. её > 0, а суммарное удельное вращение глюкозы и фруктозы оказывается отрицательным. Таким образом, в процессе гидролиза происходит изменение знака угла вращения с положительного на отрицательный (инверсия). По этой причине реакцию гидролиза сахарозы называют также реакцией инверсии сахарозы.
Реакция инверсии сахарозы является каталитической реакцией. Роль катализатора играют ионы водорода, источником которых может служить любая сильная кислота.
В процессе реакции исходная концентрация сахарозы (c0) уменьшается и к моменту времени t составляет величину c1, при этом концентрации глюкозы и фруктозы возрастают и становятся равными c2 и c3 соответственно. Из уравнения реакции следует, что из одного моля сахарозы образуется один моль глюкозы и один моль фруктозы, следовательно, концентрации глюкозы и фруктозы будут одинаковыми и равны концентрации, вступившей в реакцию сахарозы: c2 = c3 = c0 – c1.
После полного завершения реакции (условно это состояние обозначается символом ∞) концентрация сахарозы станет равна 0, а концентрации глюкозы и фруктозы – исходной концентрации сахарозы: c2 = c3 = c0.
Протекание реакции сопровождается изменением угла вращения плоскости поляризации с 0 вначале реакции до ∞ после полного вступления в реакцию всей исходной сахарозы (таблица 1.).
Таблица 1.1. Изменение концентрации реагирующих веществ и продуктов реакции и угла вращения плоскости поляризации во времени
|
Время протекания реакции |
Концентрации |
Угол вращения плоскости поляризации |
||
|
сахарозы (1) |
глюкозы (2) |
фруктозы (3) |
||
|
0 |
c0 |
0 |
0 |
0 = 1∙c0∙l |
|
t |
c1 |
c2 = c0 – c1 |
c3 = c0 – c1 |
t = [1∙c1+(2+3)(c0 – c1)]∙l |
|
∞ |
0 |
c0 |
c0 |
∞ = (2+3)∙c0∙l |
Каждый компонент раствора вносит свой вклад в величину угла вращения плоскости поляризации: сахароза – 1, глюкоза – 2, фруктоза – 3. На основании правила аддитивности запишем выражение для суммарного угла вращения :
= 1 + 2 + 3 = (1∙c1 + 2∙c2 + 3∙c3)∙l
где: 1, 2 и 3 – удельные вращения угла плоскости поляризации сахарозы, глюкозы и фруктозы соответственно. С учетом таблицы 1.1, в начальный момент:
0 = 1∙c0∙l ,
к моменту времени t:
t = [1∙c1 + 2(c0 – c1) + 3(c0 – c1)]∙l = [1∙c1 + (2 + 3)(c0 – c1)]∙l ,
а в конце реакции:
∞ = (2 + 3)∙c0∙l
Из вышесказанного следует, что:
0 – ∞ = 1∙c0∙l – (2 + 3)∙c0∙l = [1 – (2 + 3)]∙c0∙l ,
и
t – ∞ = 1∙c0∙l – [1∙c1 + (2 + 3)(c0 – c1)]∙l = [1 – (2 + 3)]∙c1∙l
Таким образом, получается, что разность t – ∞ пропорциональна концентрации сахарозы, и:
![]()
Подстановка полученного выражения в кинетическое уравнение реакции I-го порядка даёт результат:
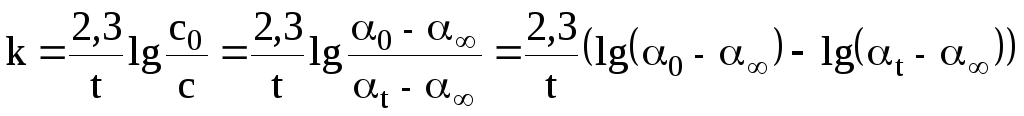 (3)
(3)
После приведения к линейному виду получим:
![]()
Таким образом, для реакции I-го порядка зависимость lg(t – ∞) = f (t) должна носить линейный характер. Величина lg(0 – ∞) может быть получена экстраполяцией этой зависимости на t = 0.
Реакция гидролиза сахарозы находит практическое применение при производстве помадных конфет. В этом процессе гидролиз сахарозы катализируется ферментом инвертазой. Образующаяся фруктоза обладает высокой гигроскопичностью (способностью поглощать воду), что препятствует высыханию и черствению помады. Кроме того фруктоза придаёт помаде дополнительную сладость поскольку является значительно более сладким сахаром, чем сахароза.
