
- •4.2.3.Основное уравнение молекулярно-кинетической теории
- •4.2.4.Внутренняя энергия идеального газа.
- •4.2.4.1. Число степеней свободы молекулы
- •4.2.4.2.Теорема о равнораспределении энергии по степеням свободы молекулы
- •4.2.4.3.Внутренняя энергия идеального газа
- •4.3.1.2.Термодинамическая система
- •4.3.1.3.Термодинамические параметры.
- •4.3.1.4. Равновесное состояние. Равновесные процессы.
- •4.3.2.2. Законы и уравнения термодинамики идеального газа
- •4.3.3. Внутренняя энергия термодинамической системы.
- •4.3.4.Первое начало термодинамики.
- •4.3.5.Теплоемкость идеального газа.
- •4.3.5.1.Понятие теплоемкости.
- •4.3.5.2. Изохорическая теплоемкость.
- •4.3.5.3. Изобарическая теплоемкость.
- •4.3.5.4.Теплоемкость в других изопроцессах
- •4.3.5.5.Трудности классической теории теплоемкости.
- •4.4.5.2.Изобарический процесс
- •4.7.Конденсированное состояние вещества.
- •4.7.1.Жидкости
- •4.7.2.Поверхностное натяжение
- •4.7.3.Смачивание. Капиллярные явления
4.4.5.2.Изобарический процесс
Для изобарического процесса
P= const → δQ= dU+ δA = νCV·dT + νRdT = νCРdT
Q = νCР·ΔT (4.4.16)
4.4.5.3.Изотермический процесс
Для изотермического процесса
T= const → dT=0 → dU=0 → δQ = δA
Q=A=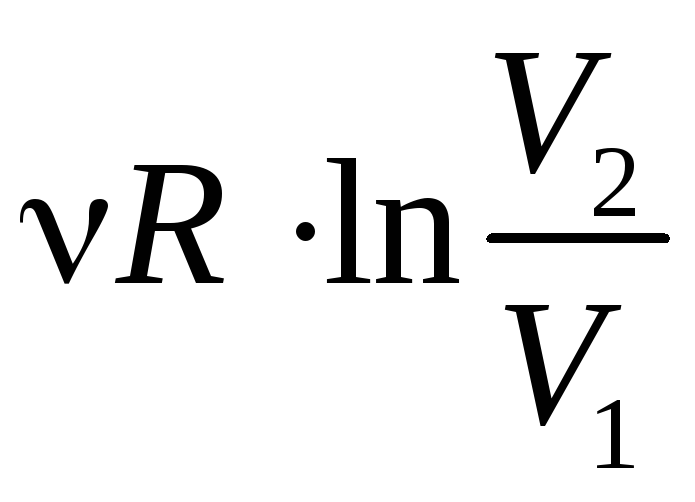 (4.4.17)
(4.4.17)
4.4.5.4. Адиабатический (изэнтропический) процесс
Для адиабатического (изэнтропического) процесса
S=const
![]() δQ = 0 → δA = - dU
δQ = 0 → δA = - dU
![]() (4.4.17)
(4.4.17)
4.7.Конденсированное состояние вещества.
4.7.1.Жидкости
Область существования вещества в жидком состоянии ограничена со стороны высоких температур переходом его в газообразное состояние, а со стороны низких температур — переходом в твердое состояние — кристаллизацией.
По своим физическим свойствам жидкости занимают промежуточное положение между газами и твердыми телами. Жидкости, как и твердые тела, способны сохранять свой объем и у них существует свободная поверхность. В то же время жидкости, подобно газу, принимают в поле силы тяжести форму того сосуда, в который они налиты. Как и газы, жидкости обладают текучестью, а подобно твердым телам, они имеют очень малую сжимаемость и способны сопротивляться растяжению.
Малая сжимаемость жидкостей обусловлена тем, что им присуще довольно сильное межмолекулярное взаимодействие. Поэтому в жидкости даже небольшое уменьшение взаимных расстояний между молекулами приводит к появлению больших сил отталкивания. Коэффициент сжимаемости жидкостей, характеризующий относительное изменение объема жидкости при увеличении внешнего давления на единицу, изменяется в пределах от 2·10-1 до 2·10-2 Па. Так, например, для воды он равен 4,53·10-1 Па. С увеличением давления коэффициент сжимаемости жидкости уменьшается, так как по мере того как жидкость сжимается, уменьшаются расстояния между ее молекулами и увеличиваются силы отталкивания между ними. Это и затрудняет дальнейшее сжатие жидкости.
Наоборот, с повышением температуры коэффициент сжимаемости возрастает, так как при нагревании объем жидкости, а, следовательно, и расстояние между ее молекулами увеличиваются. При этом силы отталкивания между молекулами уменьшаются, и сжатие жидкости облегчается.
Изучение рассеяния рентгеновских лучей, нейтронов и электронов в жидкости показывает, что ближайшие соседи каждой молекулы жидкости располагаются в определенном порядке, образуя структуру, сходную со структурой твердого тела. Однако уже на расстояниях порядка трех-четырех молекулярных диаметров сходство утрачивается. Это и послужило основанием к употреблению для жидкости термина ближний порядок в. отличие от дальнего порядка, имеющего место в кристаллах. Было также, установлено, что с повышением температуры упорядоченность в расположении соседних молекул жидкости постепенно уменьшается и, слёдовательно, их расположение становится все более хаотическим.
Промежуточное положение жидкости между газами и твердыми телами проявляется в том, что эти оба состояния являются предельными для вещества в жидком состоянии. Именно с этим и связана особая сложность свойств жидкого состояния вещества и те большие трудности, которые возникают при разработке его теории.
При изучении свойств жидкости используют по существу средние величины такие, как, например, средняя энергия взаимодействия молекул и средняя энергия их теплового движения, среднее взаимное расположение частиц жидкости и т. п. Это привело к применению статистических методов для описания тех или иных свойств жидкости и к разработке статистической теории жидкости.
Однако при использовании статистической теории для расчета свойств жидкостей возникают большие трудности в учете межмолекулярных взаимодействий в конкретных жидкостях.
Тепловое движение в жидкости, вдали от критической точки, имеет следующий характер. Каждая молекула в течение некоторого времени колеблется около определенного положения равновесия. Затем скачком перемещается в новое положение равновесия, отстоящее от предыдущего на расстоянии, примерно равном размеру самой молекулы. Таким образом, молекулы лишь медленно перемещаются внутри жидкости, пребывая часть времени около определенных мест, находясь в «оседлом» состоянии. Среднее время «оседлого» существования молекул называют временем релаксации. Оно резко убывает с повышением температуры жидкости, при этом подвижность молекул сильно возрастает.
При перескоке молекулы из одного временного положения равновесия в другое нарушаются ее связи с соседними молекулами, и, следовательно, затрачивается энергия. Иначе говоря, при перескоке в новое временное положение равновесия молекула должна преодолеть потенциальный барьер высотой, создаваемый взаимодействием ее со старыми соседями. Эту минимальную энергию, необходимую для перемещения молекулы в новое временное положение равновесия, называют энергией активации W. Средняя кинетическая энергия молекул жидкости, обусловленная их тепловым движением, не намного меньше энергии активации, поэтому благодаря флуктуациям она в некоторые моменты времени оказывается достаточной для того, чтобы молекула смогла перескочить в новое временное положение равновесия.
Среднее
время релаксации
![]() связано с энергией активации W
соотношением
связано с энергией активации W
соотношением
![]() (4.7.1)
(4.7.1)
где![]() - средний период колебания молекулы
около временного положения равновесия,
k
- постоянная Больцмана,
Т -
абсолютная температура.
- средний период колебания молекулы
около временного положения равновесия,
k
- постоянная Больцмана,
Т -
абсолютная температура.
Средний период колебания молекулы имеет порядок 10-12 с, а время релаксации для обычных маловязких жидкостей оценивается примерно в 10-11с. Время релаксации зависит от природы жидкости, ее температуры и для разных жидкостей может оказаться самым различным, но всегда меньшим среднего периода.
Специфический механизм теплового движения молекул в жидкости позволяет объяснить двойственный характер свойств жидкости по отношению к внешним силовым воздействиям.
Если время действия внешней силы больше времени релаксации, то молекулы жидкости совершают скачки преимущественно в направлении действия силы, т.е. возникает поток молекул в этом направлении, обусловливающий ее текучесть. Если время действия внешней силы меньше времени релаксации, то молекулы жидкости не успевают изменить свои положения временного равновесия и текучесть жидкости не успевает проявиться. Жидкость в этом случае подобно упругой среде оказывает сопротивление изменению не только ее объема, но и формы. При очень кратковременном действии внешней силы может даже произойти нарушение прочности жидкости, т. е. могут появиться трещины, разломы и т. д.
В соответствии с описанным выше механизмом теплового движения в жидкости зависимость вязкости жидкости от температуры определяется формулой
![]() (4.7.2)
(4.7.2)
где множитель А зависит от природы жидкости и до некоторой степени от ее температуры.
Формула
(4.7.2), впервые выведенная Я. И. Френкелем,
показывает, что вязкость жидкости при
повышении температуры уменьшается, в
то время как для газов растет пропорционально
![]() (см.
формулу 4.2.29). Объясняют это тем, что для
газов вязкость в основном определяется
скоростью хаотического теплового
движения молекул. В противоположность
этому, в жидкостях вязкость определяется
подвижностью молекул, во многом зависящей
от действия межмолекулярных сил. Вязкость
жидкостей зависит также и от давления
и быстро возрастает с его увеличением.
Это объясняют тем, что при повышении
давления возрастает энергия активации
и соответственно увеличивается время
релаксации.
(см.
формулу 4.2.29). Объясняют это тем, что для
газов вязкость в основном определяется
скоростью хаотического теплового
движения молекул. В противоположность
этому, в жидкостях вязкость определяется
подвижностью молекул, во многом зависящей
от действия межмолекулярных сил. Вязкость
жидкостей зависит также и от давления
и быстро возрастает с его увеличением.
Это объясняют тем, что при повышении
давления возрастает энергия активации
и соответственно увеличивается время
релаксации.
Величину η-1, обратную вязкости жидкости, принимают за меру текучести жидкости и называют текучестью жидкости.
При понижении температуры вязкость некоторых жидкостей возрастает настолько, что они практически перестают течь и превращаются в аморфные тела (см.п. 4.7.4).
Для многих жидкостей вязкость связана простой зависимостью с удельным объемом V жидкости:
![]() ,
(4.7.3)
,
(4.7.3)
где ω — предельный объем молекул жидкости, а следовательно,
(V-ω) — свободный объем. Экспериментально было установлено, что значение ω близко к постоянной b в уравнении Ван-дер-Ваальса. Постоянная С в этой формуле учитывает силы межмолекулярного взаимодействия жидкости и играет роль, аналогичную постоянной а в уравнении Ван-дер-Ваальса.
