
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
14.2.2. Растворение металлов под током в коррозйонноактивных средах
Скорость коррозии металлов может быть определена из поляризационных кривых в коррозионноактивнои среде. Катодная поляризационная кривая, полученная, например, на цинке в слабокислом растворе при достаточно высоких поляризациях, будет соответствовать реакции восстановления ионов гидроксония, а анодная — растворению цинка (рис. 14.4, кривые 1 и 2).
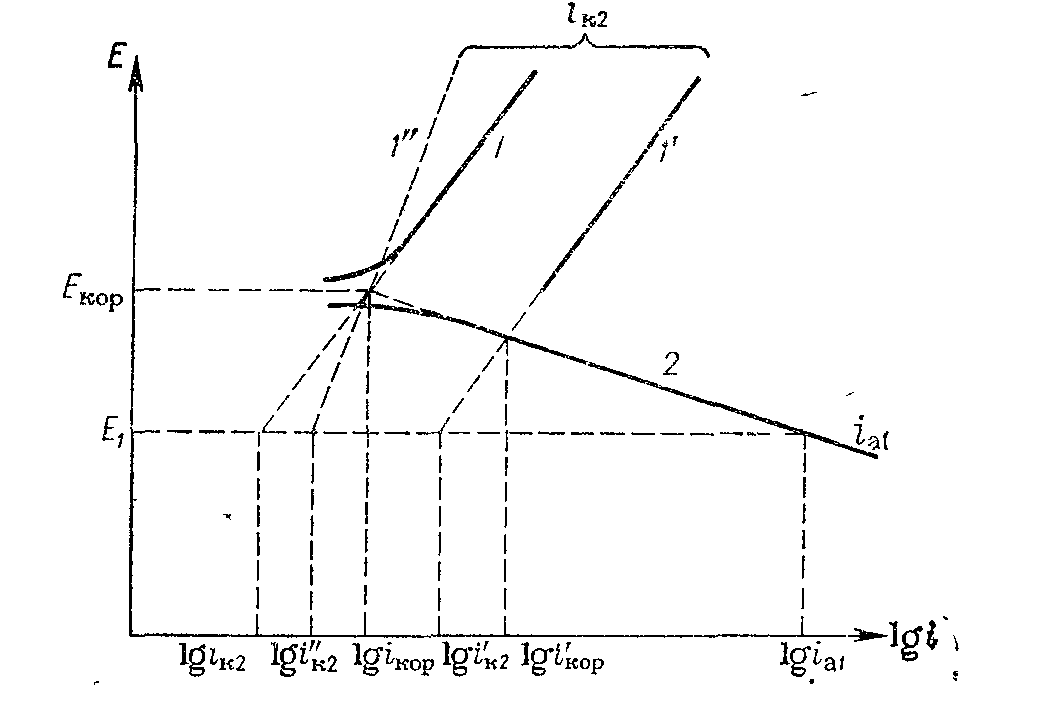
Рис. 14.4. Катодные поляризационные кривые выделения водорода (1, 1’, 1’’) и анодная кривая (2) ионизации металла на металлическом электроде в отсутствие ионов металла в растворе.
Экстраполяция тафелевских участков поляризационных кривых, каждая из которых соответствует одной из сопряженных реакций, до пересечения дает значения коррозионного потенциала Екор и тока коррозии lg iкор.
Небольшой сдвиг от коррозионного потенциала (ΔЕ) в отрицательную сторону вызывает ускорение процесса выделения водорода и замедление реакции ионизации цинка. В результате в цепи будет протекать ток:
![]()
или
![]()
Разложим экспоненты в ряд и ограничимся двумя первыми членами разложения
![]()
откуда
![]()
Из этого уравнения видно, что чем больше плотность тока коррозии, тем меньше сдвиг потенциала от значения коррозионного потенциала при заданном значении катодной плотности тока. Обозначим:
![]() ;
;
![]()
Тогда
![]()
откуда для малых ΔЕ
![]()
Метод, основанный на определении токов коррозии по последнему уравнению, называется методом поляризационного сопротивления. Для расчета тока коррозии снимают поляризационную кривую в области небольших отклонений от коррозионного потенциала и находят i/ΔE. Величины bк и ba обычно бывают известны либо определяются из поляризационных кривых при больших поляризациях.
Из рассмотрения поляризационных кривых следует, что увеличение анодной поляризации приводит к росту анодного тока растворения металла. Так, при потенциале Е1 (см. рис. 14.4) анодный ток растворения цинка (lg ia1) значительно превышает ток коррозии, а ток выделения водорода (lg ik2) уменьшается и, следовательно, истинное значение тока коррозии цинка при анодном потенциале снижается. Падение тока коррозии при анодной поляризации корродирующего металла называется положитель-ным разностным эффектом (положительным дифференц-эффек-том). Чем больше наклон катодной поляризационной кривой (кривая 1’’ на рис. 14.4), тем меньше снижение скорости выделения водорода и тока коррозионного растворения цинка.
В ряде случаев, например при растворении магния и алюминия в растворах, содержащих хлорид-ионы, наблюдается противоположное явление — увеличение скорости выделения водорода при анодной поляризации металла, т. е. отрицательный разностный эффект (отрицательный дифференц-эффект).
Причиной отрицательного разностного эффекта может быть образование ионов промежуточной валентности при растворении металла, которые затем, окисляясь, восстанавливают воду или ионы гидроксония до водорода. Второй причиной увеличения скорости выделения водорода может быть существование на поверхности металлов оксидных или других пленок (адсорбционных), которые отрываются при интенсивном растворении металла. В результате удаления пленки на чистой поверхности перенапряжение выделения водорода снижается, что вызывает сдвиг катодной поляризационной кривой в положительную сторону (рис. 14.4, кривая 1’). Как видно из рисунка, ток выделения водорода при этом возрастает (lg i’к2) по сравнению с металлом, не покрытым оксидной пленкой (lg iк2), но остается ниже тока коррозии на свежем металле (lg i’кор). В пользу существования пленок на алюминии указывает тот факт, что при растворении алюминия и магния в щелочных растворах отрицательный разностный эффект отсутствует.
Я. М. Колотыркин и Г. М. Флорианович высказали мысль о том, что отрицательный разностный эффект может быть вызван изменением кислотности прианодного слоя. Действительно, В. В. Сысоева, И. А. Черепкова и Г. Л. Барунина методом микростеклянного электрода установили, что при анодной поляризации алюминия в 3%-ном растворе NaCl происходит подкислеиие при-анодного слоя. Парциальная поляризационная кривая выделения водорода, построенная с учетом изменения рНs, принимает нормальный вид, т. е. скорость выделения водорода возрастает вместе со сдвигом потенциала в электроотрицательную сторону. Однако парциальная поляризационная кривая выделения водорода не совпадает с поляризационной кривой выделения водорода при катодной поляризации (рис. 14.5). Следовательно, хотя изменение рН прианодного слоя и играет определенную роль в отрицательном дифференц-эффекте, но не объясняет целиком причину его возникновения. По-видимому, отрицательный дифференц-эффект возникает как следствие влияния на кинетику процессов одновременно нескольких из указанных выше факторов.
При катодной поляризации электрода в коррозионноактивной среде наблюдаются явления, аналогичные рассмотренным: обычно происходит лишь уменьшение скорости ионизации металла. Этот эффект носит название протект-эффекта.

Рис. 14.5. Анодные и катодные поляризационные кривые на алюминиевом электроде:
1 — парциальная кривая растворения алюминия, практически совпадающая с общей анодной поляризационной кривой; 2 — парциальная кривая выделения водорода; 3 — то же с учетом pHs (расчет); 4 — катодная поляризационная кривая выделения водорода на предварительно аноднополяризованном алюминии.
Появление дифференц- и протект-эффектов происходит не только при сдвиге потенциала от внешнего источника тока, но и при контакте корродирующего металла с другим металлом. Так, положительный дифференц-эффект на цинке легко обнаружить, измеряя скорость выделения водорода на чистом цинке и при его контакте с платиной. При контакте цинка с платиной количество выделяющегося на цинке водорода меньше, чем на цинке при коррозионном потенциале. Если же привести в соприкосновение железный и цинковый электроды, погруженные в морскую воду, то происходит сдвиг потенциала железа в катодную сторону и снижение скорости коррозии благодаря протект-зффекту.
