
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
14.2. Электрохимическая коррозия
В коррозионной электрохимической системе идет процесс самопроизвольного разрушения металла (коррозия) при воздействии на него агрессивной среды (проводника второго рода). Процессы коррозии, подчиняющиеся закономерностям электрохимической кинетики, называются электрохимической коррозией.
Электрохимическая коррозия — сложный гетерогенный процесс, связанный с протеканием по крайней мере двух окислительно-восстановительных сопряженных реакций на поверхности корродирующего металла. В результате протекания сопряженных реакций корродирующий металл приобретает определенный стационарный потенциал, называемый в данном случае коррозионным потенциалом. Коррозионный потенциал, несмотря на необратимость процесса коррозии, может быть устойчив в течение длительного времени.
Оценка принципиальной возможности протекания электрохимической коррозии производится, как указано выше, сравнением равновесных потенциалов сопряженных электрохимических реакций. Суждение же о реальной скорости процесса коррозии можно получить лишь из кинетических зависимостей протекания сопряженных реакций. Такие зависимости представлены на рис. 14.1 для системы цинк — соляная кислота концентрации 0,1 кмоль/м3 с добавкой 10–4 кмоль/м3 хлорида цинка. Поскольку поляризация при выделении и растворении цинка невелика, катодная и анодная кривые довольно круты и ток обмена велик. Но ввиду малой концентрации ионов цинка в растворе катодная поляризационная кривая достаточно быстро выходит на предельный диффузионный ток.
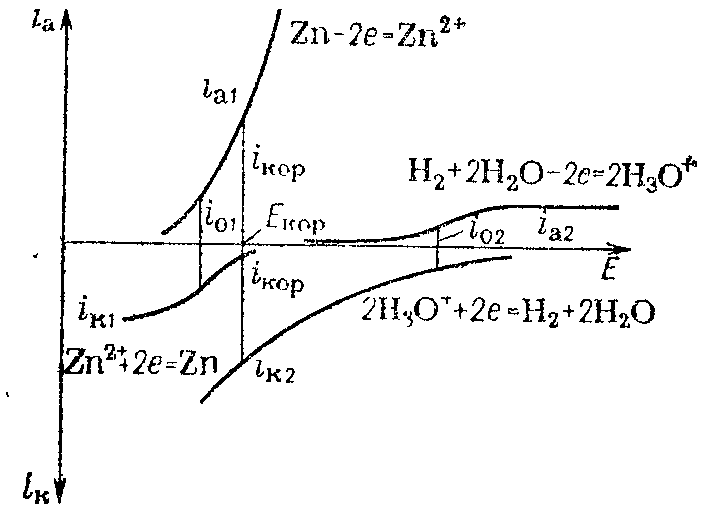
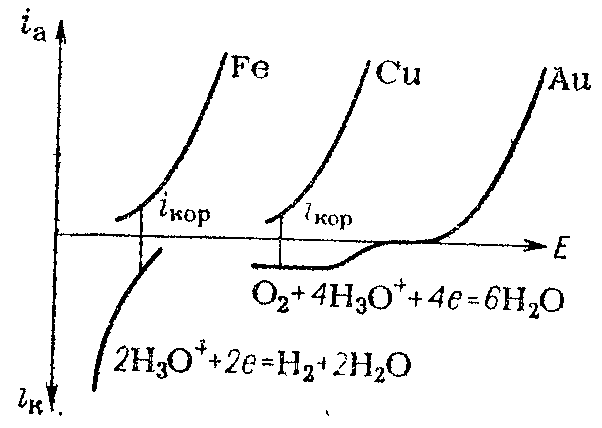
Рис. 14.1. Частные поляризационные кривые разряда — ионизации цинка и водорода на цинковом электроде.
Рис. 14.2. Расположение поляризационных кривых ионизации некоторых металлов относительно кривых восстановления ионов гидроксония и молекулярного кислорода в кислом растворе.
Перенапряжение же водорода на цинке очень велико, чем и определяются малые значения тока обмена и пологий характер поляризационной кривой. Растворение цинка и выделение водорода протекают путем передачи электронов от атома цинка ионам гидроксония, следовательно, растворение цинка будет идти со скоростью, определяемой равенством катодных и анодных токов,
т. е.
iкор = iк1 + iк2 = ia1 + ia2
Здесь индексы 1 и 2 относятся соответственно к цинку и водороду. Стационарный потенциал, отвечающий этому равенству, и будет потенциалом коррозии или коррозионным потенциалом. В рассматриваемом случае потенциал коррозии достаточно удален как от равновесного потенциала цинкового электрода, так и от равновесного потенциала водородного электрода. Вследствие этого
iк2 >> iк1; ia1 >> ia2
и можно записать
iкор = iк2 = ia1
Скорость растворения цинка является скоростью его электрохимической коррозии; она может быть охарактеризована в единицах плотности тока и называется плотностью тока коррозии. Плотность тока коррозии, а следовательно, и скорость коррозии, определяемая ординатой от Екор до пересечения с поляризационной кривой, может быть найдена не только по количеству цинка, перешедшего в раствор в единицу времени, но и по количеству выделившегося водорода, так как при коррозионном потенциале скорости этих процессов равны.
Процессом, сопряженным с растворением металла, может быть, помимо реакции восстановления ионов гидроксония, также и реакция восстановления молекул растворенного кислорода пли восстановительная реакция типа Fe3+ + e = Fe2+ и др.
Если в растворе отсутствуют вещества, способные восстанавливаться на данном металле, то процесс электрохимической коррозии не протекает, а на электроде устанавливается потенциал, связанный с адсорбцией ионов (адсорбционный потенциал). Примером такого рода потенциалов являются потенциалы, устанавливающиеся на идеально поляризуемых электродах.
На скорость коррозионного процесса и стационарный потенциал основное влияние оказывают природа металла и свойства среды. На металлах, равновесный потенциал которых положительнее равновесного потенциала водородного электрода, растворения металла не происходит и водород не выделяется. Однако если в растворе имеется растворенный кислород, который в зависимости от рН может восстанавливаться по реакции
O2 + 4Н3О+ + 4е = 6Н2O или О2 + 2Н2О + 4е = 4ОН–
то коррозия металла может протекать с сопряженной реакцией восстановления кислорода, так как равновесные потенциалы этих
реакций при одинаковом рН на 1,23 В положительнее равновесного потенциала водородного электрода (рис. 14.2).
Из расположения анодных поляризационных кривых (рис. 14.2) видно, что в слабокислых растворах, содержащих небольшие концентрации ионов соответствующих металлов, такой металл, как Fe, будет корродировать с сопряженной реакцией восстановления как ионов гидроксония, так и молекул кислорода. Но медь, равновесный потенциал которой положительнее равновесного потенциала водородного электрода в слабокислых растворах, окисляться с восстановлением ионов гидроксония не может. В присутствии растворенного кислорода сопряженной реакцией на меди будет реакция восстановления молекул кислорода. Более благородные металлы (например, Аu, а также Hg, Ag) обладают настолько высокими положительными потенциалами, что на них невозможно восстановление не только ионов гидроксония, но и растворенного кислорода, поэтому они являются устойчивыми в растворах, не содержащих других окислителей. Однако и некоторые из этих металлов (Hg, Ag) будут подвержены коррозии, если в растворе имеется окислитель с очень высоким положительным равновесным потенциалом, например азотная кислота.
Существенное влияние на коррозию оказывает рН раствора. Равновесный потенциал реакции восстановления ионов гидроксония смещается на 0,059 В в электроотрицательную сторону при повышении рН на единицу при 25 °С. Поэтому скорость коррозии металла, например цинка, будет уменьшаться при переходе от кислых к нейтральным растворам. Но в щелочных растворах цинк растворяется с образованием гидроксокомплексов по реакции
Zn + 4ОН– – 2е = Ζn(ΟΗ)42–
равновесный потенциал которой значительно отрицательнее равновесного потенциала в растворе простых ионов. Поэтому скорость коррозии цинка вновь возрастает при переходе от нейтральных к щелочным растворам.
Этот пример также показывает, какое большое влияние оказывает комплексообразование на скорость коррозии. Повышение скорости коррозии в присутствии комплексообразователя связано с ускорением процесса анодного растворения. Формально это связано со сдвигом анодной поляризационной кривой в отрицательную сторону.
Эффект комплексообразования наблюдается при коррозии золота. Золото не растворяется в азотной кислоте, так как равновесный потенциал восстановления азотной кислоты отрицательнее равновесного потенциала золота. Но золото растворяется в смеси азотной и соляной кислот (царской водке) и это связано с тем, что в этом случае золото растворяется с образованием анионов АuСl4–, а равновесный потенциал реакции
Аu + 4Сl– – 3е = АuС14–
отрицательнее равновесного потенциала восстановления азотной кислоты.
В связи с тем, что скорость реакции восстановления ионов гид- роксония определяется скоростью переноса электрона, положение поляризационной кривой этой реакции не зависит от перемешивания. Поэтому скорость коррозионных процессов с сопряженной реакцией восстановления ионов гидроксония не зависит от перемешивания раствора. Скорость же коррозии металла с сопряженной реакцией восстановления кислорода может зависеть от перемешивания, так как концентрация кислорода в растворе невелика и скорость его восстановления зачастую лимитируется стадией диффузии.
Таким образом, скорость коррозии зависит от взаимного рас-положения поляризационных кривых и механизма катодного процесса восстановления окислителя и анодного растворения металла. Значение коррозионного потенциала всегда лежит между значениями равновесных потенциалов сопряженных реакций, однако на металлах с большими плотностями тока обмена и высоким перенапряжением выделения водорода устанавливается коррозионный потенциал, весьма близкий по своему значению к равновесному потенциалу металлического электрода. Типичными примерами таких систем являются цинк в щелочном растворе цинката и амальгамы щелочных металлов в водных растворах.
При сильном же торможении скорости анодного растворения, например никеля в кислых растворах, и высоких плотностях тока обмена сопряженной реакции восстановления — ионизации водорода значение коррозионного потенциала близко к равновесному потенциалу водородного электрода при данном рН.
