
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
5.2. Диффузия в растворах электролитов
Процессы диффузии, как и электрическая проводимость, связаны с движением ионов. Однако в первом случае ионы разного знака двигаются в одном направлении под действием градиента концентрации (активности), а во втором — в противоположные под действием градиента электрического потенциала. И в том, и в другом процессах электронейтральность раствора не нарушается.
Если диффундирующие частицы не несут электрического заряда, то скорость диффузии wiд определяется градиентом химического потенциала, если же частицы заряжены — градиентом электрохимического потенциала
![]()
где w’iд — скорость перемещения компонента (или данного сорта попов) вдоль оси х при градиенте, равном единице. Знак минус в выражении означает, что диффузия протекает в направлении, противоположном увеличению градиента электрохимического потенциала.
Продифференцируем
выражение для электрохимического
потенциала
(см. 2.6) по х
и
подставим полученное выражение для
![]() в
уравнение скорости диффузии:
в
уравнение скорости диффузии:
![]()
где ∂φ / ∂x — градиент электрического потенциала.
Умножая правую и левую части уравнения на концентрацию компонента Сi, получим
![]()
где Ji — поток компонента, кмоль/(м2∙с).
Когда ∂φ / ∂x = 0
![]()
Допустив, что активность компонента равна его концентрации, получим;
![]()
Сравнивая это выражение с уравнением первого закона диффузии Фика
![]()
имеем
![]()
Абсолютная скорость движения w0i иона связана с его коэффициентом диффузии соотношением:
w0i =DiziF/RT
откуда
w’iд = w0i/ziF
Подставим выражение для w’iд в выражение для Di:
![]() .
.
Умножим числитель и знаменатель правой части уравнения на число Фарадея
![]()
где li = w0iF – подвижность иона или ионная электрическая проводимость (см. 5.1.2).
Таким образом, уравнение для потока компонента может быть записано в виде:
![]()
Общее уравнение для потока диффузии, выраженное через концентрацию компонента, имеет вид:
![]()
Подставляя
в него выражение для
![]() через коэффициент диффузии
и абсолютную скорость движения, получим:
через коэффициент диффузии
и абсолютную скорость движения, получим:
![]()
или
![]()
Если раствор содержит только один 1—1-валентный электролит, то |zk| = |za| и Ск = Са = С. Следовательно, уравнения для скорости движения ионов получим в виде:
![]()
![]()
На ранней стадии процесса диффузии скорость движения одного из ионов обычно выше, чем другого. Это вызывает появление градиента потенциала ∂φ/∂x, который будет стремиться выравнять скорости движения ионов. Градиент потенциала сначала растет, а затем, когда скорости движения уравняются, становится постоянным. Следовательно, в стационарном состоянии диффузии wk = wa и из уравнений скоростей движения ионов получаем:
![]()
Подставляя последнее уравнение в выражение для скорости переноса катиона (wк.д) или аниона (wа.д), получим:
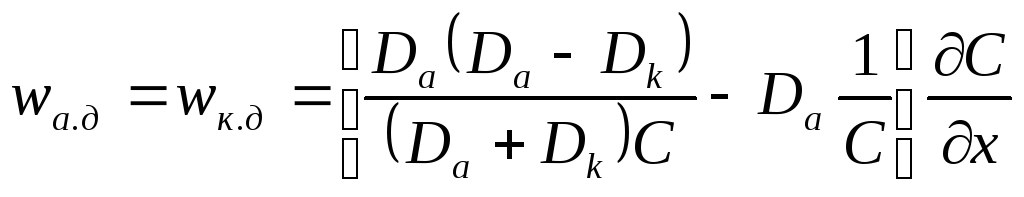
или
![]()
Выражение для потока примет вид:
![]()
При сравнении этого выражения с уравнением для потока из закона Фика видно, что диффузию электролита в отсутствие других ионов можно характеризовать эффективным коэффициентом диффузии:
![]()
Подставив в эту формулу вместо Dк и Da их выражения через w0k и w0a, получим:
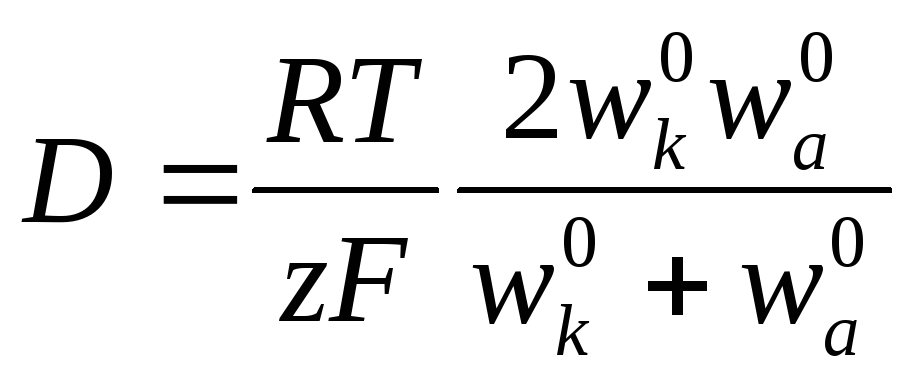
Это уравнение применимо лишь к разбавленным растворам электролитов. Необходимо отметить, что при диффузии механизм движения ионов иной, чем при протекании тока. При диффузии катионы и анионы двигаются в одном направлении, причем более быстрые частицы тормозятся более медленными, а более медленные ускоряются более быстрыми ионами. Поэтому в отличие от движения в электрическом поле при диффузии отсутствует релаксационный эффект, а катафоретический эффект имеет другое значение. При движении ионов в электрическом поле катионы и анионы двигаются в противоположных направлениях и поэтому всегда тормозят друг друга.
Используя уравнение
![]()
и выражая поток вещества Ji в токовых единицах
ii = ziFJi
для общей плотности тока, протекающего через раствор, получим:
![]()
и
![]()
Из последнего уравнения следует:
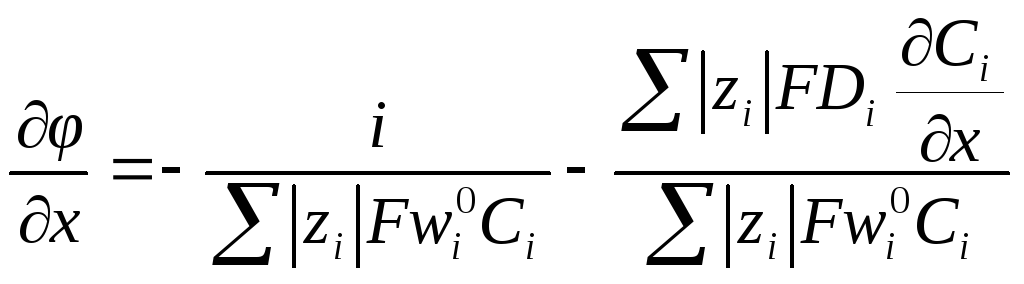
Тая
как
![]() = κ
(см.
5.1. 2), то окончательно имеем:
= κ
(см.
5.1. 2), то окончательно имеем:

или
![]()
Из уравнения видно, что падение потенциала в электролите при прохождении электрического тока связано с омическим падением потенциала Δφом = i/κ, которое зависит от тока, протекающего через раствор, и диффузионным потенциалом Δφд, определяемым различием в скоростях движения диффундирующих частиц. По-скольку диффузионный потенциал не зависит от тока, то он сохраняется и после выключения тока до тех пор, пока не прекратится процесс диффузии. Таким образом, диффузионный потенциал, возникающий при прохождении электрического тока, зависит от общей электрической проводимости электролита и при ее увеличении уменьшается. Поэтому в растворах, содержащих фоновый электролит, значение диффузионного потенциала невелико и диффузия ионов подчиняется простому уравнению Фика.
Аналогичное явление происходит и при самодиффузии, т. е. в условиях, когда частицы вещества диффундируют в растворе этого же вещества. Процессы самодиффузии можно исследовать, если в раствор какого-либо вещества ввести его изотоп. Если коэффициенты диффузии изотопа и простого иона равны, то при самодиффузии диффузионный потенциал не возникает и процесс подчиняется закону Фика.
Коэффициенты диффузии ионов в разбавленных растворах могут быть вычислены из уравнений, а также определены экспериментально, например из полярографических измерений. В табл. 5.4 приведены значения коэффициентов диффузии некоторых ионов, измеренные в различных фоновых электролитах.
Подставляя в уравнение для Di численные значения постоянных, получим:
![]()
Коэффициенты диффузии, рассчитанные из уравнения и полу- ченные из полярографических измерений, обычно удовлетворительно совпадают.
Коэффициент диффузии 1 — 1 -валентного электролита можно рассчитать по уравнению, непосредственно получающемуся из приведенной выше формулы, если в нее подставить значения постоянных:
![]()
В табл. 5.5 приведены значения коэффициентов диффузии, рассчитанные из электрических проводимостей при бесконечном разведении (Dрассч) и экспериментально измеренные при различных концентрациях электролита (Dэксп).
Как видно из таблицы, коэффициенты диффузии несколько уменьшаются с увеличением концентрация электролита и, что
Таблица 5.4. Коэффициенты диффузии (D∙109, м2/с) некоторых ионов в разл
|
С, кмоль/м3 |
Ag+ |
Tl+ |
Pb2+ |
Cd2+ |
||||
|
KNO3 |
KNO3 |
KCl |
NaCl |
KNO3 |
KCl |
KCl |
KNO3 |
|
|
0,01 0,1 1,0 3,0 |
1,585 1,532 1,546 – |
– 1,82 1,65 – |
– 1,74 1,57 1,35 |
– 1,77 1,50 0,92 |
8,76 8,28 8,02 – |
8,99 8,67 8,20 8,14 |
8,15 7,15 7,90 7,90 |
– 6,90 6,81 – |
вполне естественно, ниже рассчитанных при бесконечном разведении. В растворах, содержащих общий анион, например для хлоридов и нитратов щелочных металлов, коэффициент диффузии возрастает при переходе Li →Cs, что связано с уменьшением сольватации катионов и увеличением их подвижности.
Зависимость коэффициентов диффузии от вязкости η раствора подобна зависимости электрической проводимости от вязкости,
Таблица 5.5. Коэффициенты диффузии (D∙109, м2/с) 1 — 1-валентных электролитов в водных растворах при 25 °С (Робинсон и Стокс)
|
Соль |
Dрассч при С = 0 |
Dэксп при различных концентрациях электролита (кмоль/м3) |
||||
|
0,001 |
0,003 |
0,005 |
0,007 |
0,01 |
||
|
LiCl NaCl KCl RbCl CsCl LiNO3 NaNO3 KNO3 AgNO3 KClO4 |
1,366 1,610 1,993 2,051 2,044 1,336 1,568 1,928 1,765 1,871 |
1,345 1,585 1,964 – 2,013 – – 1,899 – 1,845 |
1,331 1,570 1,945 2,007 1,992 1,296 – 1,879 1,719 1,835 |
1,323 1,560 1,934 1,995 1,978 1,289 1,516 1,866 1,708 1,829 |
1,318 1,555 1,925 1,984 1,969 1,283 1,513 1,857 1,698 1,821 |
1,312 1,545 1,917 1,973 1,958 1,276 1,503 1,846 – 1,790 |
если не происходит изменения эффективного радиуса ионов или их ассоциации. В таких растворах должно выполняться правило:
Di η = const
Однако измерения подвижности ионов в электролите, искусственно загущенном глицерином или сахарозой, показали, что экспериментально выполняется соотношение
li ηp = const
где р — коэффициент, меньший единицы.
Следовательно, предыдущее уравнение следует записать в виде:
Di ηp = const
ичных фоновых электролитах
|
IO3– |
Zn2+ |
Fe(CN)64– |
Fe(CN)63– |
|||
|
KCl |
KNO3 |
KCl |
KNO3 |
NaOH |
KCl |
KCl |
|
– 10,15 9,89 9,36 |
– 10,01 8,92 7,24 |
6,60 6,38 6,20 – |
6,76 6,73 7,23 7,69 |
– 6,54 5,13 4,18 |
– 6,50 6,32 6,20 |
7,84 7,62 7,63 7,36 |
Для больших катионов, например иона тетраамиламмония, р ≈1.
Таким образом, зависимость коэффициента диффузии от концентрации электролита может быть обусловлена изменением вязкости раствора и межионных взаимодействий. В разбавленных растворах изменение вязкости незначительно, поэтому основным эффектом в снижении коэффициента диффузии является увеличение межионных взаимодействий. Зависимость коэффициента диффузии от концентрации раствора можно получить, используя уравнение первого закона Фика для реальных растворов. Этот вопрос уже рассмотрен в разд. 2.6.
Эффективный коэффициент диффузии
![]()
![]()
изменяется с концентрацией гораздо меньше, чем Di, что указывает на существенное влияние сил межионного взаимодействия. Однако при высоких концентрациях электролита (более 0,1 кмоль/м3) обычно приходится использовать либо экспериментально определенные коэффициенты диффузии, либо рассчитанные по эмпирическим уравнениям. Значение коэффициента диффузии изменяется с температурой по формуле Аррениуса.
