
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
Плотность тока, протекающего через электрод (регистрируемая прибором), всегда равна разности частных плотностей токов: i = i2 – i1. При равновесном потенциале измеряемый ток равен нулю и i1 = i2 Значение частных плотностей токов при равновесном потенциале называется плотностью тока обмена i0. Следовательно, если потенциал электрода равен равновесному (Е = Еp), можно записать: il = i2 = i0 или, воспользовавшись последними уравнениями разд. 8.2:
![]()
При сдвиге потенциала от равновесного значения через электрод начинает протекать ток, равный разности
![]()
Умножим и разделим правую часть уравнения на i0, причем в каждом из членов разности в знаменателе i0 заменим на соответствующие члены предыдущего уравнения:

и
![]() и
и
![]()
Из этого уравнения, называемого полным уравнением поляризационной кривой, следует, что при сдвиге потенциала от равновесного значения в катодную сторону (Е < Ер) i = iK < 0, а при сдвиге в анодную сторону (Е > Ер) i = ia > 0. Таким образом, при указанной системе записи плотности тока i = i2 – i1 мы уславливаемся считать катодный ток отрицательным, а анодный положительным. Равноценна и противоположная система записи (i = i1 – i2), но мы ею не будем пользоваться.
Соотношения между полной поляризационной кривой и частными поляризационными кривыми показаны на рис. 8.7.
При достаточно высоких катодных или анодных перенапряжениях измеряемый ток очень близок к iк или iа. Это связано с тем, что при увеличении перенапряжения один из экспоненциальных членов в последнем уравнении стремится к нулю. При потенциалах электрода, близких к равновесному, нельзя пренебречь ни одной из составляющих. В этом случае η << RT/zF и экспоненты в правой части уравнения можно разложить в ряд. Ограничиваясь двумя первыми членами ряда (еx = 1 + х и е–x = 1 – х), получим:
![]()
Так как αа + αк = 1, то
![]()
Это уравнение называется полным уравнением поляризационной кривой при малых перенапряжениях. В координатах плотность тока — перенапряжение онопредставляет прямую линию с наклоном i0(zF/RT), проходящую через начало координат, причем значение плотности тока не зависит от коэффициентов переноса. Область перенапряжений, в которой экспериментально реализуется линейная зависимость, невелика и, например, при отклонениях от линейности в

Рис. 8.7. Зависимость плотности тока от перенапряжения при αк = αа = 0,5.
1% составляет 0,013/z В, если α = 0,5. При уменьшении α область линейности резко сокращается и, когда α = 0,4, равна 0,0026/z В. Из наклона прямой di/dη = i0(zF/RT) при малых поляризациях определяется ток обмена, а обратная величина dη/di, при η → 0 равная
![]()
получила название сопротивления переноса заряда постоянному току.
При высоких перенапряжениях, когда η >> (RT/zF) , один из членов разности в уравнении полной поляризационной кривой уменьшается, а другой — возрастает настолько, что уменьшившимся членом можно пренебречь. При катодном процессе, по условию, перенапряжение имеет отрицательный знак, при анодном — положительный. В соответствии с этим
![]() ;
;
![]()
Логарифмируя, получаем:
![]() ;
;
![]()
или
![]()
![]()
Поскольку ik отрицательно, в этих уравнениях под знаком логарифма стоит абсолютное ее значение.
В дальнейшем изложении мы не будем пользоваться обозначением |ik|, но будем помнить, что ik есть абсолютное значение катодной плотности тока. Кроме того, под знаком логарифма должна стоять плотность тока в безразмерных единицах, например в долях плотности тока обмена. Этим требованием обычно пренебрегают и выражают ik в А/м2.
Оба уравнения могут быть представлены в форме
η = a + b lg |i|
носящей название уравнения Тафеля.
Построение катодной и анодной поляризационных кривых в полулогарифмических координатах позволяет определить значение плотности тока обмена, а также коэффициенты переноса (рис. 8.8). Экстраполяция линейных участков, подчиняющихся уравнению Тафеля, на нулевое перенапряжение дает значение логарифма плотности тока обмена.
По углам наклона линейных участков в координатах η — lg i определяют коэффициенты переноса:
![]() ;
;
![]()

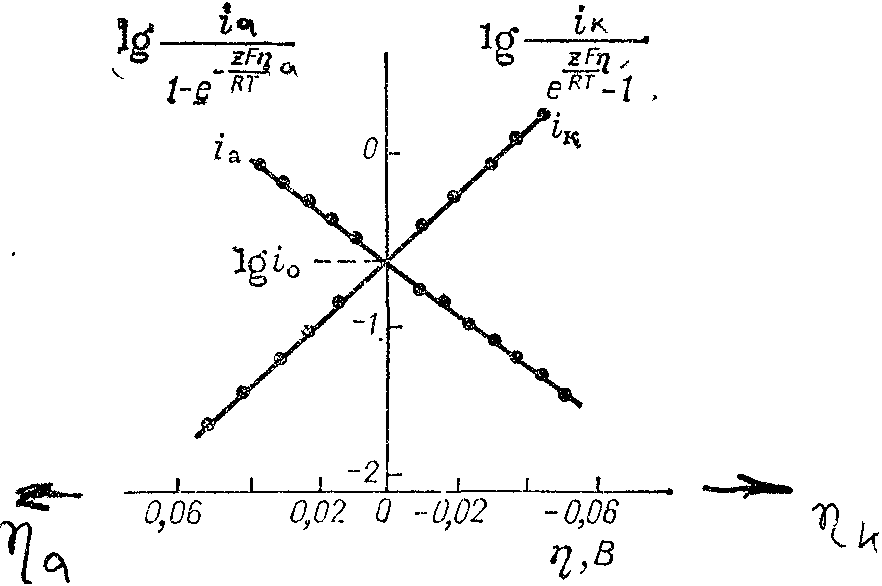
Рис. 8.8. Зависимость перенапряжения от плотности тока на амальгамном кадмиевом электроде в растворе CdSO4 (концентрации 0,005 кмоль/м3) + K2SO4 (концентрации 0,4 кмоль/м3).
Рис. 8.9. Поляризационные кривые на амальгамном цинковом электроде в растворе перхлората цинка в диметилформамиде, построенные в координатах О. А. Есина.
Как показал О. А. Есин, уравнение полной поляризационной кривой может быть проанализировано и в общей форме. Вынося в этом уравнении один из членов разности за скобки и помня, что αk + αa = 1, получим:
![]() или
или
![]()
Преобразовываем далее:
 ;
;

или


Два
последних уравнения выражают соответственно
истинные скорости
анодного и катодного процессов и
справедливы во всей области
перенапряжений. Каждое из уравнений
представляет прямую
линию в координатах η
—
 ( η —
( η —
 )
(рис.
8.9). Обе прямые проходят в области катодных
и анодных перенапряжений
и соответствуют истинной скорости
анодного и катодного
процессов как в катодной, так и в анодной
областях перенапряжений.
Прямые пересекаются при η
= 0
и их точка пересечения
на оси ординат дает значение логарифма
плотности тока
обмена. Коэффициенты переноса определяются
из уравнений:
)
(рис.
8.9). Обе прямые проходят в области катодных
и анодных перенапряжений
и соответствуют истинной скорости
анодного и катодного
процессов как в катодной, так и в анодной
областях перенапряжений.
Прямые пересекаются при η
= 0
и их точка пересечения
на оси ординат дает значение логарифма
плотности тока
обмена. Коэффициенты переноса определяются
из уравнений:
 ;
;

Используя выражения для частных поляризационных кривых, можно получить уравнение для равновесного потенциала. Так как i1 = i2 при Е = Еp, получим:
![]()
и
![]()
Учитывая, что αa + αk = 1, имеем:
![]()
Сравнивая последнее выражение с уравнением Нернста, получим:
![]()
Таким образом, стандартный потенциал электродной реакции зависит от соотношения констант скоростей катодного и анодного процессов.
Уравнения для частных поляризационных кривых при постоянных значениях аOx и aRed в координатах Е — lg i являются прямыми линиями. По координатам точки пересечения прямых могут быть определены логарифмы плотности тока обмена и равновесный потенциал. Такой способ определения i0 и Еp часто применяется, так как не на всех электродах можно непосредственно измерить равновесный потенциал. Это связано с тем, что многие из электродов (Fe, Ni в растворах собственных ионов), а также некоторые окислительно-восстановительные электроды, имеют низкие токи обмена. В равновесных условиях на основную реакцию обмена накладываются побочные процессы, которые возникают в результате присутствия примесей на металле (окислы) или в растворе. Возможно также протекание неравновесных коррозионных процессов. Результатом является смещение измеряемого потенциала от равновесного потенциала основной реакции. Кроме того, при низких токах обмена равновесие устанавливается медленно.
Экстраполируя поляризационные кривые из области высоких катодных и анодных потенциалов, в отдельных случаях удается избежать влияния побочных процессов. С одной стороны, это связано с тем, что вклад в общий ток тока восстановления примеси незначителен ввиду малости ее концентрации, а с другой стороны — при этих потенциалах побочные реакции могут не протекать.
Как показывают экспериментальные данные, равновесные потенциалы, определенные из кинетических измерений, хорошо совпадают, когда это возможно, с полученными из измерения равновесий, и их совпадение является критерием обратимости электродной реакции (или истинного равновесия на электроде).
