
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
8.1. Поляризационные кривые
Основным отличием скорости электрохимической реакции от скорости любой гетерогенной химической реакции является ее зависимость от потенциала. Поэтому очень часто эту фундаментальную зависимость сначала выражают графически в координатах: скорость реакции в единицах плотности тока (i, А/м2) – потенциал или перенапряжение. Такая зависимость называется поляризационной кривой (катодной или анодной). Далее выводят кинетическое уравнение, описывающее данную поляризационную кривую или хотя бы часть ее и основанное на определенных представлениях о механизме протекающей реакции.
Поляризационные кривые часто имеют довольно сложный вид (рис. 8.1). При малых плотностях тока катодная и анодная поляризационные кривые имеют вид экспоненты (участок 1)*. Затем следует участок возрастающей кривой (участок 2), к которому экспоненциальное уравнение неприменимо. Участок 3 соответствует затуханию роста i с η; он переходит в площадку, отвечающую независимости плотности тока от потенциала.
На экспоненциальном участке поляризационной кривой скорость реакции обычно лимитируется стадией переноса электрона, На участке 2 скорости стадий переноса электрона и концентрационных изменений соизмеримы, в связи с чем рост плотности тока с потенциалом происходит медленнее, чем на участке 1. Участок 3 отвечает смене лимитирующей стадии. Скорость реакции здесь практически целиком ограничивается концентрационными изменениями и при концентрациях реагирующих частиц у поверхности электрода, близких к нулю, переходит в область так называемых предельных токов, не зависящих от потенциала.
В соответствии с характером поляризационных кривых эти участки имеют названия: 1) область электрохимической кинетики; 2) область смешанной кинетики; 3) область концентрационной кинетики.
Если изменение концентрации реагирующих частиц у поверхности обусловлено замедленной стадией диффузии, то область 3 называется областью диффузионной кинетики.
Кроме показанного на рис. 8.1 способа изображения поляризационных кривых, есть еще способ, представленный на рис. 8.2 и применяющийся обычно в полярографии. Согласно этому способу, вниз от линии нулевого тока откладывают анодные токи, вверх – катодные. Точка пересечения поляризационной кривой с линией
* При очень малых плотностях тока, вблизи равновесного потенциала, экспоненциальная зависимость нарушается. О причине этого см. 8.2.1.
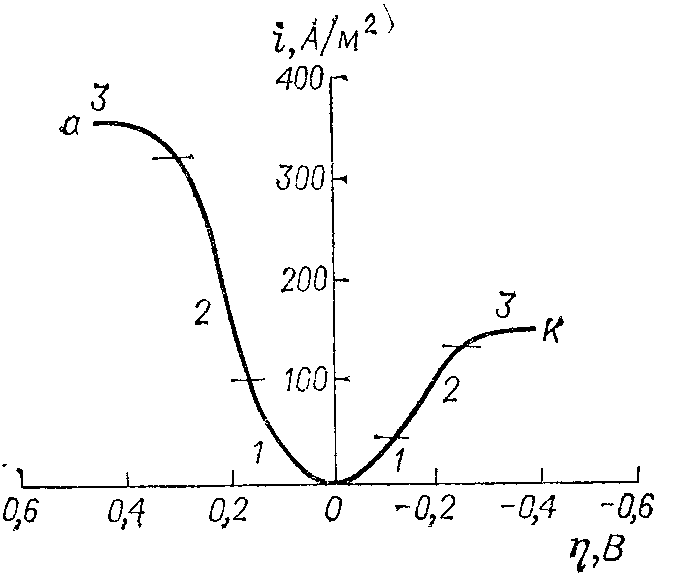

Рис. 8.1. Катодная (к) и анодная (а) поляризационные кривые на натриевом электроде в растворе NaClO4 в тетрагидрофуране концентрации 0,5 кмоль/м3.
Рис. 8.2. Поляризационные кривые реакции Ti3+ ↔ Ti4+ на ртутном капельном электроде:
1 — в растворе щавелевой кислоты (обратимый процесс); 2 — в соляной кислоте (необратимый процесс).
нулевого тока дает значение равновесного потенциала. Кривая 2 рис. 8.2 аналогична кривым рис. 8.1 и соответствует необратимому процессу, кривая 1 – обратимому.
В случае замедленного протекания электрохимической стадии происходит разделение волны на анодную и катодную и такие кривые соответствуют необратимому процессу. Если же скорость процесса лимитируется стадией диффузии и поляризационная кривая представляет собой единую анодно-катодную волну, то такой процесс называется обратимым. В этом случае перенапряжение определяется сдвигом равновесного (обратимого) потенциала из-за изменения концентрации потенциалопределяющих ионов у поверхности электрода. При изменении условий эксперимента может измениться природа замедленной стадии, а следовательно, и обратимость процесса. Кроме того, обратимость или необратимость процесса в определенной мере связана с точностью эксперимента. Так, при увеличении точности эксперимента процесс, казавшийся обратимым, может проявить характерные черты необратимости.
Методы экспериментального получения стационарных поляризационных кривых разнообразны. В гальвано- и потенциостатическом методах поддерживаются постоянными либо плотность тока, либо потенциал, а другой параметр (соответственно, потенциал или ток) регистрируется, когда достигает стационарного значения. Полученные таким методом кривые, называются стационарными поляризационными кривыми.
В динамических методах ток или потенциал изменяются с течением времени по определенному закону (обычно линейно) и регистрируется потенциал или ток, соответственно, как функция первого параметра. Такие поляризационные кривые называются динамическими, При снятий динамических кривых скорость

Рис. 8.3. Схема, поясняющая построение поляризационной кривой при задании постоянного потенциала (а) и постоянного тока (б).
изменения (развертки) тока или потенциала может изменяться в очень широких пределах – от сотых долей милливольта в секунду до сотен вольт в секунду. Если скорости развертки достаточно малы, то динамические поляризационные кривые, как правило, совпадают со стационарными и могут быть интерпретированы как стационарные поляризационные кривые. При высоких скоростях развертки динамические кривые существенно отличаются от стационарных, что связано как с протеканием процесса в нестационарных условиях, так и с наложением дополнительных факторов, например нефарадеевских токов (токов заряжения).
Поляризационные кривые сложных процессов существенно зависят от метода снятия кривой (с заданием тока или потенциала). Например, для кривой, изображенной на рис. 8.3, а любому заданному значению потенциала Е1 – Е4 соответствует вполне определенное значение тока i1 – i4. Если поддерживать постоянным ток, то, как видно из рис. 8.3, б, току i1 соответствует только потенциал Е1, току i2 – потенциал Е2 или область потенциалов E3 – E4, току i3 – потенциал Е5 и Е6, току i4 – потенциал Е7. Экспериментально это выражается в том, что при определенном значении тока i потенциал в области E2 – Е4 «ползает», а кривая, полученная с заданием тока, имеет вид, изображенный на рис. 8.4.

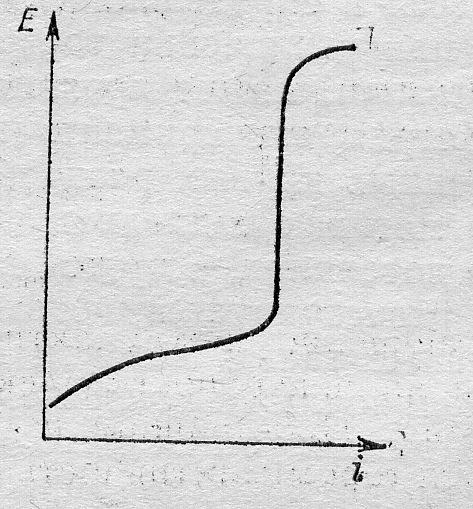
Рис. 8.4. Поляризационная кривая (рис. 8.3, б), полученная при задании постоянного тока.
Рис. 8.5. Правильное изображение поляризационной кривой, полученной в гальваностатическом режиме.
Строго говоря, при графическом изображении потенцио- и гальваностатических кривых координатные оси должны быть различны. Поскольку по оси х откладывается аргумент, а по оси y – функция, то кривые, изображенные на рис. 8.3, а и б, соответствуют потенциостатическому режиму, а гальваностатическому режиму отвечает кривая на рис. 8.5.
В литературе по электрохимии такое различие в построении поляризационных кривых не является общепринятым, поэтому следует указывать, каким способом получена та или иная кривая.%)%
