
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
5.1.2.4. Электрическая проводимость растворов
Электрическая проводимость растворов определяется скоростью движения ионов, а также их числом в единице объема и, следовательно, зависит от концентрации, природы растворенного вещества и растворителя, температуры и давления.
Удельная электрическая проводимость сильных электролитов с ростом концентрации линейно возрастает, проходит через максимум, и затем уменьшается (рис. 5.6). Наибольшим значением κ в водных растворах обладают минеральные кислоты, затем гидроксиды и соли. Аналогичный характер имеет зависимость κ — С и в случае неводных растворителей, но абсолютные значения κ меньше (рис. 5.7).
Концентрация электролита, отвечающая максимуму электрической проводимости, специфична для данного электролита и растворителя. С повышением температуры удельная электрическая проводимость возрастает (рис.. 5.8). Однако при достаточно высо ких температурах удельная электрическая проводимость с ростом температуры, как это установлено еще Аррениусом, уменьшается.
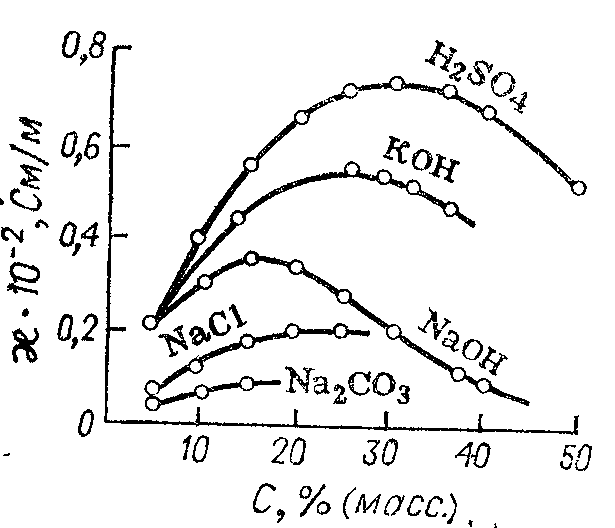

Рис. 5.6. Зависимость удельной электрической проводимости водных растворов некоторых соединений от концентрации С.
Рис. 5.7. Зависимость удельной электрической проводимости κ неводных растворов некоторых солей от концентрации С.
LiС1 растворен в диметилацетамиде, LiBr и А1С1з —в пропиленкарбонате;

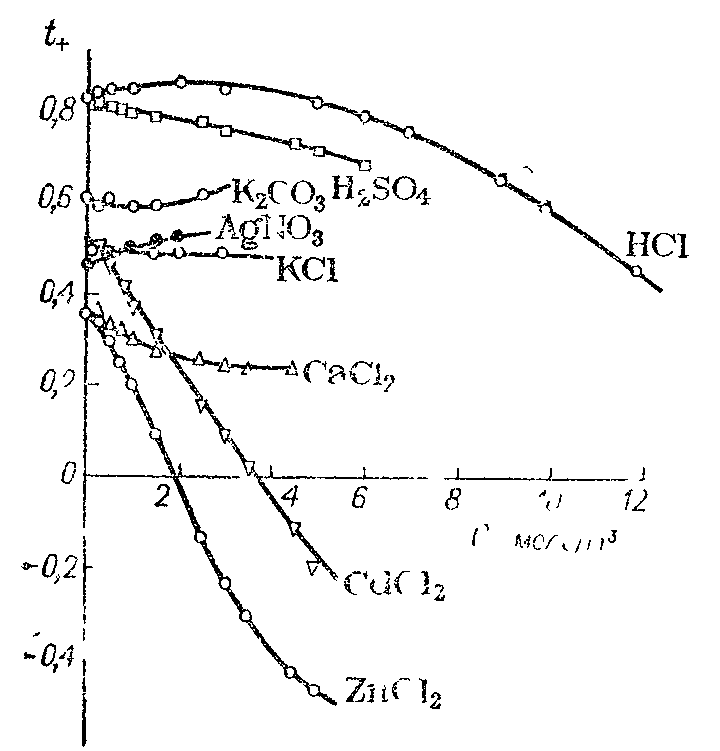
Pиc. 5.8. Зависимость удельной электрической проводимости гидроксида натрия от концентрации при разных температурах.
Рис. 5.9. Зависимость чисел переноса катионов некоторых электролитов от концентрации.
Эквивалентная электрическая проводимость максимальна в бесконечно разбавленных растворах, с ростом концентрации — уменьшается, а с повышением температуры — возрастает.
Кольрауш показал, что в ряде случаев в разбавленных растворах эквивалентная электрическая проводимость линейно уменьшается в соответствии с уравнением:
![]()
По Гхошу иногда получается лучшее совпадение с экспериментом, если изменение эквивалентной электрической проводимости представить уравнением
![]()
Эквивалентную электрическую проводимость при бесконечном разведении (нулевой концентрации) можно найти экстраполяцией
на
С
=
0 прямолинейных участков λ–![]() кривых, отвечающих уравнениям
Кольрауша или Гхоша.
кривых, отвечающих уравнениям
Кольрауша или Гхоша.
Большие значения проводимости сильных кислот и оснований определяются высокой скоростью движения иона гидроксония и гидроксид-иона. Ниже приведены подвижности некоторых ионов в водных растворах при бесконечном разведении и 25 °С:
Ион l∞∙104, Ион l∞∙104, Ион l∞∙104,
См∙м2/экв См∙м2/экв См∙м2/экв
Ag+ 61,9 Na+ 50,1 ⅓ Fe(CN)63– 99,1
⅓ Al3+ 63,0 ½ Ni2+ 54,0 ¼ Fe(CN)64– 111,0
½ Ca2+ 59,5 ½ Pb2+ 70,0 I– 76,8
½ Cd2+ 54,0 ½ Zn2+ 54,0 MnO4– 61,3
½ Co2+ 49,0 (CH3)4N+ 44,9 NO3– 71,4
⅓ Cr3+ 67,0 (C2H5)4N+ 32,6 OH– 197,6
½ Cu2+ 55,0 (C3H7)4N+ 23,4 ½ SO42– 80,0
½ Fe2+ 53,5 (C4H9)4N+ 19,4 ½ WO42– 69,4
⅓ Fe3+ 68,0 (C5H11)4N+ 17,4 HCOO– 54,6
Н3О+ 349,8 Br– 78,1 CH3COO– 40,9
½ Hg2+ 63,6 Cl– 76,3 CH2ClCOO– 39,8
K+ 73,5 ½ CrO42– 83,0 C6H5COO– 32,3
Li+ 386 F– 55,4
NH4+ 73,5
Поскольку числа переноса ионов определяются скоростями движения всех сортов ионов в электролите, то, естественно, что в кислотах и щелочах числа переноса ионов гидроксония и гидр-оксида при бесконечном разведении будут существенно больше половины, в то время как для растворов солей отклонение чисел переноса от величины 0,5 не очень значительно. С увеличением концентрации числа переноса катиона и аниона в водных растворах некоторых электролитов остаются постоянными, а в других — более или менее резко изменяются (рис. 5.9). Отрицательные значения чисел переноса ионов Cd2+ и Zn2+ в растворах CdCl2 и ZnCl2 не имеют физического смысла и показывают лишь, что примененный метод измерения регистрирует суммарный эффект, связанный с переносом катиона в составе отрицательно заряженного комплексного аниона.
