
- •Раздел 1. Классификация и номенклатура биоорганических соединений.
- •Раздел 2. Сопряженные системы.
- •Раздел 3 Передача электронных влияний в биоорганических соединениях. Кислотно-основные свойства биоорганических соединений.
- •Раздел 4. Изомерия биоорганических соединений
- •Раздел 5. Механизмы биоорганических реакций.
- •Раздел 6 . Классификация, номенклатура, физические и химические свойства карбоновых кислот.
- •Раздел 7. Природные биологические активные вещества липиды и высшие карбоновые кислоты
- •Раздел 8. Природные биологические активные вещества аминокислоты
- •Раздел 9. Полипептиды. Белки
- •Раздел10. Углеводы. Классификация. Моносахариды.
- •Раздел 11. Углеводы. Олигосахариды. Полисахариды.
- •(Основная связь α-1, 4, ветвление α-1, 6 через 20-25 остатков глюкозы)
- •(Основная связь α-1, 4, ветвление α-1, 6 через 8-12 остатков глюкозы)
- •Раздел 12. Нуклеиновые кислоты, нуклеотиды, нуклеозиды, азотистые основания
- •Раздел 13. Синтетические биологически активные вещества - лекарственные препараты
- •Раздел 14. Алкалоиды. Витамины.
- •Раздел 15.Реакции полимеризации и поликонденсации. Полимеры в стоматологии.
Раздел 8. Природные биологические активные вещества аминокислоты
Исходный уровень знаний для усвоения темы основан на школьной
программе органической химии, программе по химии «Протолитическая теория кислот и оснований. Буферные системы», разделах 1- 6 данного пособия.
Для усвоения темы и приобретения компетенции по данному разделу надо знать и уметь написать
формулы:
20 аминокислот, биогенных аминов (ГАМК, ß- аланин, 2-аминоэтанол -1, 2- аминоэтантиол-1, гистамин) и амидов- глутамина и аспарагина
- записывать строение биполярного (цвиттер) - иона, определять область изоэлектрической точки, значение рН водного раствора аминокислоты, составлять схему ионизации аминокислоты в водном растворе,
составлять уравнения реакций
-образования солей при взаимодействии аминокислот с кислотами и основаниями,
-сложных эфиров,
-декарбоксилирования, переаминирования (трансаминирования) амино – и кетокислот.
- окислительного дезаминирования глутаминовой кислот.
Перечень реакций декарбоксилирования:
а. глутаминовая кислота —> 4-аминобутановая (γ – аминомасляная, ГАМК)
б. гистидин —> гистамин
в. триптофан —> триптамин
г. серин —> 2- аминоэтанол -1 (коламин)
д. цистеин —> 2-аминоэтантиол-1 (меркамин)
е. аспарагиновая кислота —> 3-аминопропановая (β-аланин)
перечень реакций трансаминирования
а. ала + щук —> ПВК + асп
б. ала + а-кетоглутаровая —> ПВК + глу
в. асп + ПВК —> щук + ала
г. асп + а-кетоглутаровая —> щук + глу
Ключевые слова
Аминокислота, амфотерность, буферный раствор, витамин В6, дезаминирование, декарбоксилирование, диастереомер, изоэлектрическая точка, концевые аминокислоты, окислительное дезаминирование, основание Шиффа (азометин), пептид (полипептид), пептидная группа, переаминирование ( трансаминирование), поликонденсация, стереоизомер, стереоряд, энантиомер.
Содержание раздела (Дидактические единицы)
8.1. Особенности строения 20 природных аминокислот, входящих в состав белков: L - конфигурация , а (альфа) - строение. Структурные формулы природных аминокислот.
8.2. Классификация аминокислот:
- по кислотно-основным свойствам: нейтральные, кислые, основные,
- по строению радикала и функциональным группам в радикале:
алифатические, ароматические, гидроксисодержащие, серусодержащие,
диаминомонокарбоновые, моноаминодикарбоновые,
- по биологическому признаку: незаменимые и заменимые.
8.3 Номенклатура - тривиальные названия, условные трехбуквенные обозначения.
8.4. Особенности пространственного строения.
8.5. Физические свойства природных аминокислот.
8.6. Ионизация аминокислот в водном растворе.
-изменение заряда в водных растворах – следствие дополнительной
ионизации карбоксильной и ли аминогруппы,
- изоэлектрическая точка аминокислот (рI),
- заряды аминокислот при различных значениях рН.
8.7. Химические свойства аминокислот in vitro:
- образование солей с кислотами, основаниями,
- свойства карбоксильной группы: образование сложных эфиров, амидов,
- декарбоксилирование при нагревании с Ва(ОН)2.
8.8.Химические свойства природных аминокислот in vivo:
-декарбоксилирование - ферментативная реакция образования
биогенных аминов с участием витамина В6
аминокислота ———> биогенный амин + СО2
- внутримолекулярное дезаминирование
аспарагиновая кислота —> фумаровая кислота + NH3
- трансаминирование ( переаминирование)
аминокислота(1) + кетокислота(2) —>кетокислота(1) + аминокислота (2)
- окислительное дезаминирование глутаминовой кислоты.
8.9. Аминокислоты и их производные - лекарственные препараты.
Приложение. Основы теории.
Общий список аминокислот, обозначения
Классификация по признаку химического строения и состава
Алифатические аминокислоты моноаминомонокарбоновые
Аланин (Ala), Валин (Val), Глицин (Gly), Изолейцин (Ile), Лейцин (Leu)
Ароматические аминокислоты моноаминокарбоновые
Тирозин (Tyr), Фенилаланин (Phe)
Гетероциклические ароматические аминокислоты моноаминомонокарбоновые
Гистидин (His), Триптофан (Trp )
Циклическая аминокислота
Пролин (Pro)
Моноаминодикарбоновые аминокислоты – кислые и их амиды
Аспарагиновая (Asp), Глутаминовая (Glu),
Аспарагин (Asn ), Глутамин( Gln )
Диаминомонокарбоновые кислоты- основные
Аргинин (Arg), Лизин (Lys), Оргинитин (не входит в состав белков)
Гидроксисодержащие алифатические аминокислоты
Серин (Ser), Треонин (Thr)
Серусодержащие алифатические аминокислоты
Метионин (Met), Цистеин (Cys )
Классификация по физико-химическим свойствам
Гидрофобные аминокислоты:
Аланин, валин, лейцин, изолейцин, метионин, пролин, триптофан, фенилаланин.
Гидрофильные аминокислоты:
Аргинин, аспарагиновая кислота, аспарагин, гистидин, глутаминовая кислота, глутамин, лизин, серин, тирозин, треонин, фенилаланин.
Особенности строения 20 природных аминокислот, входящих в состав белков: принадлежат L –стереоряду, L - конфигурация, аминогруппа находится во 2-положении, которое часто называют а-положение.
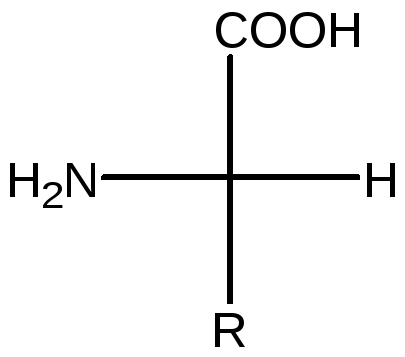
Классификацию аминокислот проводят несколькими способами, на основании различных признаков.
В основу положены кислотно-основные свойства:
-нейтральные моноаминомонокарбоновые не содержат в составе радикала амино – и карбоксильных групп, склонных к ионизации (все, кроме кислых и основных),
- кислые моноаминодикарбоновые содержат в радикале карбоксильную группу (аспарагиновая, глутаминовая),
- основные диаминомонокарбоновые содержат в радикале аминогруппу (аргинин, лизин, орнитин).
В основу положено строение радикала и наличие иных функциональных групп в радикале:
- алифатические (глицин, валин, лейцин, изолейцин),
-ароматические (карбоароматические- фенилаланин, тирозин, гетероароматические (триптофан, гистидин),
- циклическая (пролин),
-гидроксисодержащие (серин, треонин),
-серусодержащие (цистеин, метионин),
-диаминомонокарбоновые (лизин, аргинин),
-моноаминодикарбоновые (аспарагиновая, глутаминовая).
В основу положен биологический признак:
«незаменимые» аминокислоты не синтезируются в организме (8 аминокислот у взрослых – валин, лейцин, изолейцин, треонин, метионин, фенилаланин, лизин, триптофан, 10 аминокислот у детей – все перечисленные для взрослых, и дополнительно аргинин, гистидин). Остальные синтезируются в организме, их называют «заменимые». Среди них 2 аминокислоты следует считать условно заменимыми, т.к. они синтезируются из незаменимых (тирозин из фенилаланина, цистеин – с участием метионина).
Физические и кислотно-основные свойства аминокислот
Природные аминокислоты - твердые кристаллические вещества, растворимые в воде, в кристаллическом состоянии- биполярные ионы (цвиттер-ионы)
В водном растворе происходит ионизация аминокислот, содержащих в радикале амино и карбоксильные группы. Изменение заряда в водных растворах – следствие дополнительной ионизации карбоксильной или аминогруппы.
Моноаминодикарбоновые кислоты аспарагиновая и глутаминовая кислоты приобретают заряд -1, среда раствора кислая, рН <7.
Диаминомонокарбоновые кислоты аргинин и лизин приобретают заряд +1, среда раствора щелочная, рН >7.
Если заряд аминокислоты равен нулю (в растворе ионизированы одна амино- и одна карбоксильная группа), то аминокислота находится в своей изоэлектрической точке. То значение рН раствора, в котором суммарный заряд аминокислоты равен нулю, называется изоэлектрической точкой (р I ).
Изоэлектрические точки аминокислот (рI):
- нейтральные рI ~ 7 , кислые рI< 7 , основные рI > 7.
Заряды аминокислот при различных значениях рН изменяются:
а. значение рН < рI, нейтральная аминокислота имеет заряд +1, кислая +1, основная +2
б. значение рН > рI, нейтральная аминокислота имеет заряд -1, кислая -2, основная -1.
Аминокислота и белок всегда имеют заряды ( + или - ), но если заряды скомпенсированы, то аминокислота или белок находятся в своей изоэлектрической точке.
Кислотно-основные свойства аминкислот
Таблица 6
-
аминокислота
рКа( СООН)
рКа( NH2)
{ a }D(в воде)
аланин
2,35
9,87
+ 8,5
4-аминомасляная кислота
4.03
10.56
аргинин
1,82
8,99
+ 12,5
аспарагин
2,14
8,72
+ 28.0
аспарагиновая кислота
1,99; 3,80
9,90
+ 25
валин
2,29
9,74
+28,3
глицин
2,35
9,78
глутаминовая кислота
2,10; 4, 07
9,47
+12,0
глутамин
2,17
9,13
+6,3
лейцин
2,33
9,74
- 11,0
лизин
2,16
9,06; 10,54( а)
+13,5
пролин
1,95
10,64
-86,2
серин
2,19
9,21
-7,5
тирозин
2,20; 10,41(ОН)
9,21
треонин
2,09
9,10
триптофан
2,46
9,41
-33,7
фенилаланин
2,20
9,31
-34,5
цистеамин (меркамин)
8,35 (SH)
10,81
цистеин
1,92; 8,37(SH)
10,70
-16,5
Среди реакций in vivo большую роль играют реакции декарбоксилирования и трансаминирования (переаминирования).
Химическая суть процесса трансаминирования (переаминирования): при ферментативном взаимодействии аминокислоты и одной из трех кетокислот (пировиноградной, щавелевоуксусной и а-кетоглутаровой) образуются кетокислота и одна из трех аминокислот (ала, асп, глу). В составе фермента витамин В6.
+ ЩУК ↔ аспартат
R – CH( NH2)– C OOH + ПВК ↔ аланин + R – C( O)– C OOH
аминокислота + а-кетоГЛУ ↔ глу кетокислота
Аминокислоты и их производные используются как лекарственные препараты.
*Глицин ( аминоуксусная кислота)-применяют подъязычно или трансбукально( всасывание через слизистую щеки) , уменьшает психоэмоцирнальное напряжение, повышает умственную работоспособность.
* Глутаминовая кислота. Препарат кислота глутаминовая(Acidum glutaminicum) Применение препарата связано с очень широким спектром действия глу – участвует в энергетическом и пластическом обмене, проявляет свойства антиоксиданта. Глу проходит через гематоэнцефалический барьер. Соли глутаминат кальция и глутаминат магния также применяют при невротических реакциях.
* Гамма-аминомасляная кислота ( ГАМК ). Препарат аминалон. Действие основано на биологической функции соединения- медиаторе торможения ц.н.с.
* Метионин ( Methioninum)- применение основано для биологической функции : источник серы для синтеза других биоактивных соединений и донор метильной группы. Назначают для профилактики и при заболеваниях печени, диабете, при дистрофии, возникающей вследствие инфекционных заболеваний
*Триптофан. Биологическая активность связана с превращением в медиатор серотонин и витамин РР. Назначают при врожденных нарушениях всасывания витамина РР.
* Цистеин (Cysteinum) –участвует в образовании биологически активных веществ антиоксидантов( глутатион), в обмене веществ хрусталика глаза.
При лечении катаракты применяют электрофорез водного раствора цистеина или глазные ванночки.
-
Ацетилцистеин – разжижает мокроту. Входит в состав препаратов, например АЦЦ.
Формулы химических соединений, изучаемых в разделе 8
L- аминокислоты организма
Алифатические аминокислоты
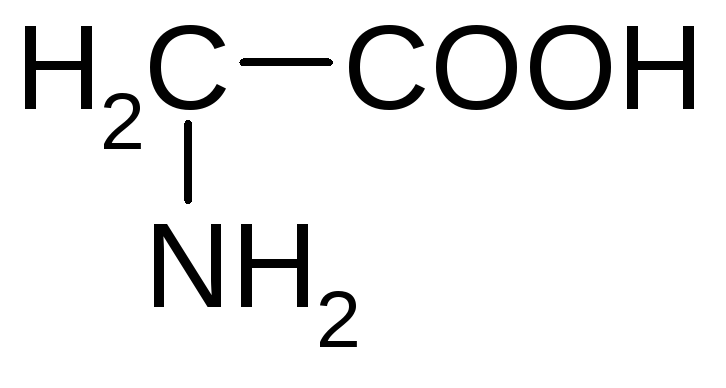
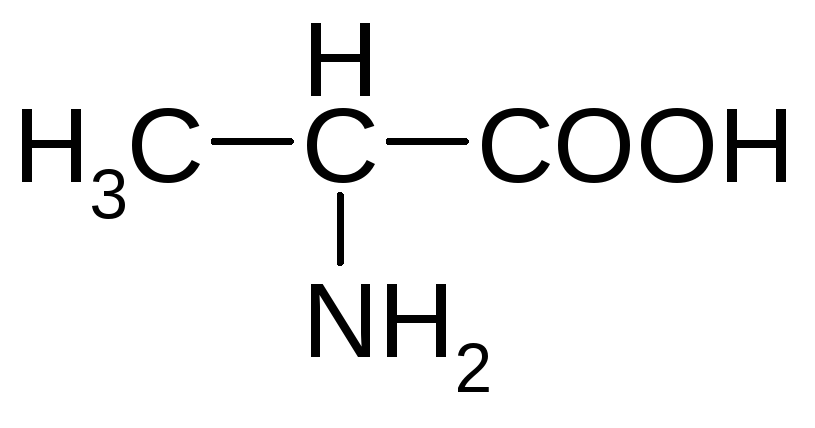

глицин аланин валин*
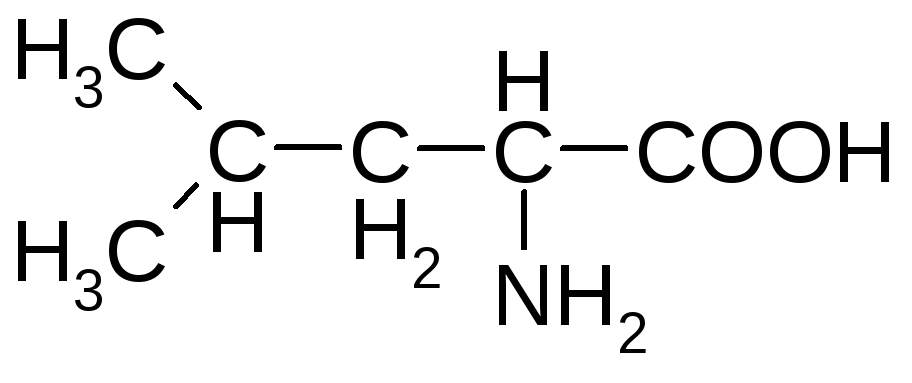
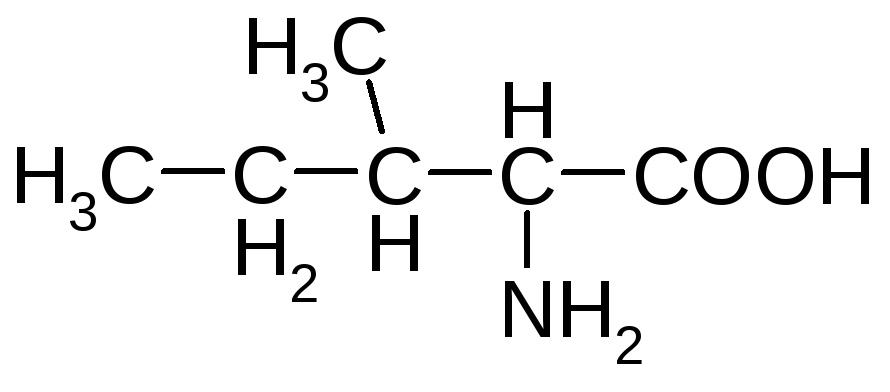
лейцин* изолейцин*
Кислые аминокислоты
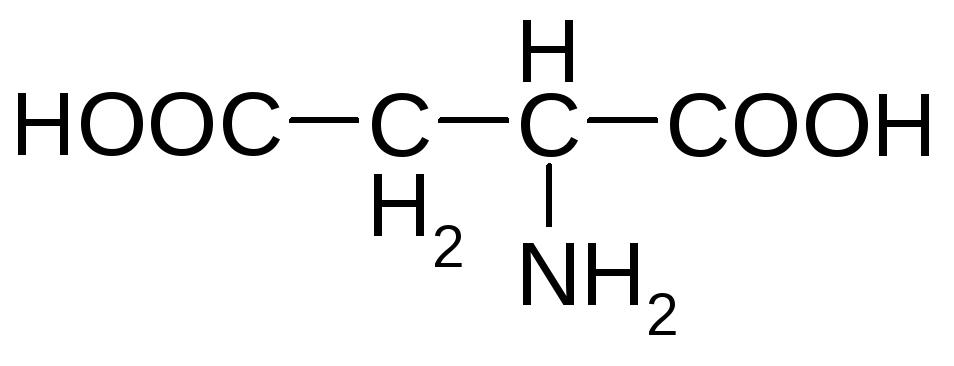
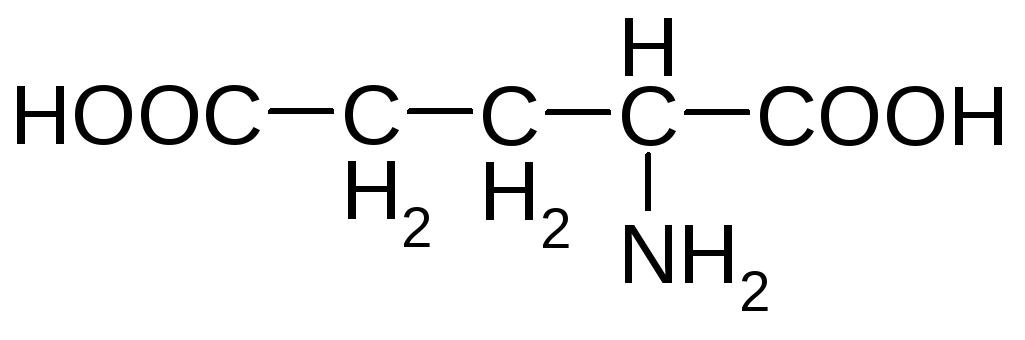
аспарагиновая глутаминовая
Основные аминокислоты
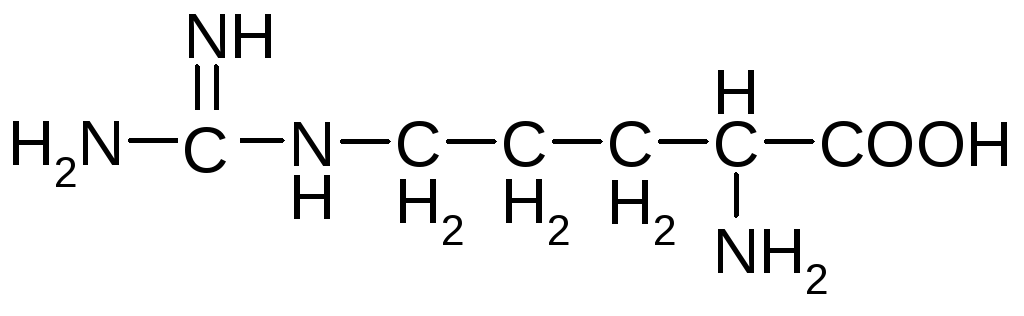
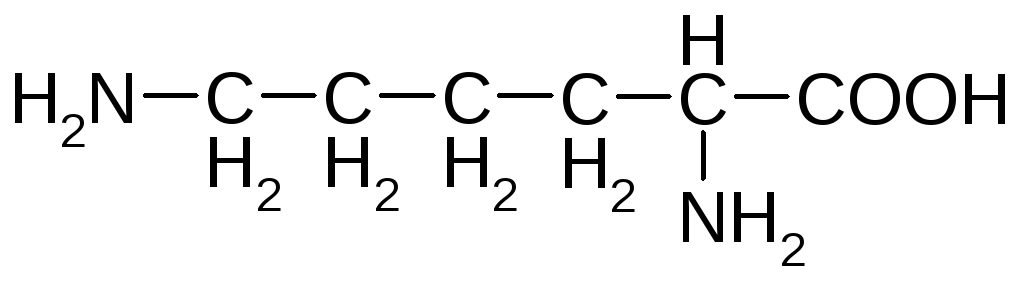
аргинин лизин*

орнитин
Аминокислоты, содержащие амидную группу
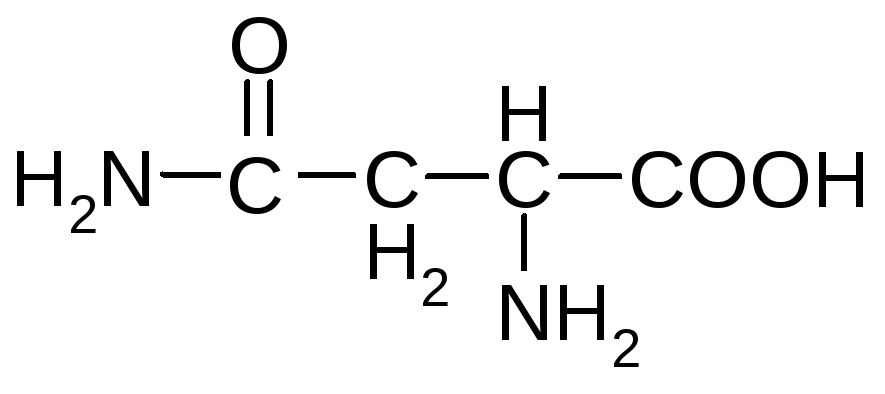
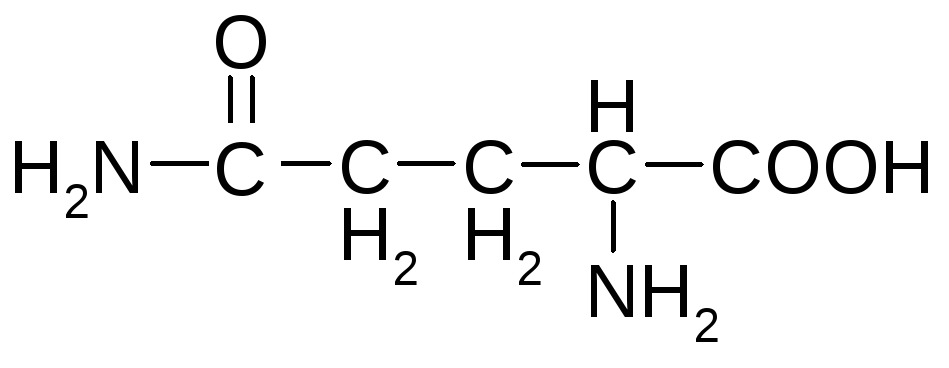
аспарагин глутамин
Серусодержащие аминокислоты
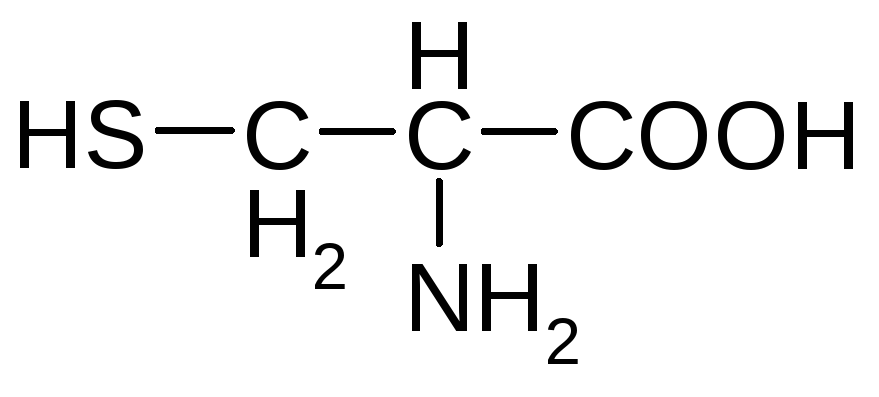
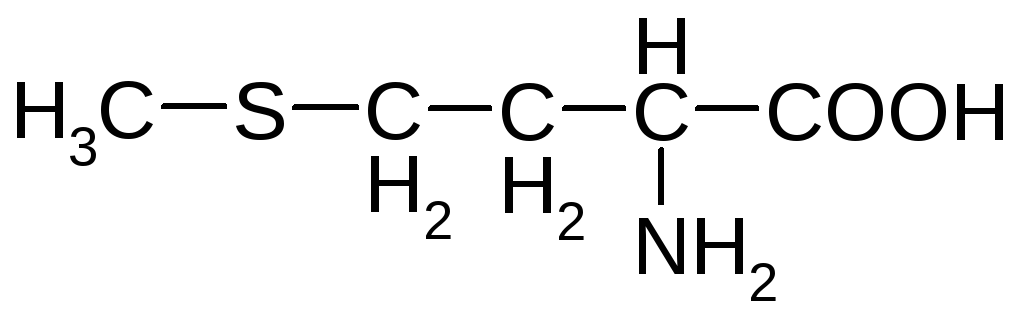
цистеин метионин*
Гидроксиаминокислоты
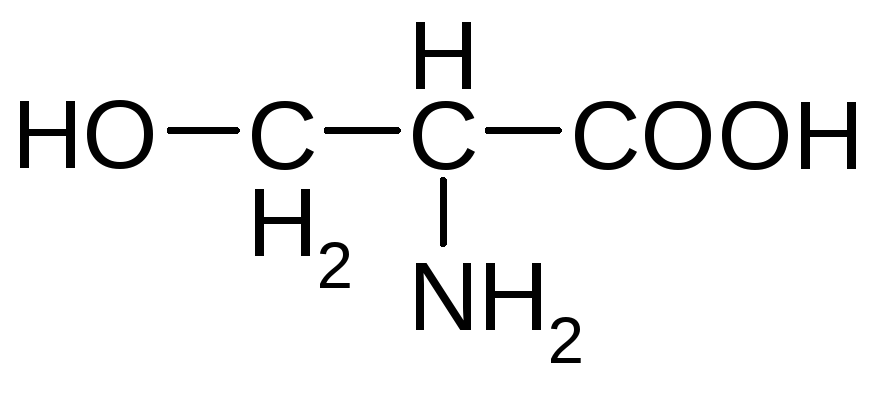
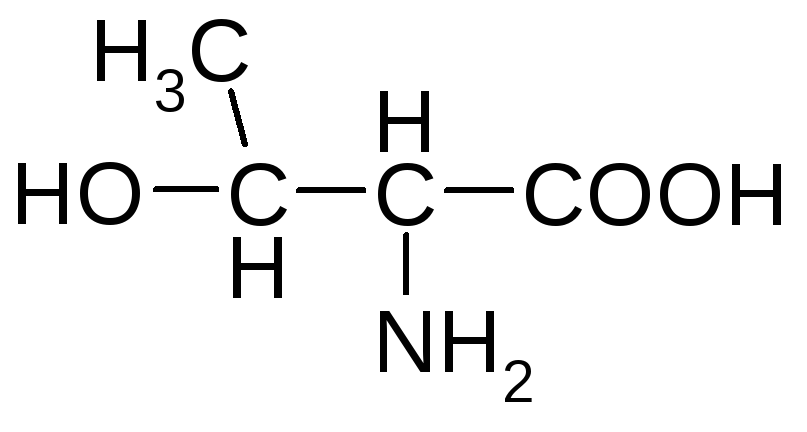
серин треонин*
Карбоциклические ароматические аминокислоты
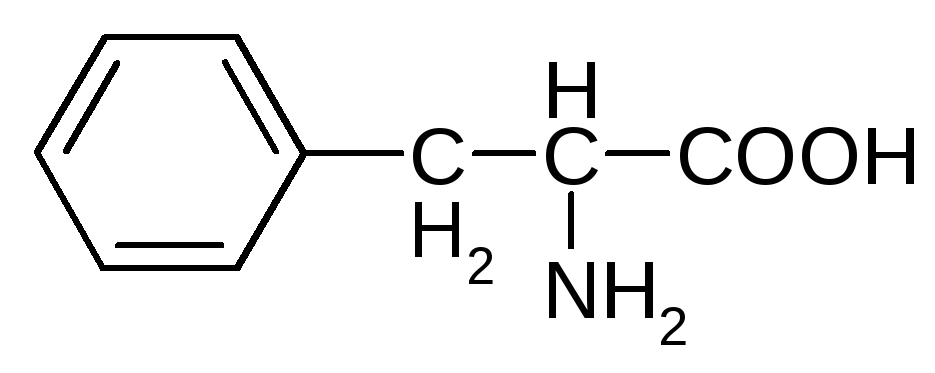
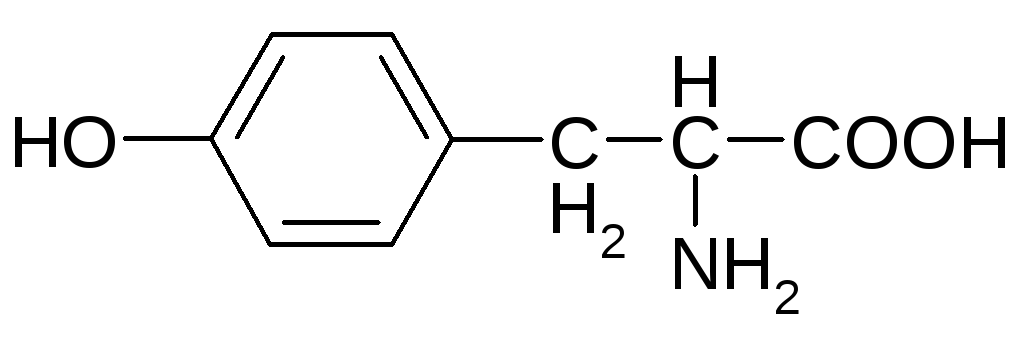
фенилаланин* тирозин
Гетероциклические ароматические аминокислоты

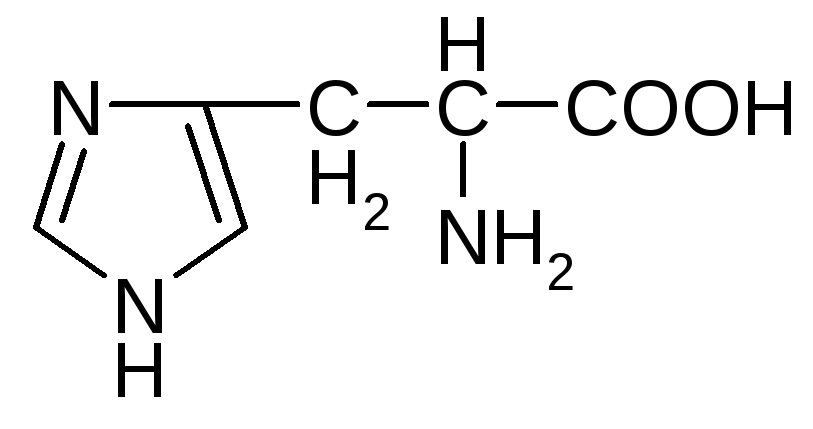
триптофан* гистидин
Циклические аминокислоты
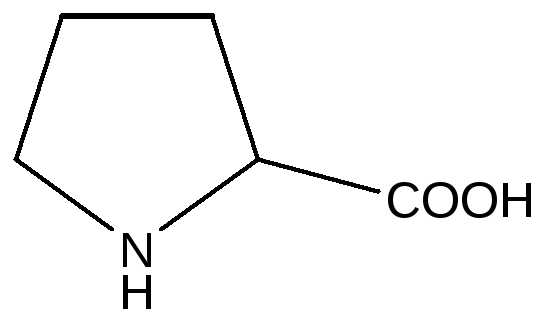
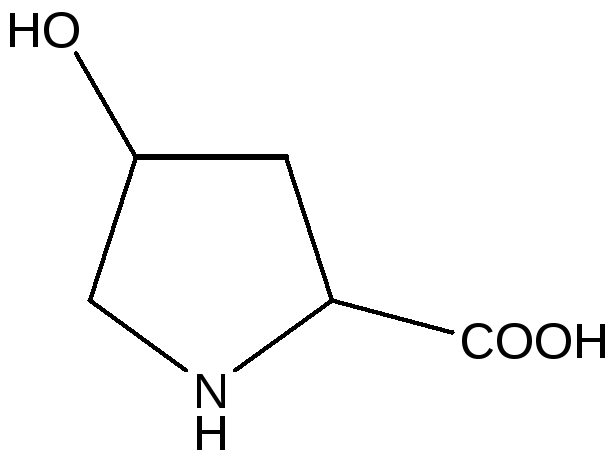
пролин 4-гидроксипролин
Обучающая задача 1
Для синтеза важнейшей биологически активной молекулы, которую называют коэнзим А, необходимо вещество β- аланин. Назовите β- аланин по номенклатуре IUPAC.Из какой природной аминокислоты in vivo по реакции декарбоксилирования образуется β- аланин?
Решение
1.В задаче указано тривиальное название неизвестного соединения -β- аланин. Очевидно, это изомер природной аминокислоты аланин, которая как и другие аминокислоты имеет а- строение.
2. Начнем с известного вещества аланина. В молекуле аланина скелет пропановой кислоты - три атома углерода. Обозначим положения а и β. Запишем формулу аланина и изомера аланина.
β а
СН3- СН- СООН СН2- СН2- СООН
| |
NH2 NH2
а- аланин β- аланин
3-аминопропановая кислота (IUPAC)
3.Перейдем к обсуждению следующего вопроса.
Для этого запишем в общем виде схему реакции декарбоксилирования а-аминокислоты и образования биогенного амина.
R- CH- COOH ——> R- CH2 - NH2 + CO2
|
NH2
Молекула CO2 отщепляется от того атома углерода, который в биогенном амине связан с аминогруппой.
5.На основании этого вывода добавим к формуле β- аланина еще одну карбоксильную группу(группа выделена другим шрифтом) и получим формулу аминокислоты, которая является источником образования β- аланина.
НООС - СН2- СН2- СООН
|
NH2
5. Название аминокислоты – аспарагиновая.
Обучающая задача 2.
Выберите условия проведения электрофореза аминокислоты глицина для введения его в ткани: на какой электрод следует нанести аминокислоту в растворе рН= 5 и рН= 8. Можно ли провести электрофорез в водной среде при рН=рI?
Решение.
1.Аминокислоты - электролиты, которые всегда имеют электрический заряд. В изоэлектрической точке рН = рI, положительный и отрицательный заряды уравновешивают друг друга, суммарный заряд равен нулю; если рН < рI, аминокислота является катионом, заряжена положительно, если рН > рI, аминокислота является анионом, заряжена отрицательно.
2. Аминокислота глицин относится к нейтральным, биполярный ион образуется в среде, близкой к рН=7. В кислой среде глицин заряжен положительно. Для обеспечения направленного движения в электрическом поле к противоположному полюсу его надо нанести на анод (+) . В щелочной среде аланин заряжен отрицательно, его наносят на катод (–).
CH2 – COO – + ОН- CH2 – COO - + Н+ CH2 – COOН
| <——> | <——> |
NH2 -Н2 О + NH3 + NH3
анион в биполярный ион катион в
щелочной среде кислой среде
3. В области рН= рI ( в изоэлектрической точке) любая аминокислота не имеет избыточного заряда. В таком растворе глицин электрофоретически неподвижен.
Обучающая задача 3
Определить среду раствора, в котором присутствует глутаминовая кислота, если заряд ее молекулы равен +1?
Решение.
1.Глутаминовая кислота относится к моноаминодикарбоновым кислотам. Ее заряд меняется в зависимости от рН среды раствора так же, как и других аминокислот.В изоэлектрической точке рН = рI суммарный заряд равен нулю, в кислой среде, если рН < рI, положительный, в щелочной среде, если рН> рI, отрицательный.
2. Положительный заряд возникнет в том случае, если диссоциация обеих карбоксильных групп подавлена, а аминогруппа присоединила протон..
Это возможно только в сильно кислой среде, если рН < рI.
НООС- СН2-СН2- СН-СООН
|
+NH3 катион глутаминовой кислоты
Обучающая задача 4
Дополните уравнение биохимической реакции трансаминирования, которая характерна для сердечной мышцы.
глу + ? ——> ? + асп
1.Реакция трансаминирования заключается во взаимодействии аминокислоты и кетокислоты. Образуются два новых вещества: тоже аминокислота и кетокислота.
(?) (?)
R1CH(NH2)-COOH + R2C(O)-COOH ——> R1C(O)-COOH + R2CH(NH2)-COOH
глу асп
На схеме реакции указаны две аминокислоты. Следовательно, надо определить кетокислоты.
3. Аминокислота глутаминовая в реакции превращается в а – кетоглутаровую кислоту (ее следует записать в правой части уравнения).
4. В результате трансаминирования получили новую кислоту аспарагиновую.
Она получается из кетокислоты щавелевоуксусной. Ее надо записать в левой части уравнения.
5.Напишем дополненную схему реакции
Глу + ЩУК ——> а-кетоГлу + асп
(запишите самостоятельно эту реакцию, используя структурные формулы)
