
- •Раздел 1. Классификация и номенклатура биоорганических соединений.
- •Раздел 2. Сопряженные системы.
- •Раздел 3 Передача электронных влияний в биоорганических соединениях. Кислотно-основные свойства биоорганических соединений.
- •Раздел 4. Изомерия биоорганических соединений
- •Раздел 5. Механизмы биоорганических реакций.
- •Раздел 6 . Классификация, номенклатура, физические и химические свойства карбоновых кислот.
- •Раздел 7. Природные биологические активные вещества липиды и высшие карбоновые кислоты
- •Раздел 8. Природные биологические активные вещества аминокислоты
- •Раздел 9. Полипептиды. Белки
- •Раздел10. Углеводы. Классификация. Моносахариды.
- •Раздел 11. Углеводы. Олигосахариды. Полисахариды.
- •(Основная связь α-1, 4, ветвление α-1, 6 через 20-25 остатков глюкозы)
- •(Основная связь α-1, 4, ветвление α-1, 6 через 8-12 остатков глюкозы)
- •Раздел 12. Нуклеиновые кислоты, нуклеотиды, нуклеозиды, азотистые основания
- •Раздел 13. Синтетические биологически активные вещества - лекарственные препараты
- •Раздел 14. Алкалоиды. Витамины.
- •Раздел 15.Реакции полимеризации и поликонденсации. Полимеры в стоматологии.
Раздел10. Углеводы. Классификация. Моносахариды.
Исходный уровень знаний для усвоения темы основан на школьной
программе органической химии, программе по биологии «Фотосинтез. Биологическая роль углеводов», разделах 1, 3 - 5 данного пособия.
Для усвоения темы и приобретения компетенции по данному разделу надо знать формулы соединений в проекциях Фишера и Хеуорса:
- триозы D,L - глицериновый альдегид, диоксиацетон, D - пентозы (рибоза, дезоксирибоза, рибулоза, арабиноза), D-гексозы (глюкоза, галактоза, манноза, фруктоза) и их энантиомеры.
- фосфорные эфиры гл – 6 - ф, гл - 1- ф, фр – 6 - ф, фр -1- ф, фр - 1,6 диф, риб -5 - ф, многоатомные спирты сорбит, манит.
- альдоновые, альдаровые, альдуроновые кислоты - глюконовая, глюкаровая, глюкуроновая.
- уметь написать схемы реакций:
образование гликозидов, окисление глюкозы бромной водой, азотной кислотой, синтез глюкуроновой кислоты, восстановление альдоз и фруктозы,
качественные реакции обнаружения альдоз ( реактив Фелинга), фруктозы ( реакция Селиванова).
Ключевые слова к теме:
Агликон , альдоза, альдоновая, альдаровая, альдуроновая кислоты, аминосахар, аномер, аномерный атом углерода , гликозид, глицит, дезоксисахар, кетоза, моносахарид, мутаротация, пираноза, структура Колли-Толленса, структура Хеоурса, фураноза, эпимеры.
Содержание раздела (Дидактические единицы)
10.1. Классификация углеводов
10.2. Моносахариды: классификация по числу атомов углерода и строению
карбонильной группы. Альдозы и кетозы. Аминосахара.
10.3. Стереоизомерия: L- и D- стереоряды моносахаров. Диастереомеры,
энантиомеры, эпимеры.
Структурная изомерия (альдозы и кетозы). Значение отдельных
представителей
10.4. Химические свойства моносахаридов.
10.4.1. Циклооксотаутомерия пентоз и гексоз. Пиранозные и фуранозные
циклы, α- и β- аномерия. Различие α - и β – аномерных форм пятичленных
фуранозных и шестичленных пиранозных циклов по расположению
полуацетальных (гликозидных, аномерных) гидроксильных групп.
10.4.2. Образование гликозидов. Биологическая роль гликозидной связи.
10.4.3. Восстановление углеводов in vitro и in vivo. Получение глицитов (на примере глюкозы и фруктозы, ксилозы).
10.4.4.Окисление углеводов in vivo и in vitro на примере глюкозы, галактозы. Образование альдоновых (оновых), альдаровых (аровых) и альдуроновых (уроновых) кислот. Биологическое значение.
10.4.5. Образование фосфорных эфиров (глюкоза-1-ф, глюкоза-6-ф, фруктоза-1,6-дифосфат). Значение для организма.
Приложение. Основы теории.
Углеводы - группа природных соединений. Большинство из них имеет состав Сn(Н2О )m (m =n , m< n )- отсюда и возникло название «углеводы», тем более, что при нагревании их без доступа кислорода образуются два вещества: углерод и вода.
Углеводы подразделяют на три класса:
- моносахариды
- олигосахариды (оligos - греч - малый )
- полисахариды.
Олиго - и полисахариды можно рассматривать как продукты поликонденсации моносахаридов, которые отличаются числом мономерных звеньев моносахаридов.
Олиго - и полисахариды могут состоять из одинаковых или различных моносахаридов. В первом случае такие полисахариды называются гомополисахариды, а во втором - гетерополисахариды.
Моносахариды классифицируют по числу атомов углерода (триозы, тетрозы, пентозы, гексозы) и строению карбонильной группы на альдозы и кетозы.
Природные аминосахара, содержащиеся в организме человека, относятся к
D- стереоряду. Конфигупацию определяют по последнему асимметрическому атому углерода (в пентозе С4, в гексозе С5)
|
пентозы: D – рибоза (ddd), 2- D-дезоксирибоза (dd), D - ксилоза (dld), D - рибулоза (dd), D- арабиноза (ddl) гексозы: глюкоза (ddld) , манноза (ddll), галактоза (dlld), фруктоза (ddl).
|
Химические свойства моносахаридов:
-цикло-оксотаутомерия,
-образование гликозидов,
- реакции восстановления, окисления
Перечисленные свойства имеют большое значение для биохимических
процессов.
Циклооксотаутомерия пентоз и фруктозы in vivo сопровождается
образованием двух аномерных фуранозных циклов , а альдогексоз
(глюкозы, маннозы, галактозы) - двух аномерных пиранозных циклов
α- и β- Аномерные формы пятичленных фуранозных и шестичленных
пиранозных циклов отличают по расположению полуацетальных
(гликозидных, аномерных) гидроксильных групп. У моносахаридов D-ряда
α - форме аномерный гидроксил расположен в внизу, а в β - форме вверху
(формулы Хеуорса)


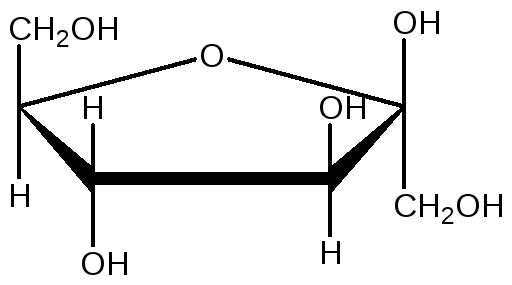
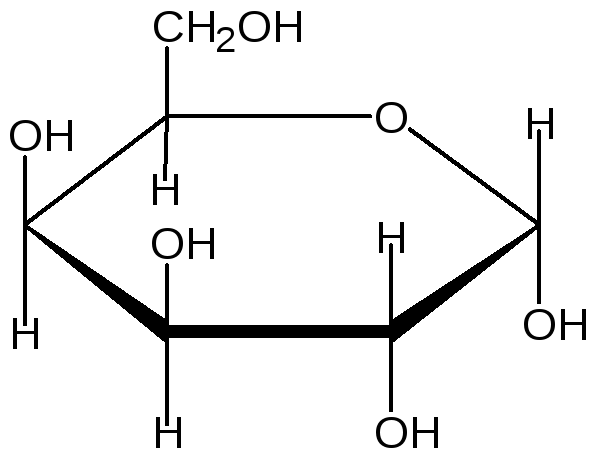
β-D-фруктофураноза α-D-Галактопираноза
( скобкой выделены аномерные гидроксильные группы)
Гликозиды получаются в результате реакции SN. Признак гликозида - замещение атома водорода в аномерной гидроксильной группе на радикал.
Восстановление углеводов in vitro и in vivo приводит к образованию глицитов. При восстановлении фруктозы и других кетоз образуются два спирта - два диастереомера.
С 6Н12О6 + [ 2Н ] ——> С6Н14О6
глюкоза сорбит
манноза маннит( ол)
галактоза галактиол (дульцит )
фруктоза сорбит + маннит
Образование двух спиртов связано с тем, что при восстановлении карбонильной группы образуется хиральный атом водорода, имеющий два зеркальных изомера.
| +2H | +2H |
HO – C – H ↔ C=O ↔ H – C – OH
| | |
L – альдоза кетоза D – альдоза
Моносахариды используются как лекарственные препараты.
Глюкоза (Glucosum)
В крови содержание глюкозы поддерживается в интервале 3, 3 -5, 5 мМоль/л ( 80 -120 мг в 100мл крови или 4-6 г в объеме всей крови ).
Свободная глюкоза встречается в виноградном соке и соке спелых сладких фруктов, в растениях она запасается в составе олигосахарида сахарозы или полисахарида крахмала.
Глюкоза и многие гексозы, их олиго - и полисахариды подвергаются «брожению», так называют процессы превращения углеводов с участием микроорганизмов
Спиртовое брожение
С6 Н12 О6 —— ферменты —— > 2 С2 Н5 ОН + 2 СО2
Молочнокислое брожение( в мышцах этот процесс носит название анаэробный гликолиз)
С6 Н12 О6 —— ферменты —— > 2 С3 Н6 О3 ( молочная кислота)
Препараты глюкозы (Glucosum, Dextrosum) выпускают в виде порошков, таблеток, стерильных растворов, добавляют в другие лекарственные средства..
Растворы стерилизуют при температуре от 1000 до 1210. для стабилизации добавляют 0,1Н раствор НСl. Для внутривенного введения используют изотонические растворы 4,0-4,5% (изотонический раствор имеет осмотическое давление соответствующее осмотическому давлению крови) и гипертонические 10—40% (выше осмотического давления крови).
Изотонические растворы применяют при кровопотере для возмещения объема циркулирующей крови, глюкоза вызывает усиление энергетических процессов в тканях. Гипертонические растворы повышают осмотические давление, усиливают отток жидкости из тканей в кровь, способствуют выделению из органов токсических веществ и увеличивают поступление глюкозы в мозг, сердце, печень, мышцы.
Глюконат кальция – соль глюконовой кислоты (Calcii gluconas)
Препарат используют как источник кальция. Преимущества : пригоден для внутримышечного и подкожного применения в отличие от хлорида кальция, который вводят в экстренных случаях только внутривенно.
Маннит ( Mannitum)
Получают при восстановлении маннозы, шестиатомный спирт С6 Н14 О6. белый кристаллический порошок, хорошо растворимый в воде. Гипертонические растворы оказывают очень сильное диуретическое
( мочегонное) действие. Применяют в виде 10-20% растворов для внутривенного введения.
Ксилит – нашел широкое применение в составе зубных паст, ополаскивателей полости рта, жевательных резинок, обладает свойством подавлять развитие патогенной микрофлоры полости рта.
Глюконовая кислота – естественный метаболит, образуется во всех клетках организма в процессе обмена глюкозы в пентозофосфатном цикле.
Глюкуроновая кислота – входит в состав гиалуроновой кислоты (см. раздел 11 «Полисахариды»)
Обучающая задача 1.
1. Найти моносахарид, который записан двумя разными структурными формулами: Колли-Толленса и Хеуорса.
Решение.
1. Моносахариды записывают формулами Колли-Толленса, располагая атомы углеродного скелета вертикально. Цифровую нумерацию проводят сверху вниз от старшей группы, а обозначение конфигурации асимметричных центов снизу вверх, начиная от первого снизу хирального атома.
а) б) в) г)






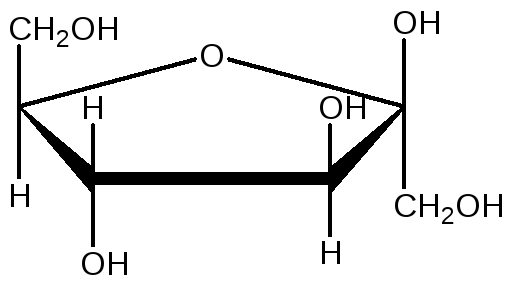

обозначение хиральных атомов
2. В соединениях а и б по 6 атомов углерода, они содержат альдегидную группу- это альдогексозы. В соответствии с конфигурацией атомов соединение а) является D -глюкозой (d d l d ), соединение б) - D -маннозой (d d l l ).
3. Формулы Хеуорса отражают циклические формы моносахарида. Пятичленный цикл называется фураноза, шестичленный цикл - пираноза. Фуранозный цикл характерен для пентоз и кетогексозы фруктозы. Пиранозный цикл типичен для природных альдогексоз.
4. Соединение в) представляет собой пятичленный цикл и не может быть альдогексозой ( in vivo встречаются только пиранозные формы альдогексоз).
5. Чтобы определить, соответствие формулы Хеуорса г) формулам Колли-Толленса, необходимо определить конфигурацию асимметричных атомов углерода в циклической формуле. Известно, что в случае d - конфигурации гидроксильная группа записывается внизу, для l - конфигурации – вверху.
Атом кислорода в «верхнем углу» цикла обозначает принадлежность к D-
ряду. Начнем определять конфигурацию атомов в указанных стрелками
направлении: атомы 5-4-3-2. Конфигурации: 5(d) – 4 (d) – 3 (l) -2(d)
соответствует D – глюкозе (формула Колли-Толленса «а» )
6. Альдогексоза D – глюкоза представлена формулами а) и г).
Обучающая задача 2
Дополните схему реакции так, чтобы получились указанные вещества:
Назовите полученное соединение.


Решение
1. Начнем решение с анализа полученного соединения. Это углевод в пиранозной форме, в нем 6 атомов углерода. В полуацетальной (гликозидной) гидроксильной группе, имеющей β- конфигурацию, ( гликозидная группа выделена скобкой), атом водорода замещен на метильный радикал, следовательно, это соединение является β- гликозидом. Полное название β- D-О-метилгалактопиранозид. Метильная группа в гликозиде является агликоном, т.е. неуглеводной частью.
3. Какой моносахарид образовал гликозид? Это D- галактоза (узнали по конфигурации асимметричных атомов углерода в гликозиде (d l l d), образованном β- D-галактопиранозой.
2. Поставим вопрос, какой известен способ получения гликозидов?
Моносахарид смешивают со спиртом и пропускают сухой газ хлороводород.
В данной реакции моносахарид D –галактоза (в виде β- D-галактопиранозы)
реагирует с метиловым спиртом.
Формулы химических соединений, изучаемых в разделе 10
Пентозы
D-Рибоза 2-дезокси-D-рибоза D-Ксилоза D-Ксилулоза

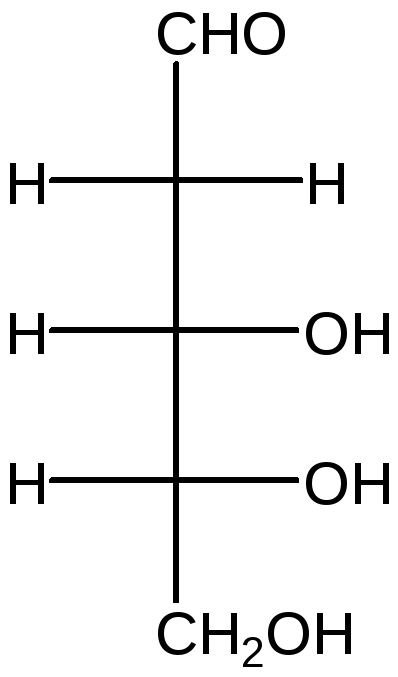
Гексозы
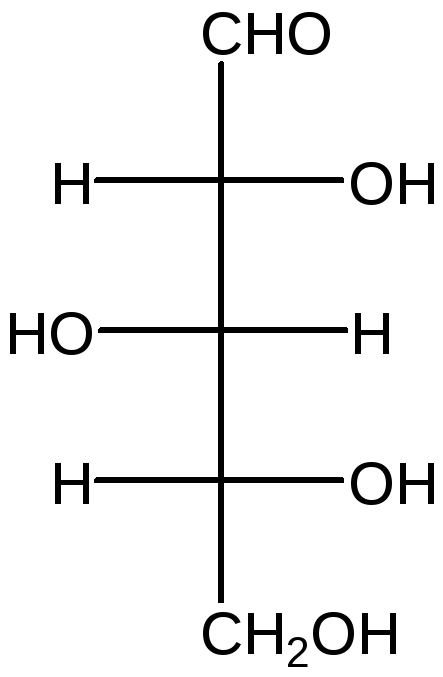
Глюкоза
β-D-Глюкопираноза D-Глюкоза(ddld) α-D-Глюкопираноза
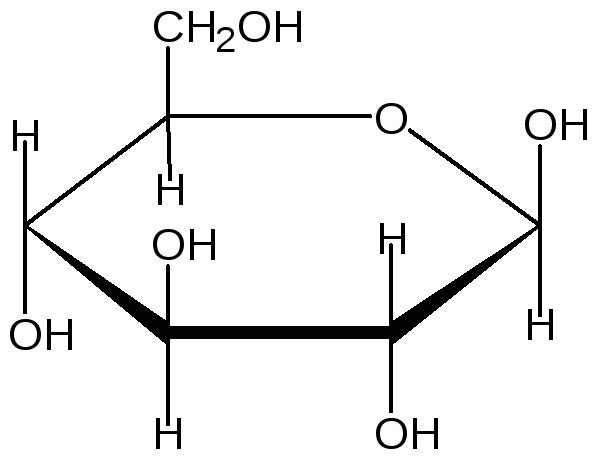
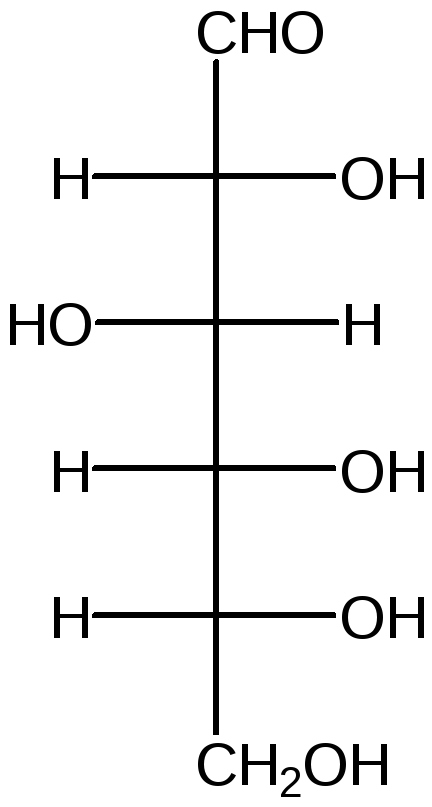
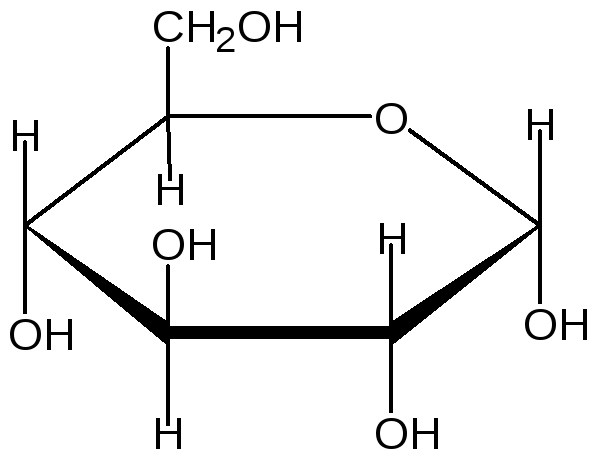
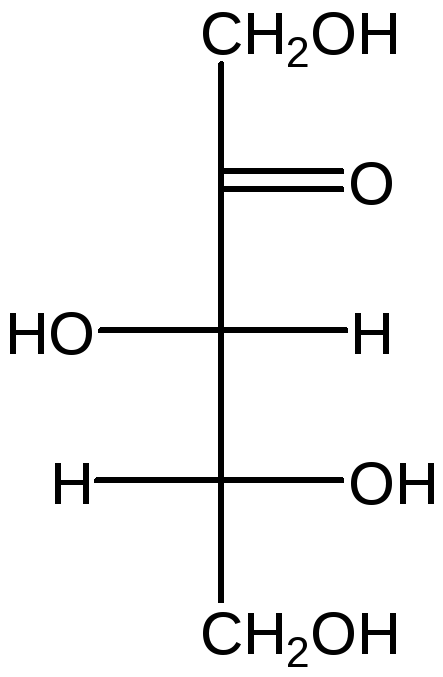
D –Манноза (ddll) D – галактоза (dlld) D – фруктоза (ddl)
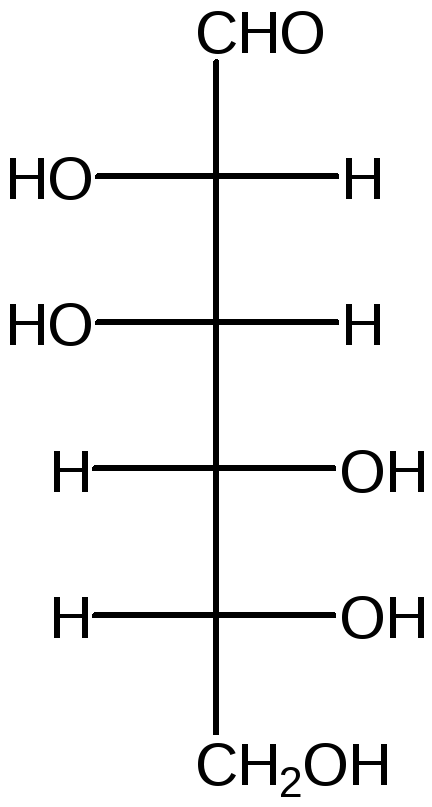
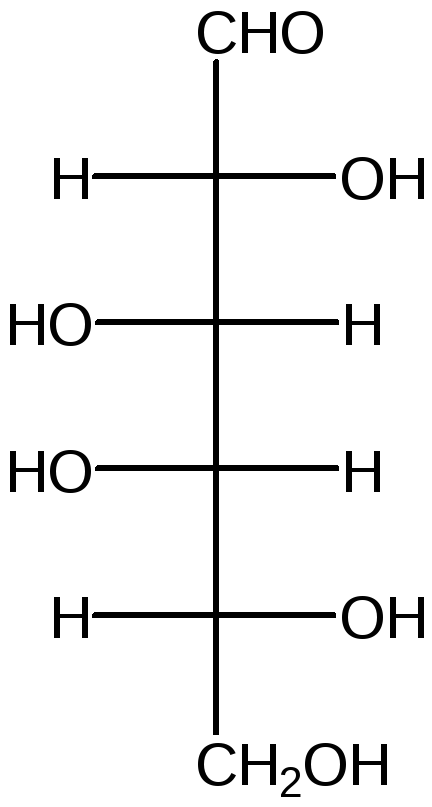

Формулы Хеуорса
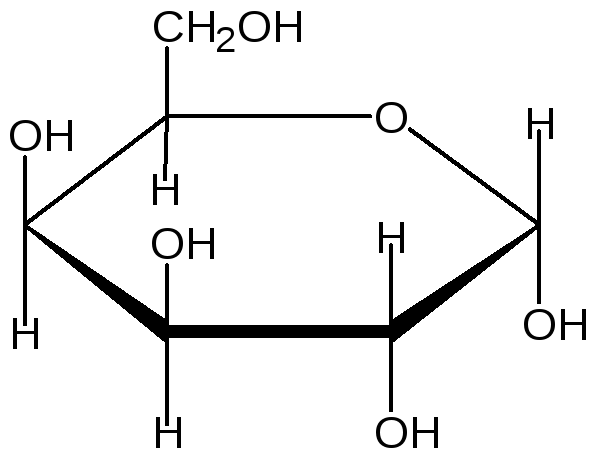

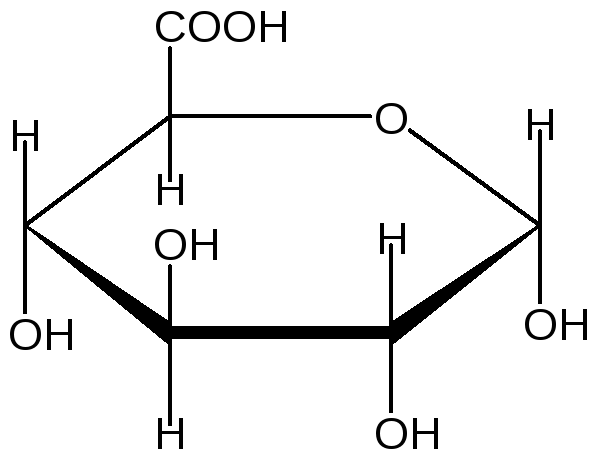 α -
D- Галактопираноза β-D-фруктофураноза
α - D- пиранозная форма
α -
D- Галактопираноза β-D-фруктофураноза
α - D- пиранозная форма
глюкуроновой кислоты
Глициты – многоатомные спирты, производные моносахаридов

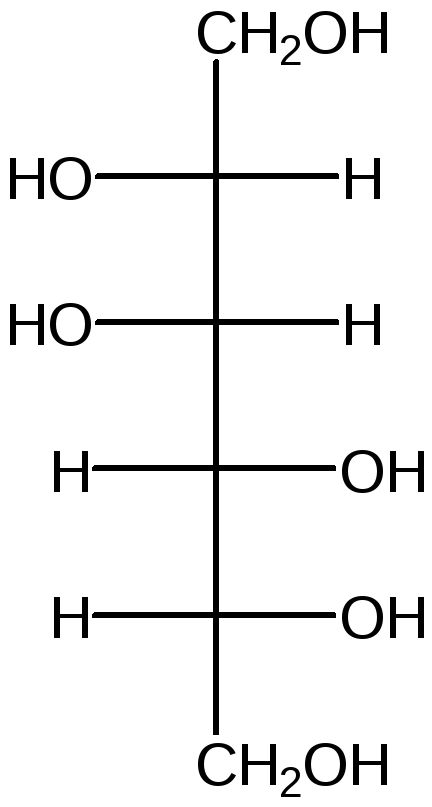
D-Сорбит D-Маннит
