
Журнал неврологии и психиатрии / 2009 / NEV_2009_12_076
.pdf
ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
Комбинированная терапия активно протекающего ремиттирующего рассеянного склероза митоксантроном в сочетании с копаксоном
Врач Д.В. САЗОНОВ1,2, д.м.н. Н.А. МАЛКОВА1,2,3, врач Е.В. БУЛАТОВА2, к.м.н. О.В. РЯБУХИНА1
Combined therapy of aggressive remitted multiple sclerosis with mitoxantron in combination with copaxon
D.V. SAZONOV, N.A. MALKOVA, E.V. BULATOVA, O.V. RYABUKHINA
1Окружной центр рассеянного склероза; 2Областной центр рассеянного склероза, Новосибирск; 3Кафедра клинической неврологии и алготерапии факультета повышения квалификации Новосибирского государственного медицинского университета
Лечили больных с так называемым агрессивным рассеянным склерозом. Агрессивным считают течение заболевания, при котором имеются клинические и томографические признаки высокой активности болезненного процесса с частотой обострений не менее 3 за 2 года. Наблюдали 9 больных с таким течением. Для лечения применяли комбинированную терапию, включавшую фазу индукции, в которой ведущими являются иммуносупрессивные препараты, и фазу поддерживающей терапии препаратами ряда иммуномодуляторов. Для наиболее эффективного использования возможностей комбинированной терапии был разработан вариант на основе препаратов с разнонаправленными механизмами действия — митоксантрона и копаксона. Установлены стабилизация и улучшение состояния больных (77,8%) с уменьшением частоты обострений.
Ключевые слова: высокоактивной (агрессивный) ремиттирующий рассеянный склероз, митоксантрон, копаксон, комбинированная терапия.
Patients with so called aggressive multiple sclerosis were treated. The course of disease is considered aggressive if there are clinical and tomographic signs of high disease activity with the frequency of exacerbations not less than 3 during 2 years. Nine patients with this course of disease were examined. They received a combined therapy including the induction phase in which immunosuppressive drugs played a key role, and a phase of supporting therapy with immunomodulators. A variant based on drugs with opposite mechanisms of action (mitoxantron and copaxon) was worked out for the most effective using of possibilities of combined therapy. Stabilization and improvement of a patient’s state by 77,8%, along with a reduction of exacerbation frequency, was found.
Key words: highly active (aggressive) remitted multiple sclerosis, mitoxantron, copaxon, combined therapy.
Рассеянный склероз (РС) — прогрессирующее аутоиммунное заболевание, в основе патогенеза которого лежит хронический процесс воспалительной демиелинизации и нейродегенерации в центральной нервной системе, проявляющиеся вариабельной неврологической симптоматикой [1, 3]. Обычно заболевание начинается в молодом возрасте и практически неизбежно ведет к инвалидизации. Выключение в связи с этим большого числа трудоспособных людей из активной жизни, большие расходы на диагностику, лечение, реабилитацию и социальную помощь делают проблему РС социально и экономически значимой [2].
Общепринято мнение, что РС, самое распространенное демиелинизирующее заболевание, является мультифакториальным. Его развитие обусловлено действием факторов внешней среды (вируса и/или другого патогена, экологических и географических факторов) и наследственной предрасположенностью, реализуемой полигенной системой, включающей особенности иммунного ответа и определенного типа метаболизма [4]. Сочетание внешних и генетических факторов в конечном итоге приводит к развитию аутоиммунного процесса, направленного против нервной ткани с образованием очагов демиелинизации и нейродегенерации [6].
Рассеянный склероз — заболевание с доказанным аутоиммунным патогенезом, поэтому все стратегии лечения с доказанной эффективностью так или иначе имеют в механизме своего действия точки приложения в иммунной системе. При ремиттирующей форме РС активно используются препараты интерферонов-β (ребиф, авонекс, бетаферон) и глатирамера ацетат (копаксон), относящиеся к группе иммуномодуляторов. На более поздних стадиях заболевания и в тех случаях, когда течение приобретает злокачественный характер, либо является таковым с самого начала, иммуномодулирующей терапии недостаточно и встает вопрос о назначении иммуносупрессивных препаратов. Традиционно в этой ситуации применяли некоторые цитостатики — циклофосфан, метотрексат и азатиоприн. В последние годы все более широкое применение в терапии РС находят так называемые цитостатики второго поколения — синтетические противоопухолевые препараты, которые обладают узконаправленным действием на иммунокомпетентные клетки, такие как кладрибин и митоксантрон. Они имеют меньше побочных эффектов по сравнению с препаратами первого поколения и лучше переносятся больными.
В терапии быстро прогрессирующего РС наиболее широко применяется лечение митоксантроном в сочетании с метилпреднизолоном.
© Коллектив авторов, 2009 |
1e-mail: d.sazonov_ocrs@mail.ru |
Zh Nevrol Psikhiatr Im SS Korsakova 2009;109:12:76
76 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2009 |

ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА
Митоксантрон — синтетический противоопухолевый препарат. В онкологии митоксантрон применяют в основном при гемобластозах: неходжкинских лимфомах, острых лейкозах у взрослых, при обострениях хронического миелолейкоза, также он используется при метастазирующем раке молочной железы. Митоксантрон реализует свое противоопухолевое действие, интерполируясь в ДНК и образуя разрывы цепи ДНК и межцепевые связи. Таким образом, препарат избирательно подавляет пролиферацию быстро делящихся клеток. Механизм действия препарата при РС связан с подавлением активности Th1хелперов, В-клеток и стимуляцией апоптоза воспалительных Т-клеток. В последних исследованиях [12] показано, что митоксантрон помимо уже известного влияния на Т-клетки значительно снижает уровень аутореактивных В-клеток.
Наиболее масштабным клиническим исследованием эффективности и безопасности митоксантрона было международное многоцентровое исследование MIMS (Mitoxantrone in progressive multiple sclerosis), выполнявшееся в Германии, Бельгии, Венгрии и Польше. Было установлено, что митоксантрон хорошо переносится, позволяя сокращать прогрессирование инвалидизации и клинических осложнений [10].
По сравнению с другими химиопрепаратами митоксантрон относительно прост в применении и имеет минимальное количество побочных эффектов. Тем не менее, при применении митоксантрона, как и других аналогичных химиотерапевтических препаратов, возможно угнетение кроветворения (лейкопения, тромбоцитопения, реже
— эритроцитопения). Препарат обладает кардиотоксичностью, проявляющейся в форме кардиомиопатии, в сокращении фракции выброса левого желудочка, появлении аритмий и в ряде случаев ишемических поражений миокарда, поэтому общая доза на протяжении всей жизни, превышающая 140 мг/м2 поверхности тела, не рекомендуется. Могут возникать тошнота, рвота, понос, общая слабость, повышение температуры тела, аменорея, алопеция и другие побочные эффекты. Наиболее серьезным из отсроченных побочных эффектов является развитие митоксантрон-индуцированных гемобластозов, протекающих чаще всего в виде острого лимфобластного лейкоза. Кроме того, существует опасение, что митоксантрон может увеличить вероятность развития злокачественных опухолей в будущем, поскольку его влияние на ДНК допускает теоретическую возможность мутагенного и канцерогенного действия.
При лечении пациентов с быстро развивающимся ремиттирующим РС предпочтительными являются схемы комбинированной терапии, включающие фазу индукции, в которой ведущими являются иммуносупрессивные препараты, и фазу поддерживающей терапии препаратами ряда иммуномодуляторов. Использование схем комбинированной терапии дает ряд преимуществ: во-первых, они позволяют снизить суммарную дозу иммуносупрессантов, что значительно уменьшает риск развития осложнений; во-вторых, становится возможным проведение нескольких (от 3 до 4) коротких стабилизирующих курсов иммуносупрессивной терапии в случае последующего ухудшения состояния больного.
Выбор препаратов для комбинированной терапии, а также построение протоколов лечения должны проводиться с учетом особенностей механизма действия препаратов,
спектра их побочных эффектов, особенностей введения иммуносупрессантов и иммуномодуляторов. Первыми были применены протоколы комбинированной терапии на основе препаратов β-интерферонов: ребиф + метотрексат [7], бетаферон + азатиоприн [11], бетаферон + митоксантрон [9]. Эти схемы разрабатывались в первую очередь на основании общности механизмов действия этих препаратов — снижении проницаемости гематоэнцефалического барьера и прямом противовоспалительном действии. Они показали свою эффективность и хорошую переносимость, однако не было достигнуто значительного расширения механизмов действия комбинаций препаратов по сравнению с монотерапией. Для наиболее эффективного использования возможностей комбинированной терапии были разработаны варианты лечения на основе препаратов с разнонаправленными механизмами действия — митоксантрона и копаксона.
Первым сообщением об эффективности лечения высокоактивного ремиттирующего РС с помощью последовательной поддерживающей терапии копаксоном после проведения стабилизирующих курсов митоксантрона была работа британских исследователей, опубликованная в 2006 г. [13]. За ней последовало крупное исследование эффективности комбинированной терапии митоксантроном и копаксоном американских коллег, опубликованное в 2008 г. [8, 14].
По результатам этих исследований был сделан вывод о высокой эффективности комбинированной терапии митоксантроном в сочетании с копаксоном, превышающей эффективность монотерапии копаксоном при «агрессивном» течении ремиттирующего РС как по клиническим (частота обострений), так и по томографическим (число гадолиний-накапливающих очагов) данным. Большинство нежелательных эффектов терапии связано с митоксантроном, но их выраженность остается умеренной и не требует прекращения терапии.
Целью настоящей работы являлась оценка эффективности, безопасности и переносимости комбинированной терапии высокоактивного (агрессивного) ремиттирующего РС митоксантроном в сочетании с копаксоном.
Задачи исследования были следующие: 1) оценить клинические и томографические показатели эффективности комбинированной терапии агрессивного ремиттирующего РС митоксантроном в сочетании с копаксоном; 2) оценить клинические и параклинические показатели безопасности и переносимости комбинированной терапии агрессивного ремиттирующего РС митоксантроном в сочетании с копаксоном.
Материал и методы
Агрессивным считается такое течение ремиттирующего РС, при котором у пациента наблюдаются высокие показатели клинической и томографической активности процесса: частота обострений не менее 3 за 2 года, как правило, с неполным восстановлением, накоплением остаточного неврологического дефицита и активными очагами на МРТ.
При отборе пациентов для комбинированной терапии митоксантроном в сочетании с копаксоном мы руководствовались определенными критериями включения и исключения.
Критерии включения были следующие: возраст больных от 18 до 55 лет; достоверный диагноз ремиттирующего
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2009 |
77 |
ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
РС, согласно критериям W. Ian McDonald, 2005; степень инвалидизации по шкале EDSS 3,0—6,5 баллов; продолжительность заболевания более 1 года; как минимум 3 клинически подтвержденных обострения за последние 2 года; высокая активность болезни (прибавление 1,0 и более баллов EDSS за последний год); активные контрастируемые очаги по данным МРТ; достаточная мотивация больного.
Критериями исключения являлись: прогрессирующие формы РС; оценка по шкале Куртцке EDSS менее 3 и более 6,5 баллов; частота обострений 1 раз в год и менее; психическая патология; тяжелая сопутствующая соматическая патология; несогласие больного.
Наблюдали 9 больных (5 мужчин и 4 женщины) с агрессивным ремиттирующим РС. Их средний возраст к началу терапии составил 26,1 года (колебания от 21 до 33 лет). Средняя длительность заболевания к началу терапии составила 4,8 года (1,5—12 лет). Два пациента завершили лечение, 7 продолжают терапию. На момент начала терапии все пациенты имели ремиттирующее течение, оценка неврологического дефицита по шкале EDSS в среднем составила 5,3 балла (4—6) до начала терапии. Частота обострений составляла 1,3 в год. Средняя скорость прогрессирования составила 1,8 балла в год.
При выборе стратегии терапии митоксантроном использовали модифицированную схему J. Ramtahal и соавт. [13]. Пациенты получали по 12 мг/м2 поверхности тела ежемесячно в первые 3 месяца (3 курса) с переходом на 6 мг/м2 1 раз в 3 месяца (2 курса) и назначением копаксона по 20 мг подкожно ежедневно с 4-го месяца. Учитывая, что все пациенты на момент включения находились в состоянии обострения заболевания, мы сочли целесообразным к основной терапии митоксантроном добавить внутривенное введение стероидных препаратов — метилпреднизолон 1000 мг [5] в течение первых 3 мес. Сочетание митоксантрона с метилпреднизолоном в течение первых 3 мес рассматривалось как индуцируюшая фаза, а последующее введение митоксантрона с копаксоном — как фаза поддерживающая.
Анализ эффективности терапии в нашем исследовании мы проводили с использованием показателей частоты обострений, балла EDSS до начала исследования и на момент последней оценки состояния.
Всем больным была проведена магнитно-резонансная томография (МРТ) головного мозга с контрастированием; перед началом лечения и после заключительного курса терапии митоксантроном была проведена также эхокардиография для исключения вероятной кардиомиопатии; ЭКГ осуществлялась перед каждым введением препарата. Все больные проходили общеклиническое обследование: общий анализ крови с подсчетом лейкоцитарной формулы, общий анализ мочи, биохимический анализ крови, оценку жизненно важных показателей (АД, ЧСС, ЧД) и соматического статуса как минимум раз в 3 месяца.
Результаты и обсуждение
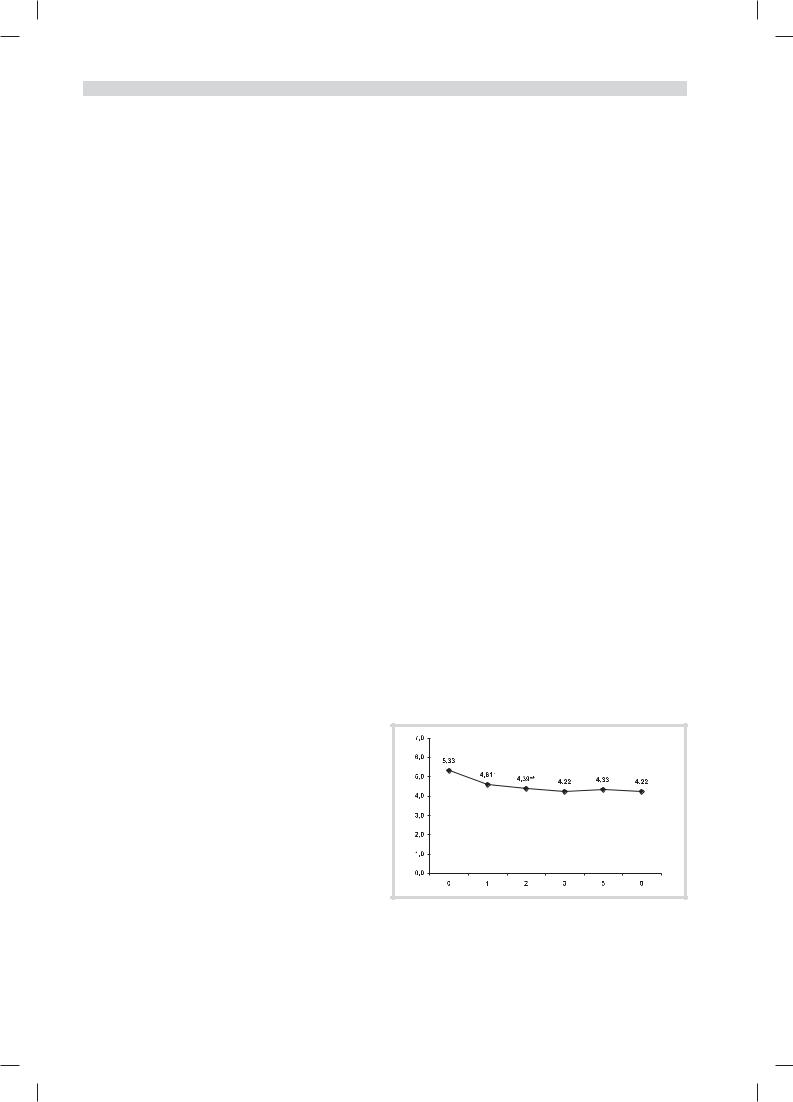
Среднее исходное значение EDSS (перед проведением первого курса терапии) составило 5,3 балла. К 8-му месяцу терапии средний балл EDSS снизился на 1,1 балла (с 5,3 до 4,2). Динамика этих показателей в процессе терапии представлена на рисунке.
Эффективность лечения, оцениваемая по изменению показателей инвалидизации по шкале EDSS, была следу-
ющей; с улучшением — 7 (78%) больных, с ухудшением
— 2 (22%).
Частота обострений, составлявшая до начала лечения 1,3 в год, на фоне проведения терапии уменьшилась до 0,5 обострений в год. При этом 6 (66,7%) пациентов после начала терапии не имели ни одного обострения в течение как минимум 12 мес, а также не имели новых или контрастнакапливающих очагов на МРТ спустя 6 и 12 мес после начала терапии.
Таким образом, можно сделать вывод о высокой эффективности терапии агрессивного ремиттирующего РС митоксантроном в сочетании с копаксоном.
В 2 случаях терапия была недостаточно эффективной. Приводим краткие сведения об этих пациентах.
Больная П., 21 год, заболела в возрасте 17 лет, дебют
— с нарушения двигательных функций (выраженная слабость в ногах после умеренной физической нагрузки). На момент начала терапии митоксантроном длительность заболевания была 4,5 года, степень инвалидизации по шкале EDSS — 6,0 балла, скорость прогрессирования — 1,33 балла в год. До включения в программу пациентка в течение 1 года получала терапию бетафероном, на фоне которой зафиксировано 3 обострения.
После введения 1-й дозы митоксантрона у пациентки на ЭКГ зарегистрирована частая экстрасистолия с нагрузкой на правые отделы сердца, но без выраженных гемодинамических нарушений по данным эхокардиографии. Ко времени 2-го введения митоксантрона (через 1 мес) нарушения на ЭКГ выражались в редких экстрасистолах, однако после проведения курса терапии ситуация повторилась. На основании этого было решено уменьшить дозу митоксантрона до 5 мг/м2. За период до начала терапии копаксоном инвалидизация больной не уменьшилась, составляя 6,0 балла по шкале EDSS. На момент 4-го введения митоксантрона у пациентки было зафиксировано обострение, выражавшееся в усугублении двигательного дефицита (потребовалась двусторонняя поддержка при передвижении), в связи с чем в лечение были добавлены кортикостероиды (метилпреднизолон 1000 мг в течение 3 дней) и плазмаферез (3 сеанса), через 3 нед обострение было купировано. Пациентка продолжала терапию копаксоном, на фоне чего было зарегистрировано повторное обострение через 2 мес после предыдущего со схожей
Динамика степени инвалидизации по шкале EDSS на фоне ком- |
бинированной терапии митоксантроном с копаксоном. |
По оси абсцисс — месяцы после начала терапии, по оси ординат — баллы по шкале EDSS. Достоверные изменения по сравнению с исходным уровнем: * — р<0,01; ** — p<0,05.
78 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2009 |

|
ЛЕЧЕНИЕ РАССЕЯННОГО СКЛЕРОЗА |
симптоматикой, потребовавшее аналогичную дополни- |
первых, не рекомендуется переводить пациента на моно- |
тельную терапию. В связи с очевидной неэффективно- |
терапию копаксоном в том случае, если он по какой-либо |
стью комбинированной терапии пациентка, начиная с |
причине (особенно ввиду плохой переносимости миток- |
5-го введения митоксантрона, была переведена на имму- |
сантрона) не получил в течение 3 первых введений его |
носупрессивную терапию митоксантроном в сочетании с |
полную расчетную дозу (30 мг/м2 поверхности тела). Во- |
метилпреднизолоном с половинной дозировкой миток- |
вторых, эффект от комбинированной терапии митоксан- |
сантрона ввиду неудовлетворительной переносимости |
троном в сочетании с копаксоном может оказаться со- |
полных доз. |
мнительным в том случае, если на фоне предшествующей |
Больной О., 30 лет, заболел в возрасте 27 лет. Заболева- |
терапии копаксоном длительностью не менее полугода у |
ние началось с мозжечковых нарушений, глазодвигатель- |
пациента отмечалась очень высокая частота обострений и |
ных расстройств (выраженная атаксия, головокружение, |
скорость прогрессирования заболевания. В таких случаях |
двоение в глазах при взгляде во все стороны и прямо). На |
рекомендуется проведение иммуносупрессивной терапии |
момент начала терапии митоксантроном длительность за- |
митоксантроном в сочетании с метилпреднизолоном. |
болевания составила 2,5 года, степень инвалидизации по |
Что касается нежелательных эффектов, то в наблю- |
шкале EDSS — 6,0 балла, скорость прогрессирования — |
даемой группе больных были отмечены следующие по- |
2,5 балла в год. До включения в программу пациент в тече- |
бочные явления: 2 случая легкой гипербилирубинемии, |
ние полугода получал терапию копаксоном, на фоне кото- |
2 случая легкой анемии (уровень гемоглобина — не менее |
рой зафиксировано 2 обострения. |
100 г/л), 3 пациентки предъявляли жалобы на нарушения |
После введения 1-й дозы митоксантрона степень ин- |
менструального цикла, также зафиксированы 2 случая |
валидизации по шкале EDSS снизилась до 5,5, после 2-го |
алопеции, 2 случая экстрасистолии (включая описанный |
введения — до 5,0 баллов и оставалась на этом уровне до |
выше), а также эпизоды тахикардии (до 120 уд/мин) — у |
начала терапии копаксоном. Через 2 мес после 3-го введе- |
3 пациентов, 1 случай Herpes Zoster. |
ния митоксантрона у пациента было зафиксировано об- |
Использование митоксантрона в сочетании с копак- |
острение, выражавшееся в значительном ухудшении дви- |
соном при лечении ремиттирующего РС позволяет значи- |
гательных функций (двусторонняя поддержка при ходь- |
тельно уменьшить частоту обострений, в большом числе |
бе), в связи с чем в лечение были добавлены кортикосте- |
случаев добиться улучшения состояния больных. Исполь- |
роиды (метилпреднизолон 1000 мг в течение 3 дней), через |
зование сочетания препаратов также позволяет значи- |
2 нед обострение было купировано, пациент смог пере- |
тельно уменьшить необходимую курсовую дозу митоксан- |
двигаться без поддержки. Больной продолжал терапию |
трона (40 мг/м2) и увеличить длительность проведения |
копаксоном, на фоне которой было зарегистрировано по- |
терапии (практически неограниченно после перехода на |
вторное обострение (до 6,0 балла EDSS) через 1 мес после |
монотерапию копаксоном). |
4-го введения митоксантрона с усугублением пирамидных |
На основании проведенного исследования могут быть |
и мозжечковых нарушений, потребовавшее аналогичной |
сформулированы следующие выводы: 1) у большинства |
дополнительной терапии. В связи с очевидной неэффек- |
(77,8%) больных с агрессивным ремиттирующим РС на |
тивностью комбинированной терапии пациент, начиная с |
фоне комбинированной терапии митоксантроном в соче- |
5-го введения митоксантрона, был переведен на иммуно- |
тании с копаксоном отмечена стабилизация или улучше- |
супрессивную терапию митоксантроном в сочетании с |
ние состояния по шкале EDSS. Частота обострений умень- |
метилпреднизолоном. |
шилась с 1,3 до 0,5 в год; 2) комбинированную терапию |
В целом комбинированная терапия с использованием |
митоксантроном в сочетании с копаксоном больные пере- |
митоксантрона и копаксона является достаточно эффек- |
носят удовлетворительно. Тяжелых осложнений на фоне |
тивной в лечении РС с высокоактивным течением. Для |
лечения не отмечено. Ни у одного из пациентов терапия не |
оптимального подбора больных для комбинированной те- |
была прервана из-за развития побочных эффектов; в 1 слу- |
рапии следует учитывать некоторые особенности. Во- |
чае потребовалась коррекция дозы митоксантрона. |
ЛИТЕРАТУРА
1.Гусев Е.И., Демина Т.Л., Бойко А.Н. Рассеянный склероз 1997; 2. 10. Kkolou E., Toufexis J., Gaglia E., Pantzaris M. Clinical effect of Mitoxan-
2.Гусев Е.И., Бойко А.Н. Рассеянный склероз: от новых знаний к новым методам лечения. Рос мед журн 2001; 1: 5.
3.Гусев Е.И., Завалишин И.А., Бойко А.Н. Рассеянный склероз и другие демиелинизирующие заболевания. M 2004.
4.Малкова Н.А., Иерусалимский А.П. Рассеянный склероз 2006; 6: 123.
5.Сазонов Д.В., Малкова Н.А. Клиническая эффективность длительной иммуносупрессивной терапии быстро прогрессирующего рассеянного склероза. Сиб консилиум 2007; 6: 61: 41—45.
6.Шмидт Т.Е., Яхно Н.Н. Рассеянный склероз 2003; 7.
7.Calabresi P.A. et al. An open-label trial of combination therapy with interferon β-1a and oral methotrexate in MS. J Neurol 2002; 58: 314—317.
8.Gold R. Combination therapies in multiple sclerosis. J Neurol 2008; Suppl 1: 51—60.
9.Jeffery D.R. et al. A pilot trial of combination therapy with Mitoxantrone and interferon β-1b using monthly gadolinium-enhanced magnetic resonance imaging. Multiple Sclerosis 2005; 11: 573—582.
trone in patients with multiple sclerosis. Multiple Sclerosis 2006; 210.
11.Pulicken M. et al. Optimization of the safety and efficacy of interferon beta 1b and azathioprine combination therapy in multiple sclerosis. Multiple Sclerosis 2005; 11: 169—174.
12.Putzki N., Kumar M., Kreuzfelder E., Limmroth V. Mitoxantrone leads to a persistent selective decrease of the B cell count in patients with multiple sclerosis. Multiple Sclerosis 2006; 211—212.
13.Ramtahal J., Jacob A., Das K., Boggild M. Sequential maintenance treatment with glatiramer acetate after Mitoxantrone is safe and can limit exposure to immunosuppression in very active relapsing remitting multiple sclerosis. J Neurol 2006; 1—5.
14.Vollmer T., Panitch H., Bar-Or A. et al. Glatiramer acetate after induction therapy with Mitoxantrone in relapsing multiple sclerosis. Multiple Sclerosis 2008; 253: 1160—1164.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2009 |
79 |
