
Журнал неврологии и психиатрии / 2006 / NEV_2006_12_05
.pdf
ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
Высокая эффективность селективного внутриартериального тромболизиса при лечении ишемического инсульта у больных с окклюзией артерий крупного калибра
В.И. СКВОРЦОВА, Г.Н. ГОЛУХОВ, Ю.Д. ВОЛЫНСКИЙ, Л.В. ГУБСКИЙ, Н.А. ШАМАЛОВ, М.Г. КИРИЛЛОВ, Г.Р. РАМАЗАНОВ, П.В. ЯКИМОВИЧ, А.С. КИРЕЕВ
High efficacy of selective intra arterial thrombolysis in ischemic stroke patients with large-vessel occlusion
V.I. SKVORTSOVA, G.N. GOLUKHOV, YU.D. VOLYNSKY, L.V. GUBSKIY, N.A. SHAMALOV, M.G. KIRILLOV, G.R. RAMAZANOV, P.V. YAKIMOVITCH, A.S. KIREEV
Научно-исследовательский институт инсульта Российского государственного медицинского университета, Городская клиническая больница ¹31, Москва
Проведение селективной внутриартериальной (ВА) тромболитической терапии (ТЛТ) возможно в рамках более широкого терапевтического окна (до 6—8 ч от начала заболевания) под ангиографическим контролем и возможностью индивидуального дозирования дозы фибринолитика. В настоящей работе высокая эффективность селективной ВА ТЛТ продемонстрирована на двух клинических примерах. В первом случае больному 55 лет с окклюзией М1-сегмента правой средней мозговой артерии (СМА) и исходным баллом по шкале NIH 13 ВА ТЛТ была проведена через 7 ч от начала ИИ, что привело к полной реканализации сосуда через 40 мин и значительному клиническому улучшению (8 баллов по шкале NIH после ТЛТ). Во втором случае у больной 64 лет со стенозом С7-сегмента левой внутренней сонной артерии и окклюзией М12-сегмента левой СМА (20 баллов по шкале NIH) проведение ВА ТЛТ также способствовало восстановлению кровотока через 60 мин и драматическому восстановлению нарушенных функций (14 баллов по шкале NIH). Таким образом, приведенные примеры демонстрируют высокую эффективность ВА ТЛТ в лечении больных с ИИ.
Ключевые слова: ишемический инсульт, лечение инсульта, тромболизис, селективный внутриартериальный тромболизис.
Thrombolysis is the most effective treatment of acute ischemic stroke that increases the proportion of patients with good clinical outcome. Selective intra-arterial thrombolysis (IAT) can be used in a wider therapeutic window (up to 6— 8 hours) under the angiographic control with tailoring of fibrinolytic dose. The results of IAT by a recombinant plasminogen activator in 2 patients are presented. Patient 1, male, 55 years old, with M1 cerebral middle artery (CMA) occlusion and with NIHSS score 13 on admission was treated by IAT after 7 hours of stroke onset. Recanalization was observed 40 minutes after IAT started. The NIHSS score was 8 after IAT. Patient 2, female, 64 y.o., with NIHSS score 20 on admission and C7 internal carotid artery and M1 CMA occlusion was treated by IAT. Recanalization was observed 60 minute after the beginning of IAT, with NIHSS score being decreased to 14. These clinical cases demonstrate the high efficacy of intra arterial thrombolysis in ischemic stroke patients.
Key words: ischemic stroke, stroke management, thrombolysis, intra-arterial thrombolysis.
Нарастающая частота церебрального ишемического инсульта и его «омоложение», в конечном итоге приводящие к крайне неблагоприятным социальноэкономическим последствиям, заставляют пересмотреть традиционные методы лечения и реабилитации больных с этим тяжелым заболеванием [1].
Помимо успешно осваиваемых практическим здравоохранением высокотехнологичных методов диагностики (нейровизуализация — компьютерная и маг-
© Коллектив авторов, 2006
Zh Nevrol Psikhiatr Im SS Korsakova 2006;106:12:32—40
нитно-резонансная томография; транскраниальная допплерография), специалисты проявляют огромный интерес к возможностям активного воздействия на формирующийся или сформировавшийся тромб в артериях головного мозга.
Как показывает зарубежный опыт активного ле- чения ишемического инсульта, своевременное введение фибринолитиков, а именно рекомбинантного тканевого активатора плазминогена (rt-PA), оказалось весьма эффективным способом восстановления внутримозговой циркуляции [5]. Реперфузионная терапия применяется в двух модификациях: системный тромболизис, когда препарат вводится внутривенно в первые 3 ч от начала заболевания, и селективный внут-
32 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |

СИСТЕМНАЯ ТРОМБОЛИТИЧЕСКАЯ ТЕРАПИЯ ПРИ ИШЕМИЧЕСКОМ ИНСУЛЬТЕ
риартериальный тромболизис, при котором фибринолитик вводится в стенозированную (окклюзированную) артерию непосредственно в зоне локализации тромба. Такая методика применяется в тех случаях, когда системный тромболизис не дает эффекта или когда пациент поступает в стационар позднее первых 3 ч, но временной интервал от начала заболевания не превышает 6—8 ч.
Применительно к отечественной клинической практике необходимо сделать ряд уточнений и пояснений. Проведение системного внутривенного тромболизиса не нуждается в дополнительном оборудовании. Его эффективность определяется возможностью проведения КТ-исследования при поступлении больного, наличием препарата-тромболитика и выбором индивидуального оптимального режима инфузии с адекватным клиническим сопровождением.
Для выполнения прицельного селективного артериального тромболизиса необходимы специальное оборудование, инструментарий и, что самое главное, квалифицированные специалисты, владеющие устойчивыми навыками селективных рентгенохирургических исследований. В то же время методика селективного тромболизиса имеет ряд существенных преимуществ: во-первых, помогает уточнить локализацию окклюзии, ее характер, выяснить индивидуальные особенности мозговой циркуляции; во-вторых, значимо уменьшает дозу фибринолитического препарата и тем самым снижает риск геморрагических осложнений; в-третьих, предоставляет возможность для дополнительного механического воздействия на тромб, используя для этого микрокатетер или проводник; в-четвертых, может проводиться за пределами 3-часового временного окна и, наконец, наличие катетера в пораженной артерии позволяет с помощью дробной ангиографии контролировать процесс лизиса тромба и восстановления циркуляции. В настоящее время в мировой практике накоплен достаточно большой опыт использования различных фибринолитиков для проведения внутриартериальной тромболитической терапии (rt-PA, урокиназа, рекомбинантная проурокиназа) [2—4, 6—8].
Наиболее крупным рандомизированным контролируемым исследованием по изучению эффективности и безопасности внутриартериального тромболизиса является исследование PROACT II [4]. В данное испытание были включены 180 пациентов с документированной при помощи ангиографии окклюзией средней мозговой артерии (СМА), которым в тече- ние 2 ч внутриартериально вводили 9 мг проурокиназы или плацебо с небольшими дозами гепарина. В группе, получавшей проурокиназу, отмечалась высокая частота реканализации — до 66%, тогда как в группе плацебо — только в 18% случаев, что позволило значимо увеличить количество больных с хорошим функциональным восстановлением (40% в основной группе и 25% в группе плацебо). По показателю летальности достоверных различий между группами не отмечалось, хотя в группе, пролеченной проурокиназой, выявлялось большее количество симптомных внутримозговых кровоизлияний (10,9% по сравнению с 3,1% в группе плацебо).
В мета-анализе 27 исследований внутриартериальной ТЛТ [7] было продемонстрировано, что использование данного метода лечения приводило к достоверному улучшению степени функционального восстановления у большего количества пациентов (41,5% по сравнению с 23% в контрольной группе; р=0,002) и снижению уровня летальности (27,2% по сравнению с 33,1% в контрольной группе; р=0,004), несмотря на более высокую частоту развития симптомных внутричерепных кровоизлияний (9,5% по сравнению с 3% в контрольной группе). Таким образом, внутриартериальная ТЛТ является высокоэффективным методом лечения ишемического инсульта у наиболее тяжелого контингента больных с окклюзией мозговых артерий крупного калибра.
Впервые в Российской Федерации селективный внутриартериальный тромболизис был применен в клинике НИИ инсульта Российского государственного медицинского университета в 2006 г.
Сразу же после поступления в стационар больных, минуя приемное отделение, доставляли в кабинет компьютерной томографии (КТ), где невролог проводил общеклиническое обследование, оценивал неврологи- ческий статус, контролировал забор крови для самых необходимых лабораторных тестов, после чего осуществлялось экстренное КТ-исследование. За время проведения КТ у сопровождающих лиц уточняли анамнез заболевания и жизни больного. Такая последовательность действий позволяла, во-первых, сократить время от момента поступления больного до начала рентгенохирургического вмешательства и, во-вторых, установить предварительный диагноз и ориентировоч- ную локализацию сосудистого поражения.
Малоинвазивные хирургические вмешательства производили в рентгенооперационной, оснащенной цифровым ангиографическим комплексом Philips Integris Allura.
Первым этапом вмешательства была селективная церебральная артериография, которую выполняли, используя трансфеморальный доступ по Сельдингеру для последовательного проведения катетера 6F во внутреннюю сонную артерию. После получения надежного рентгеноконтрастного изображения тромбированного сосуда диагностический катетер с помощью длинного проводника заменяли на специальный гайд-катетер (проводник-катетер) T100CFS или 6F100 см (BALT). Через просвет гайд-катетера проводили микрокатетер Vasco14 или Vasco10+ (BALT), управление которым осуществляли гидрофильным микропроводником Sorcerer-009D или 012D (BALT).
Диагностическую ангиографию выполняли путем введения 7—8 мл рентгеноконтрастного препарата омнипак 240 со скоростью 4 мл/с. Для последующей контрольной ангиографии было достаточно введения 3—4 мл препарата. Наилучшей визуализации зоны тромбоза достигали путем съемки в боковой, переднезадней, трансорбитальной и подбородочно-маку- шечной проекциях.
Для селективного тромболизиса использовали препарат rt-PA (актилизе→, «Boehringer Ingelheim»), общее количество которого составляло до 20 мг.
После реканализации тромбированной артерии и восстановления кровотока производили контрольную
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |
33 |

ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
селективную ангиографию, катетер удаляли, гемостаз осуществляли прижатием по общепринятой методике.
Больных транспортировали в отделение интенсивной терапии инсульта и нейрореанимации, где продолжали лечение. Все проведенные вмешательства прошли без осложнений в ближайшем и последующем периодах наблюдения.
Высокую эффективность селективного внутриартериального тромболизиса при лечении больных с ишемическим инсультом вследствие окклюзии мозговых артерий крупного калибра можно продемонстрировать следующими клиническими наблюдениями.
Наблюдение 1.
Пациент К., 55 лет, поступил в отделение нейрореанимации 10.08.06 в 12 ч 07 мин. При поступлении предъявлял жалобы на отсутствие движений в левых конечностях, затруднение речи.
Анамнез заболевания: заболел утром 10.08.06 в 7 ч 15 мин, когда внезапно возникла слабость в левых конечностях и стала невнятной речь. Вызванной бригадой скорой помощи были зафиксированы артериальное давление (АД) 140/80 мм рт.ст., пароксизм мерцательной тахиаритмии. Госпитализирован в ГКБ ¹31.
Анамнез жизни: рос и развивался нормально, от сверстников в физическом и умственном развитии не отставал. Длительное время страдает артериальной гипертензией с максимальными цифрами АД 160/90 мм рт.ст., адаптирован к АД 130—140/80 мм рт.ст. Регулярно принимает каптоприл в дозе 12,5 мг 2 раза в день. В течение последних нескольких лет страдает пароксизмальной формой мерцательной аритмии. Сахарный диабет, язвенную болезнь желудка, инсульты, инфаркты в анамнезе отрицает. Аллергическими заболеваниями не болел. За границу в течение последнего года не выезжал, контакт с инфекционными больными в течение предшествующих 3 нед отрицает. Стул до заболевания был регулярным.
При осмотре: состояние тяжелое. Нормостенического телосложения, умеренного питания. Кожные покровы обыч- ной окраски и влажности. Дыхание самостоятельное, ритмичное, аускультативно везикулярное. Частота дыхательных движений (ЧДД) 21 в минуту. Тоны сердца приглушены, ритм правильный, частота сердечных сокращений (ЧСС) 80 в минуту, АД 140/80 мм рт.ст. Живот мягкий, безболезненный. Перистальтика выслушивается. Функции тазовых органов частично контролирует. Температура тела 36,6°С.
В неврологическом статусе: оглушен, в месте, во времени и в собственной личности ориентирован правильно, инструкции выполняет, быстро истощается. Дизартрия. Менингеальные знаки в виде скулового симптома Бехтерева и симптома Мондонези справа. Глазные щели S=D, зрачки S=D, прямая и содружественная фотореакции живые. Нистагма нет. Тенденция к повороту глаз вправо. Сглажена левая носогубная складка. Глоточные рефлексы D=S, живые, глотание сохранено. Язык девиирует влево. Левосторонняя гемиплегия с меняющимся тонусом в левых конечностях, с тенденцией к его повышению. Глубокие рефлексы S<D. Патологических стопных рефлексов нет. Левосторонняя болевая гемигипестезия. Суммарный балл по Шкале инсульта Национального института здоровья США — 13.
Коагулограмма при поступлении: АЧТВ 43 с; ПТИ 73,7%; МНО 1,09; фибриноген 280 мг/дл; тромбоциты 398 000. Гликемия 6,1 ммоль/л. Общий и биохимический анализы крови без особенностей.
При рентгеновской КТ головного мозга, выполненной через 4 ч 45 мин от начала заболевания (рис. 1, А), выявлялись ранние признаки инфаркта мозга в виде сглаженности контраста между серым и белым веществом в области лентикулярного и головки хвостатого ядер.
При проведении транскраниальной ультразвуковой допплерографии (ТКДГ) при поступлении выявлен гемодина-
À
Á
Â
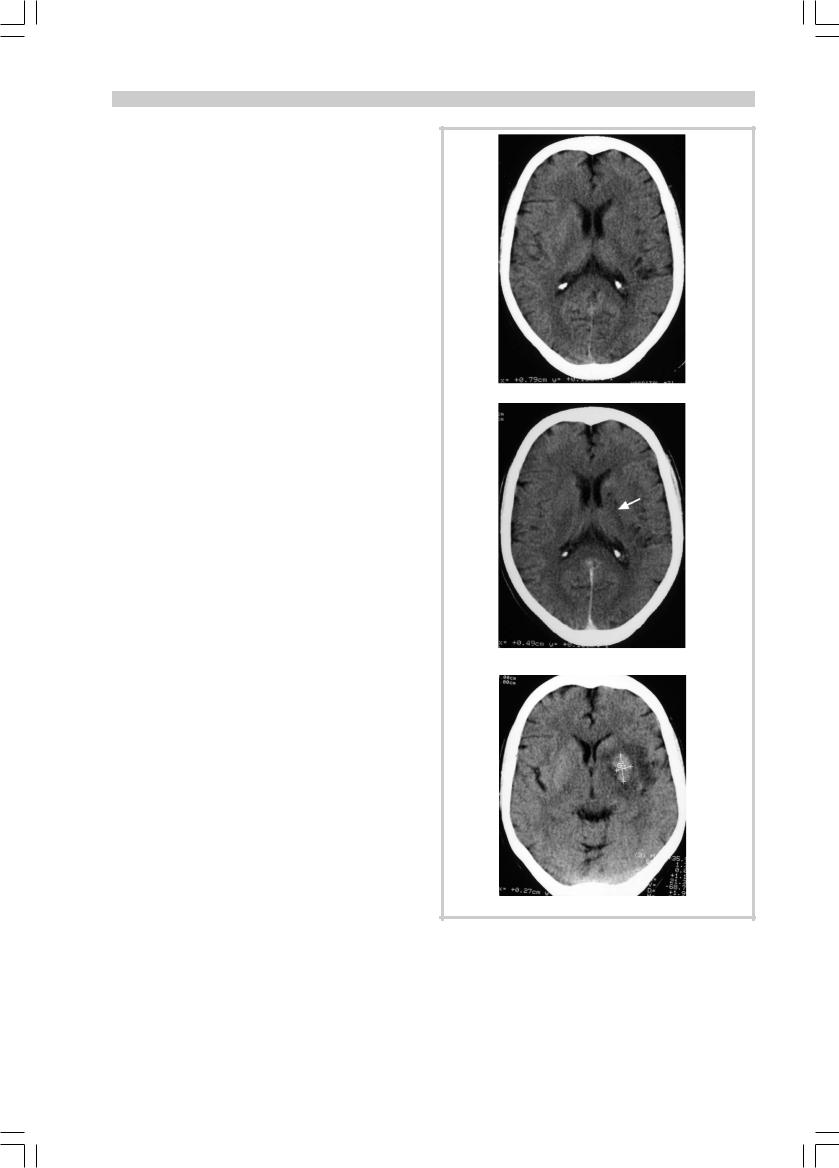
Рис. 1. Компьютерная томография головного мозга больного К.
А — при поступлении (4 ч 45 мин после начала заболевания). Контраст между серым и белым веществом в области лентикулярного ядра и головки хвостатого ядра правого полушария сглажен; Б — после проведения тромболитической терапии. Утрата ребристой структуры островка, сглаженность контраста между серым и белым веществом в области базальных ганглиев правого полушария. Гиперденсивный участок в области правого лентикулярного ядра соответствует участку геморрагического пропитывания (стрелка); В — 3-и сутки заболевания. Визуализируется область инфаркта мозга в правом полушарии с участком геморрагического пропитывания.
34 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |
СИСТЕМНАЯ ТРОМБОЛИТИЧЕСКАЯ ТЕРАПИЯ ПРИ ИШЕМИЧЕСКОМ ИНСУЛЬТЕ
мически значимый стеноз М1-сегмента правой СМА до 90% |
|
|
(рис. 2, А см. на цв. вклейке). |
|
|
Дуплексное сканирование магистральных артерий голо- |
|
|
вы (МАГ) выявило признаки начального атеросклероза ма- |
|
|
гистральных артерий головы (комплекс интима — медиа |
|
|
0,80—0,90 мм, норма — до 1,00 мм). Сонные артерии про- |
|
|
ходимы, обычного хода, кровоток симметричен, скорост- |
|
|
ные показатели в пределах нормы. |
|
|
Таким образом, учитывая данные анамнеза, клиниче- |
|
|
ской картины, результатов КТ, ТКДГ и дуплексного ска- |
|
|
нирования МАГ, больному был поставлен диагноз: ишеми- |
|
|
ческий кардиоэмболический инсульт в бассейне правой сред- |
|
|
ней мозговой артерии на фоне артериальной гипертензии, |
|
|
ИБС: пароксизмальной формы мерцательной аритмии. |
|
|
Учитывая поступление больного в клинику через 6 ч |
|
|
после развития инсульта, наличие у него выраженного нев- |
|
|
рологического дефицита (13 баллов по шкале NIH) и от- |
|
|
сутствие противопоказаний, была выполнена процедура |
|
|
селективной внутриартериальной тромболитической тера- |
|
|
ïèè. |
À |
|
Протокол селективного внутриартериального тромболи- |
||
|
||
зиса. При проведении селективной ангиографии обнаруже- |
|
|
на окклюзия М1-сегмента правой СМА с «культей», сво- |
|
|
бодным устьем и неоднородным контрастированием начала |
|
|
окклюзии без заполнения дистального русла правой СМА |
|
|
(рис. 3, А). Процедура селективного тромболизиса началась |
|
|
спустя 7 ч с момента развития ишемического инсульта (в 14 ч |
|
|
20 ìèí). |
|
|
Диагностический катетер по длинному проводнику был |
|
|
заменен проводниковым катетером, по которому система |
|
|
микрокатетер — микропроводник подведена в «культю» к |
|
|
месту окклюзии. Выполнены попытки частичной реканали- |
|
|
зации тромба (см. рис. 3, Б), однако завести микрокатетер |
|
|
по микропроводнику в тромботические массы не удалось. |
|
|
Перед местом окклюзии через микрокатетер внутриартери- |
|
|
ально болюсно введено 1 мг rt-PA с последующим введени- |
|
|
ем rt-PA через шприц-дозатор со скоростью 19 мг/ч. |
|
|
Через проводниковый катетер во время процедуры тром- |
|
|
болизиса каждые 15 мин выполняли контрольную ангио- |
|
|
графию. При первой контрольной ангиографии выражен- |
Á |
|
ных изменений сосудистого рисунка выявлено не было. Че- |
|
|
рез 30 мин от начала тромболизиса на контрольной ангио- |
|
|
грамме выявлялось заполнение всех сегментов правой СМА, |
|
|
кровоток ТIMI II. |
|
|
Через 40 мин от начала введения rt-PA у больного на- |
|
|
блюдался значительный регресс очагового неврологического |
|
|
дефицита в виде нарастания мышечной силы в левых ко- |
|
|
нечностях до 3 баллов в руке и 4 баллов в ноге. При выпол- |
|
|
нении контрольной ангиограммы определялся свободный |
|
|
кровоток по правой средней мозговой артерии (TIMI III), |
|
|
признаков дистальной эмболии не было (рис. 3, В). Введе- |
|
|
ние rt-PA было прекращено, через 15 мин был удален ин- |
|
|
тродьюссер, на место пункции наложена давящая повязка. |
|
|
Положительная клиническая динамика коррелировала |
|
|
с данными повторного ТКДГ-исследования, выполненного |
|
|
после процедуры тромболизиса, при котором был выявлен |
|
|
симметричный кровоток по обеим СМА (рис. 2,Б см. на цв. |
|
|
вклейке). При проведении повторной КТ выявлена бессим- |
|
|
птомная геморрагическая трансформация по типу пропи- |
|
|
тывания в области базальных ганглиев правого полушария |
 |
|
(см. рис. 1, Б). При исследовании показателей коагулограм- |
|
|
|
||
мы значимых изменений выявлено не было (АЧТВ 32 с, |
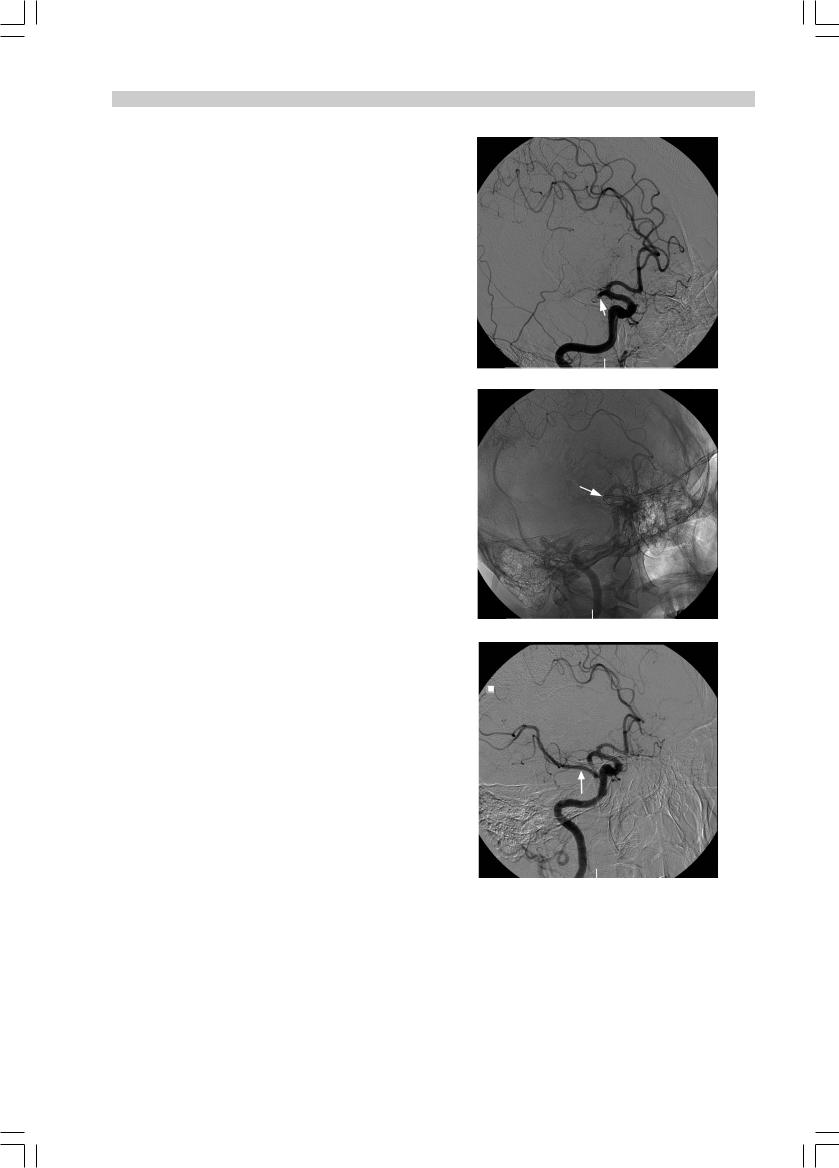
Рис. 3. Динамика ангиографического исследования в ходе |
|
ПТИ 83,8%, МНО 1,02, фибриноген 380 мг/дл). Восстанов- |
проведения селективного внутриартериального тромболизиса |
|
ление кровотока по правой СМА носило стабильный харак- |
у больного К. |
|
тер, признаков реокклюзии при повторных ТКДГ-исследо- |
А — диагностическая ангиография правой внутренней сонной арте- |
|
ваниях не выявлялось (рис. 2, В, Г см. на цв. вклейке). |
рии. Окклюзия М1-сегмента правой СМА с «культей» (стрелка) и |
|
К 3-м суткам от начала инсульта в неврологическом |
неоднородным контрастированием начала окклюзии без заполнения |
|
статусе отмечалось нарастание мышечной силы до 4,0 бал- |
дистального русла; Б — механическая реканализация микропровод- |
|
ником (стрелка) в области окклюзии М1-сегмента правой СМА; |
||
лов, полностью регрессировали тазовые расстройства, чув- |
||
В — контрольная ангиография через 40 мин от начала ТЛТ. Оконча- |
||
ствительные нарушения и гемианопсия, больной был спо- |
||
тельный результат внутриартериального тромболизиса — полное вос- |
||
собен к самостоятельному обслуживанию в пределах посте- |
||
становление кровотока по правой СМА (указана стрелкой). |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |
35 |
ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
ли. При КТ головного мозга визуализировался очаг инфаркта с небольшой зоной геморрагической трансформации (см. рис. 1, В).
В течение последующих двух дней отмечалось постепенное нарастание мышечной силы в конечностях до 4,5 баллов, что позволило пациенту передвигаться и обслуживать себя в пределах палаты уже к концу первой недели инсульта.
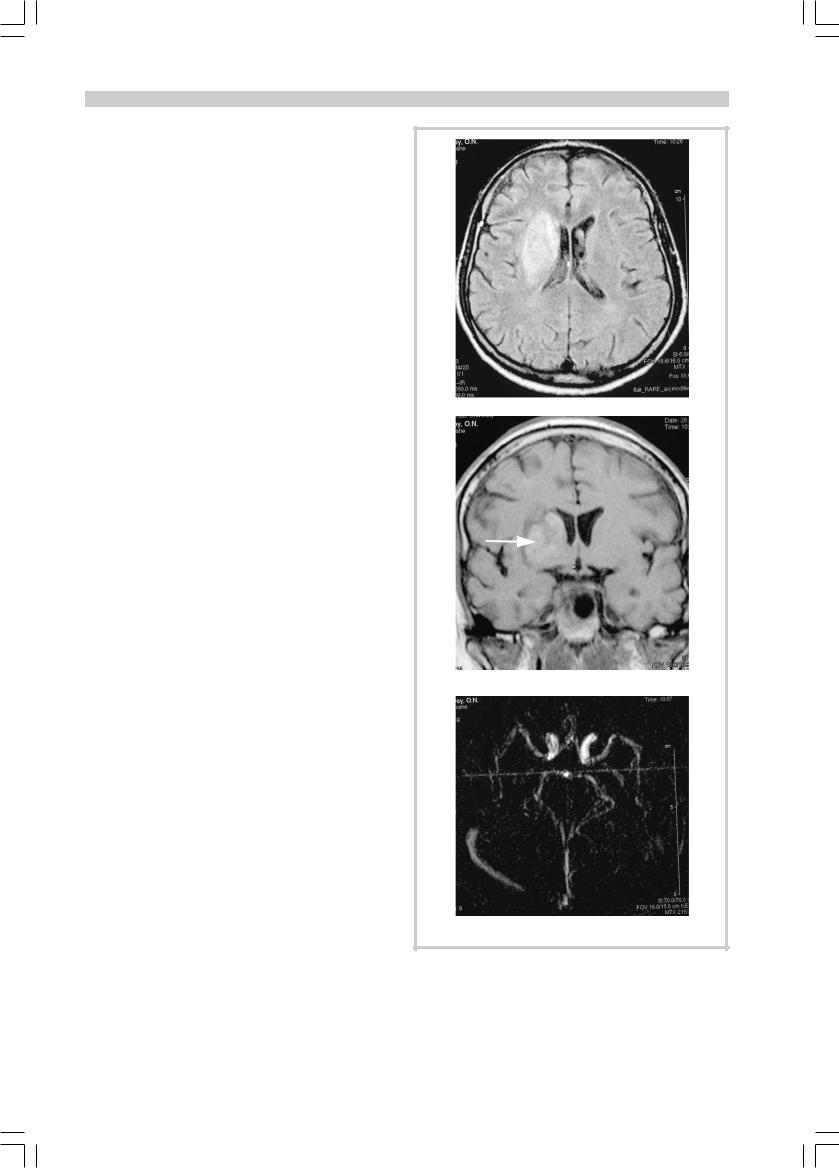
При магнитно-резонансной томографии (МРТ) на 16-е сутки инсульта подтверждено формирование инфаркта мозга с геморрагической трансформацией (рис. 4, А, Б), при проведении магнитно-резонансной (МР) ангиографии установлено полное восстановление кровотока по правой СМА (рис. 4, В).
На 28-е сутки заболевания в неврологическом статусе отмечался пронационный феномен в левой руке, больной полностью себя обслуживал (балл по модифицированной шкале Рэнкина 1). С целью вторичной профилактики инсульта пациент получал варфарин под контролем показателя МНО, ингибитор АПФ; были даны четкие рекомендации по модификации образа жизни.
Таким образом, после проведенного селективного внутриартериального тромболизиса у больного с окклюзией М1-сегмента правой СМА и исходно грубым неврологическим дефицитом отмечался драматический регресс очаговой неврологической симптоматики, что привело к полному функциональному восстановлению нарушенных неврологических функций и позволило больному быть полностью независимым в повседневной жизни.
Наблюдение 2.
Пациентка У., 64 лет, поступила в отделение нейрореанимации 17.08.06 в 21 ч 20 мин. Жалоб на момент осмотра не предъявляла из-за тотальной сенсомоторной афазии.
Анамнез заболевания (со слов сына пациентки). Заболела остро 17.08.06 в 19 ч 40 мин, когда внезапно возникла слабость в правых конечностях, перестала разговаривать и понимать обращенную речь.
Анамнез жизни: врожденный порок сердца (какой именно — родственники не помнят). Страдает постоянной мерцательной аритмией, принимает нерегулярно атенолол. В 2002 г. перенесла ишемический инсульт с правосторонним гемипарезом и речевыми нарушениями с хорошим восстановлением. До настоящего времени полностью обслуживала себя самостоятельно. Инвалид 2-й группы. Аллергических заболеваний не было. За границу в течение последнего года не выезжала и контакта с инфекционными больными в те- чение предшествующих 3 нед не было. Стул до заболевания был регулярным.
Объективно: состояние тяжелое. Нормостенического телосложения. Умеренно повышенного питания. Кожные покровы обычной окраски и влажности. Периферических отеков нет. Дыхание самостоятельное, ритмичное, аускультативно везикулярное, ослабленное в нижних отделах. Хрипы не выслушиваются, ЧДД 20 в минуту. Тоны сердца приглушены, ритм неправильный, ЧСС 65 в минуту, АД 134/71 мм рт.ст. Живот мягкий, на пальпацию не реагирует. Перистальтика выслушивается. Печень у края реберной дуги. Функции тазовых органов не контролирует. Температура тела 36,6°С.
Неврологический статус: уровень сознания — оглушение, беспокойна, речевые расстройства по типу тотальной сенсомоторной афазии, продуктивному контакту недоступна, инструкции не выполняет. Менингеальных симптомов нет. Глазные щели S=D, зрачки D≤S, прямая и содружественная фотореакции живые. Нистагма нет. Поворот головы и глазных яблок влево. Полушарный парез взора вправо. Глоточные рефлексы D=S, живые, глотание сохранено. Сглажена правая носогубная складка, язык не высовывает, в полости рта отклонен вправо. Правосторонняя гемиплегия с низким мышечным тонусом и низкими сухожильными реф-
36
À
Á
Â
Рис. 4. Результаты магнитно-резонансной томографии больного К., 16-е сутки заболевания.
А — FLAIR. Очаг инфаркта мозга в правом полушарии; Б — Т1взвешенное изображение. Стрелкой указана зона геморрагической трансформации очага поражения мозга; В — магнитно-резонансная ангиография. Полное восстановление кровотока по правой СМА.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006
СИСТЕМНАЯ ТРОМБОЛИТИЧЕСКАЯ ТЕРАПИЯ ПРИ ИШЕМИЧЕСКОМ ИНСУЛЬТЕ
лексами. Патологические стопные рефлексы справа. Суммарный балл по шкале NIH — 20.
Коагулограмма: АЧТВ 38 с; ПТИ 65,3%; МНО 1,16; фибриноген 746 мг/дл; тромбоциты 182 000. Гликемия 5,7 ммоль/л. Общий и биохимический анализы крови без особенностей.
При КТ головного мозга, выполненном через 1 ч 50 мин от начала инсульта (рис. 5, А), выявлялись ранние признаки инфаркта мозга в виде сглаженности контраста между серым и белым веществом в области лентикулярного и головки хвостатого ядер левого полушария, а также постинфарктная киста в задних отделах левой височной области.
Дуплексное сканирование МАГ выявило окклюзию правой (контралатеральной по отношению к очагу) внутренней сонной артерии (ВСА) выше бифуркации (рис. 6 см. на цв. вклейке), левая ВСА не изменена.
Таким образом, учитывая данные анамнеза, клиниче- ской картины, результатов КТ и дуплексного сканирования МАГ, больной был поставлен диагноз ишемического кардиоэмболического инсульта в бассейне левой средней мозговой артерии на фоне ИБС — постоянной формы мерцательной аритмии.
Учитывая поступление больной в клинику в течение периода терапевтического окна, наличие у нее выраженного неврологического дефицита (20 баллов по шкале NIH) и отсутствие противопоказаний, была выполнена процедура селективной внутриартериальной тромболитической терапии.
Протокол селективного внутриартериального тромболизиса. При проведении селективной ангиографии были выявлены эксцентрический неоднородный дефект заполнения (тромб) в С7-сегменте левой ВСА, стенозирующий просвет артерии на 80%, а также окклюзия устья левой СМА без заполнения дистального русла (рис. 7, А).
Вследствие обнаружения у больной отхождения левой общей сонной артерии под острым углом, диагностический катетер SIM 2 по длинному проводнику был заменен на проводниковый катетер, по которому система микрокатетер — микропроводник была подведена к участку стеноза в С7-сегменте ВСА. Выполнены попытки механической реканализации устья левой СМА, реканализовать которую не удалось — микропроводник заходил в передние хориоидальные ветви (см. рис. 7, Б).
Было принято решение о проведении тромболизиса в С7-сегменте левой ВСА (от момента развития заболевания прошло 5 ч 30 мин). Микрокатетер установлен в участок стеноза, болюсно внутриартериально через микрокатетер введен 1 мг rt-PA с последующим введением rt-PA через шприц-дозатор со скоростью 19 мл/ч. После болюсного введения rt-PA отмечалось нарастание мышечной силы в правых конечностях до 2 баллов, регрессировал полушарный поворот головы и глазных яблок.
Каждые 15 мин выполнялась контрольная ангиография. Через 30 мин после начала процедуры тромболизиса на контрольной ангиограмме выявилось уменьшение стеноза до 50% и ретроградное заполнение М4, М3, М2-сегментов левой СМА. Через 60 мин введение rt-PA было прекращено (суммарная доза rt-PA — 20 мг). На контрольной ангиограмме: остаточный стеноз менее 25%, по коллатералям из левой передней мозговой артерии (ПМА) ретроградно заполняются все сегменты левой СМА до устья (см. рис. 7, В, Г). Из бассейна левой ВСА через переднюю соединительную артерию хорошо контрастируются правые СМА и ПМА, дистальная эмболия не выявляется (см. рис. 7, Е). Инструмент удален. Через 15 мин удален интродьюссер, на место пункции наложена давящая повязка.
После окончания внутриартериального тромболизиса отмечался значительный регресс афатических нарушений (с тотальной сенсомоторной афазии до полного понимания обращенной речи и элементов моторной афазии), мышеч-
À
Á
Â
Рис. 5. Компьютерная томография головного мозга больной У.
А — при поступлении (1 ч 50 мин от начала заболевания). Контраст между серым и белым веществом в области лентикулярного ядра и головки хвостатого ядра левого полушария сглажен. Постинфарктная киста в задних отделах левой височной области; Б — после проведения тромболитической терапии. Умеренно гиподенсивная область в области базальных узлов левого полушария соответствует формирующемуся инфаркту мозга (стрелка); В — 6-е сутки заболевания. Визуализируется очаг инфаркта мозга с геморрагической трансформацией в левом полушарии.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |
37 |

ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
À |
Á |
 |
à |
Ä |
Å |
Рис. 7. Динамика ангиографического исследования в ходе проведения селективного внутриартериального тромболизиса у больной У.
А — диагностическая селективная ангиография. Эксцентрический неоднородный дефект заполнения (тромб) в С7-сегменте левой ВСА (стрелка), стенозирующий просвет сосуда на 80% и окклюзия устья левой СМА без заполнения дистального русла; Б — попытки механи- ческой реканализации устья левой СМА системой микрокатетер — микропроводник (стрелка); В — контрольная ангиография после выполнения тромболизиса. Остаточный стеноз в С7-сегменте левой ВСА менее 25% (стрелка); Г — по коллатералям из левой ПМА в капиллярную фазу ретроградно заполняются все сегменты левой СМА (стрелка) до устья; Д — суммация изображений серии контрольной ангиографии; Е — контрольная ангиография. Из бассейна левой ВСА через переднюю соединительную артерию (вертикальная стрелка) хорошо контрастируются правые СМА (горизонтальная стрелка) и ПМА.
38 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |
СИСТЕМНАЯ ТРОМБОЛИТИЧЕСКАЯ ТЕРАПИЯ ПРИ ИШЕМИЧЕСКОМ ИНСУЛЬТЕ
ная сила в правых конечностях наросла до 3 баллов, полностью регрессировал поворот головы и глазных яблок.
При проведении повторной КТ непосредственно после тромболизиса выявлены признаки формирующегося инфаркта мозга (см. рис. 5, Б).
В последующие 2 дня отмечалось нарастание мышеч- ной силы в правых конечностях до 4,5 баллов в руке и 4 баллов в ноге, пациентка стала способна к самообслуживанию в пределах палаты. КТ-исследование на 6-е сутки заболевания выявило геморрагическую трансформацию по типу пропитывания в области базальных ганглиев левого полушария (см. рис. 5, В).
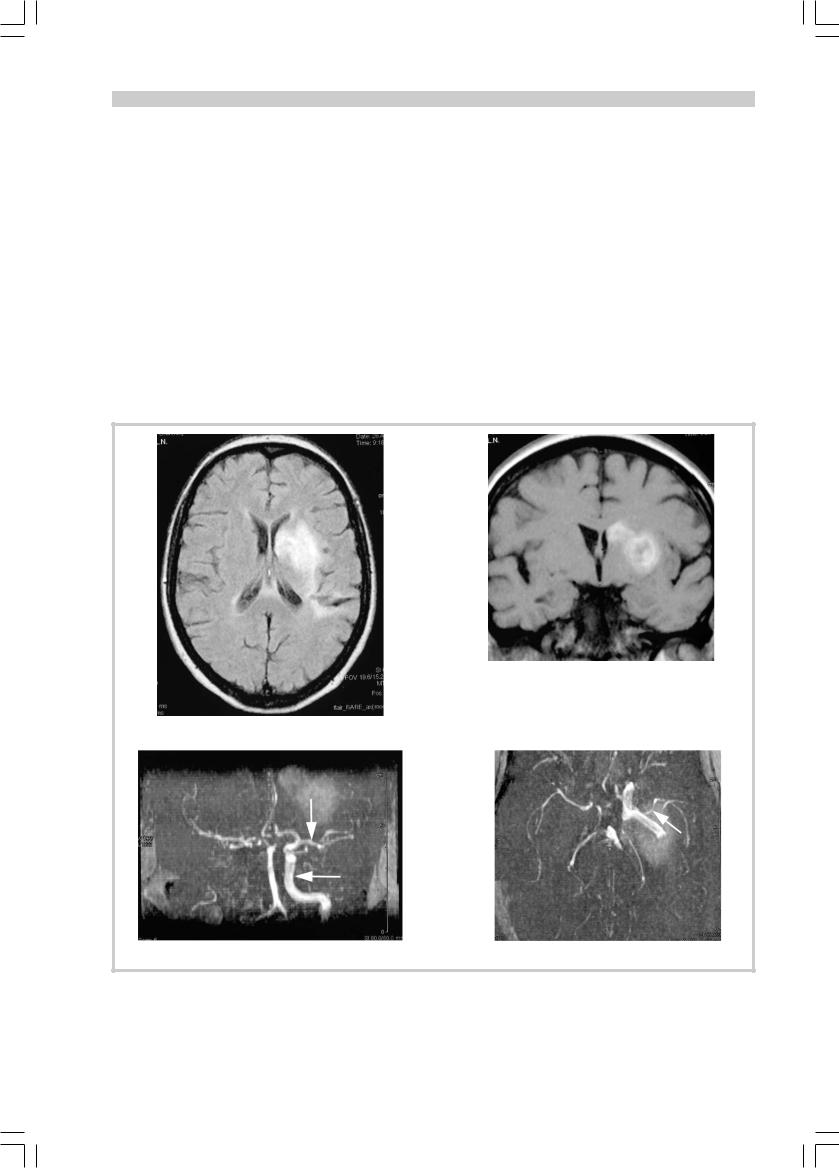
При МРТ-исследовании на 9-е сутки заболевания визуализировался инфаркт мозга в левой теменно-височной области с признаками геморрагической трансформации по типу пропитывания (рис. 8, А, Б). На МР-ангиограммах было подтверждено восстановление кровотока по левой СМА, выявлялись признаки окклюзии правой (контралатеральной) ВСА (см. рис. 8, В, Г).
На 21-е сутки заболевания в неврологическом статусе отмечался парез в правой руке со снижением мышечной
силы до 4,5 баллов, сохранялись элементы моторной афазии, больная полностью себя обслуживала (балл по модифицированной шкале Рэнкина 2). С целью вторичной профилактики инсульта был назначен варфарин под контролем показателя МНО, ингибитор АПФ; даны четкие рекомендации по модификации образа жизни.
С учетом данных, полученных при дуплексном исследовании МАГ и МР-ангиографии (окклюзия правой ВСА на всем протяжении), можно предположить, что до развития настоящего инсульта у больной в течение длительного времени сформировался тромбоз правой ВСА. Кровоснабжение правого полушария осуществлялось за счет перетока крови из левого полушария через переднюю соединительную артерию.
При окклюзии М1-сегмента левой СМА и стенозе С7-сегмента ВСА, которые привели к развитию клинической симптоматики, начало страдать также и кровоснабжение бассейна правой СМА. После про-
Á
À
 |
à |
Рис. 8. Результаты магнитно-резонансной томографии больной У., 9-е сутки заболевания.
А — FLAIR. Очаг инфаркта мозга в левом полушарии головного мозга; Б — Т1-ВИ. Геморрагическая трансформация по типу пропитывания в левом полушарии головного мозга; В — МР-ангиография. Вертикальной стрелкой указана левая СМА, горизонтальной — сифон ВСА. Отсутствие кровотока в сифоне контралатеральной правой ВСА; Г — МР-ангиография. Стрелкой указан М1-сегмент левой СМА с признаками остаточного стеноза.
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |
39 |

ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
веденного селективного внутриартериального тромболизиса произошло не только восстановление кровотока в левой СМА (ретроградно через коллатерали между СМА и ПМА), но и в бассейнах правых ПМА и СМА, т.е. восстановилось кровоснабжение правого полушария, которое было до развития настоящего заболевания. Таким образом, проведение селективного тромболизиса у пациентки с исходно тяжелым неврологическим дефицитом привело к быстрому регрессу очаговой неврологической симптоматики и полному функциональному восстановлению нарушенных неврологических функций.
Заключение
Приведенные клинические примеры селективного внутриартериального тромболизиса демонстрируют очевидные преимущества данного метода лечения ишемического инсульта: возможность лизиса тромба в более широком терапевтическом окне по сравнению с системным внутривенным тромболизисом; возможность индивидуального дозирования фибринолитического препарата путем выполнения контрольных ангиограмм, что снижает риск симптомных геморрагических осложнений.
По нашим и литературным данным, локальное внутриартериальное введение фибринолитика, как правило, сопровождается развитием геморрагического пропитывания в ишемизированную зону мозга [3]. Наши сопоставительные исследования свидетельствуют о появлении первых признаков пердиапедезного пропитывания в очаге церебральной ишемии че- рез 10—15 мин после первых признаков реканализации окклюзированного сосуда с восстановлением кровотока. Важно отметить, что мгновенное прекра-
щение инфузии тромболитика после появления первых признаков реканализации артерии крупного калибра (терминальный отдел внутренней сонной артерии, М1-сегмент средней мозговой артерии, основная артерия), как правило, приводит к формированию реокклюзии и делает всю процедуру селективного тромболизиса неэффективной. Наши наблюдения показывают, что первые признаки диапедезной геморрагической трансформации не только не сопровождаются ухудшением неврологического статуса больного, но и являются индикатором достаточной и эффективной дозы введенного препарата. По-види- мому, 10—15-минутный период «постреканализационной» инфузии тромболитика необходим для закрепления эффекта тромболитической терапии и профилактики реокклюзии артерии.
Таким образом, внедрение новых технологий реперфузионной терапии в нашей стране будет способствовать дальнейшему совершенствованию системы оказания медицинской помощи больным с инсультом и позволит не только снизить показатели смертности и инвалидности от этого заболевания, но и с учетом его медицинской и социальной значимости достоверно повысить уровень здоровья и качества жизни населения Российской Федерации. Для возможного внедрения метода селективного внутриартериального тромболизиса в регионах страны необходимо обеспечение головных региональных центров цереброваскулярной патологии и инсульта не только круглосуточной службой нейровизуализации, лабораторного и, желательно, ультразвукового сосудистого (транскраниальная допплерография) контроля, но и ангиографической операционной, укомплектованной высококвалифицированными подготовленными кадрами рентгенохирургов.
ЛИТЕРАТУРА
1.Гусев Е.И., Скворцова В.И., Киликовский В.В. и др. Проблема инсульта в Российской Федерации. Качество жизни 2006; 2: 13: 10—14.
2.Arnold M., Schroth G., Nedeltchev K. et al. Intra-arterial thrombolysis in 100 patients with acute stroke due to middle cerebral artery occlusion. Stroke 2002; 33: 1828—1833.
3.Arnold M., Nedeltchev K., Mattle H.P. et al. Intra-arterial thrombolysis in 24 consecutive patients with internal carotid artery T-occlu- sions. J Neurol Neurosurg Psychiat 2003; 74: 739—742.
4.del Zoppo G.J., Higashida R.T., Furlan A.J. et al. PROACT: A Phase II Randomized Trial of Recombinant Pro-Urokinase by Direct Arterial Delivery in Acute Middle Cerebral Artery Stroke. Stroke 1998; 29: 4—11.
5.European Stroke Initiative Recommendations for stroke Manage- ment—Update 2003. Cerebrovasc Dis 2003; 16: 311—337.
6.Lee D.H., Jo K.D., Kim H.G. et al. Local intraarterial urokinase thrombolysis of acute ischemic stroke with or without intravenous abciximab: a pilot study. J Vasc Interv Radiol 2002; 13: 769—774.
7.Lisboa C. et al. Analysis of the Safety and Efficacy of Intra-Arterial Thrombolytic Therapy in Ischemic Stroke. Stroke 2002; 33: 2866.
8.Théron J., Coskun O., Huet H. et al. Local intraarterial thrombolysis in the carotid territory. Interventional Neuroradiology 1996; 2: 111— 126.
9.Zeumer H., Freitag H.J., Zanella F. et al. Local intra-arterial fibrinolytic therapy in patients with stroke: urokinase versus recombinant tissue plasminogen activator (rt-PA). Neuroradiology 1993; 35: 159— 162.
Поступила 14.09.06
40 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2006 |
