
Журнал неврологии и психиатрии / 2007 / NEV_2007_11_09
.pdf
Дофаминергическая терапия когнитивных нарушений
В.В. ЗАХАРОВ
Dophaminergic therapy of cognitive disturbances
V.V. ZAKHAROV
Кафедра нервных болезней Московской медицинской академии им. И.М. Сеченова
Одной из наиболее хорошо зарекомендовавших себя стратегий терапии когнитивных нарушений является воздействие на церебральные нейротрасмиттерные системы. Применение ацетилхолинергических
èглютаматергических препаратов является в настоящее время «золотым стандартом» лечения наиболее распространенных форм деменции [1—4, 8, 20, 22], хотя применение первых на стадии умеренных когнитивных нарушений пока дало противоречивые результаты [19—21]. Предполагают, что развитие ацетилхолинергической недостаточности является относительно поздним событием в патогенезе когнитивных расстройств и менее тяжелые нарушения в большей степени обусловлены дисфункцией со стороны других нейротрансмиттерных систем — дофаминергической, норадренергической, серотонинергической
èäð.
Âсвязи с этим весьма интересны результаты исследований L. Bäckman и соавт., N. Volkow и соавт. [15, 30]. В цитируемых работах было показано, что в пожилом возрасте закономерно развивается легкая дофаминергическая недостаточность, о чем свидетельствует уменьшение биодоступности D2-рецепторов полосатых тел (по данным позитронно-эмиссионной томографии головного мозга). При этом прослеживается корреляция между указанными нейрохимическими изменениями и выраженностью когнитивных нарушений лобного типа, которые являются одним из основных и наиболее ранних признаков хронической сосудистой мозговой недостаточности [2, 4, 7, 12].
Âоснове данной корреляции вероятно лежит недостаточность дофаминергической активации лобных долей со стороны вентральной зоны покрышки среднего мозга (так называемый мезокортикальный дофаминергический путь).
К настоящему времени накоплен значительный клинический опыт применения дофаминергических препаратов при возрастной когнитивной дисфункции. Наиболее изученным препаратом является пирибедил, или проноран (фирма «Сервье»). Он совмещает свойства агониста дофаминовых D2/D3-рецепторов
© В.В. Захаров, 2007
Zh Nevrol Psikhiatr Im SS Korsakova 2007;107:11:45—48
èблокатора пресинаптических α2-адренорецепторов. Применение пронорана способствует усилению не только дофаминергической, но и норадренергической медиации, что весьма выгодно с клинической точки зрения, так как активация норадренергической системы играет одну из ключевых ролей в процессе запоминания новой информации. Кроме того, по экспериментальным данным проноран обладает также положительным вазоактивным эффектом в отношении церебрального и периферического кровообращения, что также является преимуществом при использовании данного препарата у пациентов с хрониче- ской сосудистой мозговой недостаточностью [5, 6, 14, 15, 24, 27, 28].
Â70—80-õ годах ХХ века в европейских странах проводилась серия плацебо-контролируемых клини- ческих испытаний, в которых был показан положительный ноотропный эффект пронорана у пациентов с возрастной когнитивной дисфункцией, не достигающей выраженности деменции [14, 15, 27, 28]. При этом, по некоторым данным, эффективность пронорана превосходила эффективность монотерапии сосудистыми препаратами [28]. В 2001 г. эти результаты были воспроизведены в работе D. Nagaraia и соавт. [25], которые применяли проноран у пациентов с синдромом умеренных когнитивных нарушений. Было показано, что применение пронорана сопровождалось достоверно бóльшим процентом улучшений когнитивных функций по Краткой шкале оценки психического статуса по сравнению с плацебо. Известно также, что на ранних стадиях болезни Паркинсона использование пронорана сопровождается не только улуч- шением двигательных, но и когнитивных функций [10].
Согласно требованиям доказательной медицины, проведение двойных слепых плацебо-контролируемых рандомизированных исследований является основным
èабсолютно необходимым методом оценки эффективности ноотропных препаратов. Однако этот метод также имеет определенные ограничения, которые препятствуют «механическому» перенесению полученных результатов на повседневную клиническую практику. Как известно, отбор пациентов при проведении клинических исследований проводится по определенным критериям, которые, как правило, значительно ограничивают число сопутствующих заболеваний и
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 11, 2007 |
45 |

ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
применение прочих препаратов. Также не всегда просто интерпретировать практическое значение полу- ченных в ходе рандомизированных исследований изменений психометрических шкал. В связи с этим целесообразен дополнительный анализ результатов применения того или иного препарата в условиях обычной клинической практики. При этом наряду с психометрическими [например «Краткой шкалой оценки психического состояния» (Mini-mental scale examination — MMSE)] используются шкалы типа шкалы «Общего клинического впечатления» (Clinical Global Impression — CGI). Последние предоставляют лечащему врачу значительную свободу в оценке практического значения проводимой терапии на основании всей совокупности изменений клинического статуса пациента. Применение таких шкал является общепринятым в мировой практике и настоятельно рекомендуется [23, 26] для применения в области когнитивной неврологии.
В 2005—2007 г. в России в рамках программы «Прометей» (координатор проекта — акад. РАМН Н.Н. Яхно) был проанализирован опыт применения пронорана в терапии возрастной когнитивной дисфункции в повседневной клинической практике. Результаты выполнения этой программы были опубликованы в целом ряде статей [6, 9, 14].
Данная публикация отражает раздел указанной программы, целью которого была оценка влияния препарата проноран на возрастные когнитивные нарушения при определении их выраженности разными методами. В этом случае сопоставляли данные психометрических шкал (MMSE) [18] и нейропсихологиче- ских тестов (тест рисования часов) [23], с одной стороны, и клинической шкалы (CGI) [27], с другой.
легкими или умеренными когнитивными нарушениями. Данные пациенты наблюдались в поликлиниках 54 городов из 37 регионов России. В лечении и наблюдении за пациентами приняли участие 212 вра- чей-неврологов амбулаторного звена.
В этой группе проноран пациентам назначали в дозе 50 мг в сутки в 1 прием в течение 3 мес. Монотерапия этим препаратом проводилась 1181 пациенту, а 875 получали проноран в сочетании с другими сосудистыми и метаболическими средствами.
Оценка эффективности терапии в этих случаях также проводилась на 6-й и на 12-й неделе лечения. Различий по возрасту, полу и выраженности когнитивных расстройств между пациентами, получавшими мототерапию пронораном и политерапию в обеих группах не было.
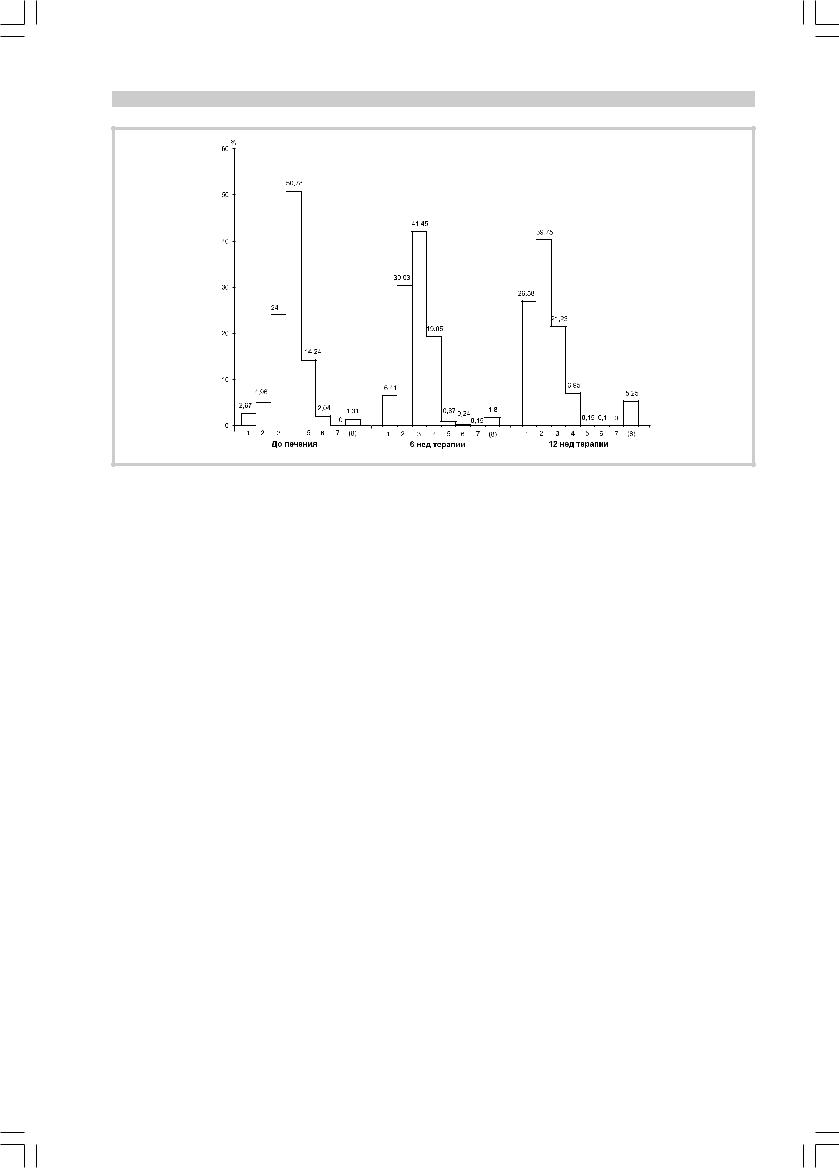
По CGI лечащий врач до начала терапии, и далее на 6-й и 12-й дни оценивал общее состояние пациента на основании всей совокупности имеющейся симптоматики по 7-балльной шкале оценке «нет нарушений» соответствовал 1 балл, «незначительные» — 2, «легкие» — 3, «умеренные» — 4, «умеренно тяжелые» — 5, «тяжелые» — 6, «крайне тяжелые нарушения» — 7 (эти баллы далее см. на рисунке).
Кроме того, отмечалась степень влияния соответствующих нарушений на повседневную жизнь больных.
Как в 1-й, так и во 2-й частях исследования в анализ не включались пациенты в остром периоде инсульта, черепно-мозговой травмы, после оперативного вмешательства, с болезнью Паркинсона и синдромом паркинсонизма, с шизофренией, а также пациенты с тяжелыми речевыми, двигательными и чувствительными расстройствами.
Материал и методы |
Результаты и обсуждение |
В соответствии с указанной целью исследование |
На фоне терапии пронораном было отмечено дос- |
было разделено на 2 части. В 1-й части для оценки |
товерное улучшение когнитивных функций. Так, сред- |
эффективности терапии использовались психометри- |
ний результат по MMSE повысился с 26,0±1,0 до |
ческие (MMSE) и нейропсихологические тесты, а во |
лечения до 27,9±3,5 балла на 12-й неделе лечения |
2-й части — шкала CGI. |
(р<0,05) (см. рисунок). |
В 1-й части был проведен анализ лечения 574 |
На фоне проводимой терапии достоверно умень- |
пациентов в возрасте от 60 до 89 лет (в среднем |
шилась также доля пациентов, допустивших сущест- |
69,5±5,5 года) с легкими или умеренными когнитив- |
венные ошибки в тесте рисования часов. До лечения |
ными нарушениями возрастного и/или сосудистого |
такие ошибки выявлялись у 48,6% пациентов, после |
характера. Эти пациенты наблюдались в поликлини- |
лечения (на 12-й неделе) — лишь у 14,3% (р<0,0001). |
ках 33 городов из 30 регионов России. Наиболее час- |
При этом не было зафиксировано достоверных раз- |
тым клиническим диагнозом была дисциркуляторная |
личий соответствующих показателей между группа- |
энцефалопатия I или II стадии. В лечении и наблюде- |
ми, получавшими монотерапию пронораном и ком- |
нии за пациентами приняли участие 132 врача-нев- |
бинированную терапию (более подробные данные по |
ролога амбулаторного звена. |
этим группам были опубликованы ранее [9]). |
Проноран назначали в дозе 50 мг в сутки в 1 прием |
Улучшение когнитивного функционирования |
в течение 3 мес. Монотерапия данным препаратом |
больных было отмечено и по шкале CGI. Если до ле- |
проводилась 385 пациентам, а 189 пациентов получа- |
чения выраженность нарушений по данной шкале у |
ли проноран в сочетании с другими сосудистыми и |
большинства пациентов варьировала от легкой до |
метаболическими средствами. Оценка эффективности |
умеренно тяжелой (3—5 баллов), то после лечения |
терапии проводилась на 6-й и на 12-й неделе лече- |
это были или умеренные либо незначительные (2—4 |
íèÿ. |
балла) расстройства. Отсутствие динамики зафикси- |
Во 2-й части был проведен анализ лечения 2058 |
ровано у 170 пациентов, а отрицательная — только у |
пациентов (1447 женщин и 611 мужчин в возрасте от |
6. Распределение больных в соответствии с показате- |
50 до 94 лет, в среднем 64,9±8,3 года) с диагнозом |
лями шкалы CGI до лечения, на 6-й и 12-й неделе |
дисциркуляторная энцефалопатия I или II стадии и |
терапии приведено на рисунке. |
46 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 11, 2007 |
ТЕРАПИЯ КОГНИТИВНЫХ НАРУШЕНИЙ |
Распределение больных (в %) по показателям шкалы CGI до лечения, на 6-й и 12-й неделе терапии. |
По оси ординат — процент больных, по оси абсцисс — баллы (1—7); (8) — нет данных. |
Терапия пронораном характеризовалась удовле- |
ние, ибо на сегодняшний день отсутствует единый |
творительным профилем безопасности и переноси- |
протокол ведения пациентов с когнитивными рас- |
мости. Нежелательные явления отмечались у 15,4% |
стройствами, не достигающими стадии деменции [7, |
пациентов. Наиболее распространенными из них были |
9, 11, 12, 20], хотя распространенность недемент- |
тошнота, головокружение, рвота, головная боль, |
ных нарушений в пожилом возрасте значительно пре- |
повышенная сонливость, боли или дискомфорт в |
вышает частоту деменции [6, 16, 18]. При этом они, |
эпигастрии, диспепсия, общая слабость. Данные яв- |
снижая качество жизни не только пациентов и их бли- |
ления не угрожали жизни пациентов, не наносили |
жайших родственников, приносят социально-эконо- |
непоправимого вреда здоровью и крайне редко (ме- |
мический ущерб обществу в целом. Поэтому раннее |
нее 1% случаев) вынуждали прекратить проводимую |
начало лечения когнитивных нарушений имеет боль- |
терапию. Несколько чаще нежелательные явления от- |
шое значение и для профилактики деменции, так как |
мечались у пациентов, получавших комбинирован- |
пациенты с умеренными когнитивными нарушения- |
ную терапию, по сравнению с получавшими моноте- |
ми, представляют собой группу высокого риска ее |
рапию пронораном (15 и 22% соответственно). |
развития в будущем (так, заболеваемость болезнью |
Таким образом, опыт практического применения |
Альцгеймера в данной категории пациентов состав- |
пронорана в условиях повседневной амбулаторной |
ëÿåò 10—15% â ãîä [25]). |
неврологической практики согласуется с результата- |
Из изложенного видно, что дофаминергическая |
ми опубликованных ранее плацебо-контролируемых |
терапия может проводиться как самостоятельный вид |
рандомизированных клинических исследований. |
лечения недементных когнитивных нарушений, так |
Применение пронорана у пациентов с хрониче- |
и в комплексе с традиционными сосудистыми и ноо- |
ской сосудистой мозговой недостаточностью способ- |
тропными препаратами. Важно, что проноран может |
ствует регрессу выраженности когнитивных наруше- |
сочетаться с другими ноотропными и сосудистыми |
ний. При этом улучшение когнитивных функций фик- |
препаратами, поскольку такое сочетание не приво- |
сируется не только с помощью психометрических, но |
дит к увеличению частоты побочных эффектов. Вме- |
общих клинических шкал. Данный факт свидетельст- |
сте с тем следует обратить внимание на то, что в на- |
вует о практической значимости выявленного когни- |
шей работе не было получено различий по величине |
тивного улучшения, которое, по нашим наблюдени- |
ноотропного эффекта между монотерапией пронора- |
ям, оказывает ощутимое положительное влияние на |
ном и комбинацией данного препарата с другими |
повседневную жизнь пациента, его поведение и са- |
сосудистыми и ноотропными лекарственными сред- |
мочувствие. |
ствами. Это дает нам основание сделать вывод, что |
Сказанное дает основание утверждать, что тера- |
указанная комбинированная терапия не имеет в дан- |
пия пронораном показана для лечения пациентов с |
ном случае особых преимуществ в отношении кор- |
недементными (легкими или умеренными) когнитив- |
рекции когнитивных расстройств по сравнению с |
ными нарушениями. Это имеет практическое значе- |
монотерапией пронораном. |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 11, 2007 |
47 |

ЛЕЧЕНИЕ НЕРВНЫХ И ПСИХИЧЕСКИХ ЗАБОЛЕВАНИЙ
Таким образом, проноран оказывает положительный ноотропный эффект при недементных (легких и умеренных) когнитивных нарушениях сосудистой этиологии. Данный эффект не фиксируется с помощью различных методов оценки нейропсихологиче- ских тестов и клинически ориентированных шкал, позволяющих оценить состояние больных в целом.
Эффективность в отношении когнитивных расстройств и удовлетворительный профиль переносимости и безопасности у пациентов пожилого возраста позволяет рекомендовать проноран для широкого клинического применения при дисциркуляторной энцефалопатии I и II стадии.
ЛИТЕРАТУРА
1.Гаврилова С.И. Фармакотерапия болезни Альцгеймера. М: Пульс 2003; 115.
2.Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. Под ред. Н.Н. Яхно. М 2002; 85.
3.Дамулин И.В., Преображенская И.С., Мхитарян Э.А. Влияние мемантина на когнитивные функции у пациентов с болезнью Альцгеймера, смешанной альцгеймеровско-сосудистой деменцией и деменцией с тельцами Леви. Неврол журн (приложение
1)2005;11:37—41.
4.Захаров В.В., Яхно Н.Н. Нарушения памяти. М: ГеотарМед 2003;150.
5.Захаров В.В., Локшина А.Б. Применение препарата проноран (пирибедил) при легких когнитивных расстройствах у пожилых больных с дисциркуляторной энцефалопатией. Неврол журн 2004;2:30—35.
6.Захаров В.В. Всероссийская программа исследований эпидемиологии и терапии когнитивных расстройств в пожилом возрасте («Прометей»). Неврол журн 2006;11:27—32.
7.Локшина А.Б. Захаров В.В. Легкие и умеренные когнитивные нарушения при дисциркуляторной энцефалопатии. Неврол журн (приложение 1) 2005;11:57—63.
8.Преображенская И.С. Экселон в терапии нейродегенеративных деменций. Неврол журн (приложение 1) 2005;11:42—46.
9.Преображенская И.С., Яхно Н.Н. Возрастная когнитивная дисфункция: диагностика и лечение. Журн неврол и психиат 2006;106:11:33—38.
10.Яхно Н.Н., Захаров В.В. Легкие когнитивные нарушения в пожилом возрасте. Неврол журн 2004;1:4—8.
11.Яхно Н.Н., Преображенская И.С. Проноран в лечении больных с ранними стадиями болезни Паркинсона. Неврол журн 2004;9:6:34—38.
12.Яхно Н.Н. Когнитивные расстройства в неврологической клинике. Неврол журн (приложение 1) 2005;11:4—12.
13.Яхно Н.Н., Локшина А.Б., Захаров В.В. Легкие и умеренные когнитивные расстройства при дисциркуляторной энцефалопатии. Клин геронтол 2005;11:38—39.
14.Яхно Н.Н., Захаров В.В., Локшина А.Б. Нарушение памяти и внимания в пожилом возрасте. Журн неврол и психиат 2006;106:2: 58—62.
15.Bäckman L., Ginovart N., Dixon R. et al. Age-related cognitive deficits mediated by changes in the striatal dopamine system. Am J Psychiat 2000;157:635—637.
16.Bille J., Bukiwsky J.V., De Ferron A. et al. Decline cerebral et therapeutique: une etude clinique multicenrique de Trivastal 50 retard en Neuro-Geriatrie. Psych Med 1986;18:609—626.
17.DiCarlo A., Baldereschi M., Amaducci L. et al. Cognitive impairment without dementia in older people: prevalence, vascular risk factors, impact on disability. The Italian Longitudinal Study on Aging. J Am Ger Soc 2000;48:775—782.
18.Folstein M.F., Folstein S.E., McHugh P.R. Mini-Mental State: a practical guidefor grading the mental state of patients for the clinician. J Psych Res 1975;12:189—198.
19.Graham J.E., Rockwood K., Beattie E.L. et al Prevalence and severity of cognitive impairment with and without dementia in an elderly population. Lancet 1997;349:1793—1796.
20.Jelic V., Kivipelto M., Winblad B. Clinical trials in mild cognitive impairment: lessons for the future. J Neurol Neurosurg Psychiat 2006;77:7:892.
21.Knopman D.S. Current treatment of mild cognitive impairment and Alzheimer’s disease. Curr Neurol Nerosci Rep 2006;6:5:365—371.
22.Kurshner H.S. Mild cognitive impairment: to treat or not to treat? Curr Neurol Neurosci Rep 2005;5:6:455—457.
23.Lovenstone S., Gauthier S. Management of dementia. London: Martin Dunitz 2001.
24.McLendon B.M., Doraiswang P.M. Defining meaningful changes in AD trials: the donepizil experience. J Ger Psych Neurol 1999;12:1:39—48.
25.Nagaraia D., Jayashree S. Randomised study of the dopamine receptor agonist piribedil in the treatment of mild cognitive impairment. Am J Psychiat 2001;158:9:1517—1519.
26.Petersen R.S., Smith G.E., Waring S.C. et al. Aging, memory and mild cognitive impairment. Int J Psychogeriat 1997;9:37—43.
27.Reisberg B. Global measures: utility in defining and measuring treatment response in dementia. Int J Psychogeriat 2007;19:3:421—456.
28.Scholing W.E. Controlled trial of trivasal retard 50 and comparision with trivasal 20 in the treatment of clinical and mental signs of neurovascular disease. Sci Med 1977;4:4—8.
29.Scholing W.E. A double-blind study using psychometric tests Trivastal versus a reference compound. Temp Med 1982;114.
30.Volkow N., Wang G., Fowler J. et al. Parallel loss of presynaptic and postsynaptic dopamine markers in normal aging. Ann Neurol 1998;44:1:143—147.
48 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 11, 2007 |
