
- •Кафедра биохимии
- •Современные представления о биологическом окислении
- •Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания
- •Цикл Кребса
- •Реакции цтк
- •Энергетический баланс одного оборота цтк
- •Лекция № 5 Тема: Биологическое окисление. Окислительное фосфорилирование. Механизмы сопряжения и разобщения, нарушения.
- •Оксидазный путь использования кислорода в клетке - окислительное фосфорилирование
- •Механизм окислительного фосфорилирования
- •Изменение свободной анергии при переносе электронов по цпэ.
- •1). Механизм фосфорилирования
- •2) Транспорт веществ через мембрану митохондрий
- •3). Теплопродукция
- •Лекция № 6
- •2. Митохондриальные монооксигеназные системы
- •Диоксигеназные реакции
- •Пероксидазный и радикальный пути использования кислорода
- •Образование активных форм кислорода
- •Свойства активных форм кислорода
- •Использование активных форм кислорода в организме
- •Повреждающее действие активных форм кислорода в организме
- •Антиоксидантная система
- •1. Ферментативная антиоксидантная система
- •2. Неферментативная антиоксидантная система
Механизм окислительного фосфорилирования
Хемиосмотическая теория Митчелла
Для объяснения механизма окислительного фосфорилирования в 1961 году Митчеллом была предложена хемиосмотическая гипотеза, которая включала четыре независимых постулата, касавшиеся функции митохондрий:
Внутренняя мембрана митохондрий непроницаема для всех ионов.
Она содержит ряд белков-переносчиков, осуществляющих транспорт необходимых метаболитов и неорганических ионов.
При прохождении электронов по дыхательной цепи внутренней мембраны происходит перемещение Н+из матрикса в межмембранное пространство.
При достаточно большом протонном градиенте протоны начинают «течь» через АТФ-синтетазу, что сопровождается синтезом АТФ.
Современные представления
В настоящее время открыты все основные компоненты ЦПЭ ОФ, изучено их строение, свойства. Открыты основные принципы окислительного фосфорилирования, механизмы некоторых стадий, регуляция окислительного фосфорилирования.
Механизм окисления
Комплексы цепи окисления располагаются в мембране в порядке повышения их редокс-потенциала. При переходе электрона от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии.

Изменение свободной анергии при переносе электронов по цпэ.
E-FMN — комплекс I; E-FAD — комплекс II, b-c1 — комплекс III; aa3 — комплекс IV.
Часть этой свободной энергии используется для переноса протонов из матрикса митохондрий в межмембранное пространство, при этом на внутренней мембране создается протонный градиент (∆рН) (в матриксе рН выше, чем в цитозоле). Так как каждый протон несет положительный заряд, на мембране появляется разность потенциалов (∆V), внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В совокупности протонный градиент и разность потенциалов составляют электрохимический потенциал, который в типичной клетке составляет около 220 мВ, и складывается из 160 мВ ∆V и 60 мВ ∆рН (при ∆рН=1).
Механизм переноса протонов через мембрану до конца не изучен. Вероятно, у разных компонентов дыхательной цепи существуют разные механизмы сопряжения транспорта е- с перемещением Н+. Однако установлено что важную роль в этом процессе играет КоQ.
Цепь окисления
2е- от НАДН2, проходят через I комплекс (ФМН→SFe белок) на КоQ, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен).
КоQ с 2е- забирает 2Н+ из матрикса и превращается в КоQН2 (восстановление КоQ проходит также с участием комплекса II).
КоQН2 переносит 2е- на комплекс III, а 2Н+ в межмембранное пространство.
Цитохром С переносит е- c III комплекса на IV комплекс.
IV комплекс сбрасывает е- на О2, высвобождаемая при этом энергия обеспечивает перекачку Н+ (механизм переноса Н+ неизвестен).
НАДН2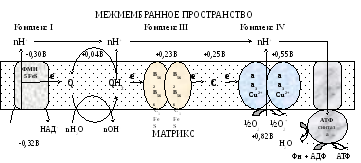
I, III и IV комплексы ЦПЭ называют пунктами сопряжения дыхания и фосфорилирования, так как они создают электрохимический потенциал, необходимый для фосфорилирования.
