
- •Кафедра биохимии
- •Современные представления о биологическом окислении
- •Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания
- •Цикл Кребса
- •Реакции цтк
- •Энергетический баланс одного оборота цтк
- •Лекция № 5 Тема: Биологическое окисление. Окислительное фосфорилирование. Механизмы сопряжения и разобщения, нарушения.
- •Оксидазный путь использования кислорода в клетке - окислительное фосфорилирование
- •Механизм окислительного фосфорилирования
- •Изменение свободной анергии при переносе электронов по цпэ.
- •1). Механизм фосфорилирования
- •2) Транспорт веществ через мембрану митохондрий
- •3). Теплопродукция
- •Лекция № 6
- •2. Митохондриальные монооксигеназные системы
- •Диоксигеназные реакции
- •Пероксидазный и радикальный пути использования кислорода
- •Образование активных форм кислорода
- •Свойства активных форм кислорода
- •Использование активных форм кислорода в организме
- •Повреждающее действие активных форм кислорода в организме
- •Антиоксидантная система
- •1. Ферментативная антиоксидантная система
- •2. Неферментативная антиоксидантная система
2. Митохондриальные монооксигеназные системы
Митохондриальные монооксигеназные системы состоят из нескольких компонентов, локализованных на внутренней поверхности внутренней мембране митохондрий, и катализируют высокоспецифичные реакции. Компонентами этих систем могут быть: НАДН2-зависимые ФАД-содержащее редуктазы,Fe2S2-белки (адренодоксин), цитохромы Р450,b5, элонгазы и т.д.
Эти системы находятся в стероидогенных тканях — в коре надпочечников, в семенниках, яичниках и плаценте; они участвуют в биосинтезе стероидных гормонов из холестерола (гид-роксилирование по С22и С20при отщеплении боковой цепи и по положениям 11β и 18).
Ферменты почечной системы катализируют гидроксилирование 25-гидроксихолекальциферола по положениям 1α и 24; в печени происходит гидроксилирование холестерола по положению 26 при биосинтезе желчных кислот.
Пролингидроксилазы включают гидроксильные группы в аминокислотные остатки пролина в молекуле проколлагена. Донором протонов и электронов для нее является витамин С. С оксипролином зрелый коллаген приобретает большую механическую прочность.
Диоксигеназные реакции
Диоксигеназыэто ферменты, которыевключают в субстрат оба атома молекулы кислорода:
А + О2→ АО2
Таким путем окисляются циклические трудноокисляемые структуры, реакции идут с разрывом цикла. Диоксигеназные реакции протекают на цитоплазматической поверхности гладкого ЭПР.
Например, гомогентизатдиоксигеназа печени, содержит Fe2+, участвует в катаболизме тирозина:
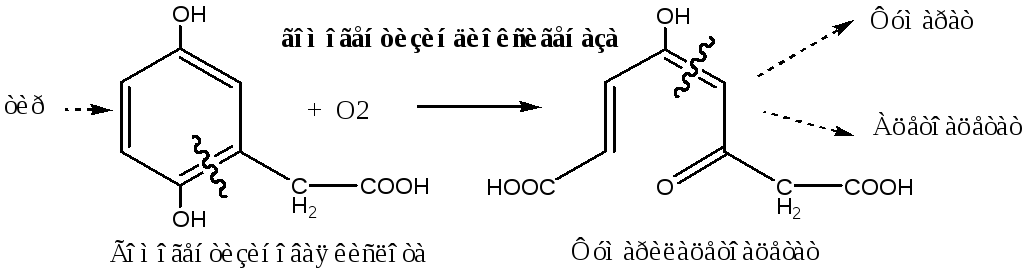
L-триптофандиоксигеназа печени, содержит гем, участвует в катаболизме триптофана:

Пероксидазный и радикальный пути использования кислорода
Кислород - потенциально опасное вещество. Молекулярный кислород О2и кислород в составе молекулы Н2О стабильные соединения, потому что их внешняя электронная орбита укомплектована электронами. Химические соединения, в составе которых кислород имеет промежуточную степень окисления, имеют высокую реакционную способность и называютсяактивными формами кислорода. К активным формам кислорода относятся свободные радикалы кислорода и перекиси.Свободный радикал- свободный атом или частица с неспаренным электроном.
Образование активных форм кислорода
Активные формы кислорода во многих клетках образуются в основном в результате последовательного одноэлектронного присоединения 4 электронов к 1 молекуле кислорода:
О2+ 1е-→ О∙2супероксидный анион-радикал.
О∙2+1е-→ О2-2пероксидный анион, он быстро протонируется с образованием перекиси водорода О2-2+ 2Н+→ Н2О2
Н2О2+ 1е-→ НО∙ + ОН-гидроксильный радикал, ОН- протонируется с образованием воды ОН- + Н+→ Н2О
ОН∙ + 1е-→ Н2О
В организме донорами электронов являются:
1). ЦПЭ. Утечка электронов из ЦПЭ на кислород является основным путем образования активных форм кислорода в большинстве клеток:
В цепи окислительного фосфорилирования Q принимая 1 электрон превращается в свободный радикал семихинон НQ∙, который при реоксигенации ишемических тканей может непосредственно взаимодействовать с кислородом, образуя супероксидный анион-радикал:HQ· + O2 → Q+ О∙2 + H+;
в монооксигеназных реакциях электрон с цитохрома Р450переходит на кислород с образованием супероксидного анион-радикала, который иногда теряется с активного центра.
Аэробные дегидрогназы (ФАД-зависимые оксидазы) переносят электроны и протоны с субстрата на кислород с образованием перекиси водорода. Примеры таких оксидаз — оксидазы аминокислот, супероксид дисмутаза, оксидазы, локализованные в пероксисомах.
2). Металлы переменной валентности. Наличие в клетках Fe2+или ионов других переходных металлов катализирует образования гидроксильных радикалов и других активных форм кислорода. Например, в эритроцитах окисление иона железа гемоглобина способствует образованию супероксидного анион-радикала.
Hb(Fe2+) +O2→MetHb(Fe3+) + О∙2
H2O2 + Fe2+ →Fe3+ + HO- + HO· (реакция Фентона)
HOCl + Fe2+ → Fe3+ + Cl- + HO· (реакция Осипова)
3). Радикалы. Активные формы кислорода, обмениваясь электроном, легко переходят друг в друга: О∙2 + Н2О2→ О2+ НО∙ + ОН-
Активные формы кислорода в организме также могут образовываться при гомолитическом разрыве связей под действием ионизирующего излучения. Ионизирующее излучение вызывает например, радиолиз воды с образованием Н2; Н2О2 и свободных радикалов: Н·, НО∙, О·. Это процесс в основном происходит на поверхности тела - в коже (понятие фотостарения).
