- •Кафедра биохимии
- •Современные представления о биологическом окислении
- •Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания
- •Цикл Кребса
- •Реакции цтк
- •Энергетический баланс одного оборота цтк
- •Лекция № 5 Тема: Биологическое окисление. Окислительное фосфорилирование. Механизмы сопряжения и разобщения, нарушения.
- •Оксидазный путь использования кислорода в клетке - окислительное фосфорилирование
- •Механизм окислительного фосфорилирования
- •Изменение свободной анергии при переносе электронов по цпэ.
- •1). Механизм фосфорилирования
- •2) Транспорт веществ через мембрану митохондрий
- •3). Теплопродукция
- •Лекция № 6
- •2. Митохондриальные монооксигеназные системы
- •Диоксигеназные реакции
- •Пероксидазный и радикальный пути использования кислорода
- •Образование активных форм кислорода
- •Свойства активных форм кислорода
- •Использование активных форм кислорода в организме
- •Повреждающее действие активных форм кислорода в организме
- •Антиоксидантная система
- •1. Ферментативная антиоксидантная система
- •2. Неферментативная антиоксидантная система
Лекция № 6
Тема: Биологическое окисление. Механизмы оксигеназного и
свободно - радикального окисления веществ. АОЗ клетки.
Факультеты: лечебно-профилактический, медико-профилактический, педиатрический. 2 курс.
ОКСИГЕНАЗНЫЙ ПУТЬ ИСПОЛЬЗОВАНИЯ КИСЛОРОДА
Оксигеназы это ферменты, которые катализируют включение кислорода в молекулу субстрата, они участвуют в синтезе и деградации многих типов метаболитов. Оксигеназы работают в составе мультиферментных комплексов, встроенных в мембрану. По способу включения кислородаих делят на: монооксигеназы и диоксигеназы.
Монооксигеназные реакции
Монооксигеназыэто ферменты, которыевключают в субстрат только один атом молекулы кислорода. Другой атом кислорода восстанавливается до воды с участием электронов и протонов НАДФН2, НАДН2, реже витамин С: А-Н + О2+ ZH2→ А-ОН + Н2О + Z
Монооксигеназные реакции протекают на цитоплазматической поверхности гладкого ЭПР, их называют микросомальным окислением, и на внутренней поверхности внутренней мембраны митохондрии.
1. Микросомальные монооксигеназные системы
Катализируют низкоспецифичные реакции. Эти монооксигеназы функционируют в комплексе с различными ЦПЭ:
А. Цепь НАДФН2-Р450 редуктаза – Цитохром Р450
Донорами протонов и электронов для этой цепи являются НАДФН2.
.НАДФН2-Р450 редуктаза. Цитозольный домен содержит 2 кофермента ФАД и ФМН, гидрофобный домен фиксирует фермент в мембране. НАДФН2-Р450редуктаза переносит 2 электрона с НАДФН2на цитохром Р450.
Цитохром Р450– интегральный гемопротеин, содержит простетическую группу гем, имеет участки связывания для кислорода и субстрата. Открыто 150 генов, кодирующих различные изоформы цитохрома Р450. Каждая из изоформ Р450 имеет много субстратов. Цитохром Р450передает 2 электрона на 1 атом молекулы кислорода, который превращается в О2-, при взаимодействии с 2 протонами О2- дает воду. Второй атом молекулы кислорода включается в субстратRH, образуяROH.
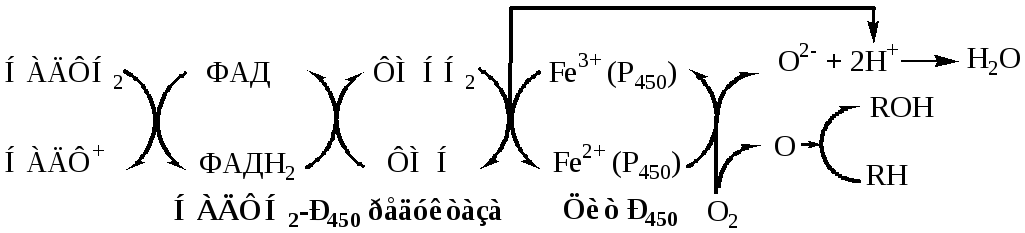
Субстратами являются гидрофобные вещества экзогенного (лекарства, ксенобиотики) и эндогенного (стероиды, жирные кислоты и т.д.) происхождения.
Регуляция активности осуществляется индукцией синтеза ферментов. Открыто более 250 веществ-индукторов. Например: барбитураты, спирты, кетоны, стероиды, ароматические углеводороды.
Б. Цепь НАДН2-цитохром b5 редуктаза – Цитохром b5 – стеароил-КоА-десатураза
Донорами протонов и электронов для этой цепи являются НАДН2.
НАДН2-цитохром b5 редуктаза– двухдоменный белок, цитозольный домен содержит ФАД, гидрофобный домен фиксирует фермент в мембране. НАДН2-b5редуктаза переносит 2 электрона с НАДН2на цитохромb5.
Цитохром b5. Цитозольный домен содержит гем, гидрофобный домен фиксирует фермент в мембране. Цитохромb5может передавать свои электроны на различные ферменты (цитохром Р450, Стеароил-КоА-десатуразу и т.д.), образуя различные ЦПЭ, при этом он участвует в десатурации и элонгации жирных кислот, в синтезе холестерина, плазминогенов и церамида.
Стеароил-КоА-десатураза– интегральный фермент, содержит негеминовое железо. Катализирует образование 1 двойной связи между 9 и 10 атомами углерода в жирных кислотах. Стеароил-КоА-десатураза переносит электроны с цитохромаb5на 1 атом кислород, при участии протонов этот кислород образует воду. Второй атом кислорода включается стеариновую кислоту с образованием её оксиацила, который дегидрируется до олеиновой кислоты.