
- •Методические указания к лабораторным занятиям по дисциплине «Химия»
- •Сыктывкар, 2016
- •1 Техника безопасности при работе в лаборатории органической
- •1.1 Общие правила работы
- •1.2 Работа с взрывоопасными и горючими веществами
- •1.3 Общие методические советы
- •2 Методы очистки органических соединений
- •2.1 Очистка твердых органических соединений методом перекристаллизации
- •2.2 Очистка твердых органических соединений методом возгонки
- •2.3 Определение температуры плавления
- •2.4 Очистка жидких органических соединений
- •2.4.1. Простая перегонка
- •2.4.2. Дробная (фракционная) перегонка
- •2.4.3. Определение показателя преломления
- •3. Синтез органических соединений Иодоформ
- •Бромэтан
- •Уксусноэтиловый эфир
- •Углеводороды
- •Контрольные вопросы по теме «Углеводороды»
- •Галогенпроизводные углеводородов
- •Контрольные вопросы по теме «Галогенпроизводные углеводородов»
- •Оксисоединения: спирты, фенолы
- •Контрольные вопросы по теме «Оксисоединения: спирты, фенолы»
- •Карбонильные соединения: альдегиды, кетоны
- •Контрольные вопросы по теме «Карбонильные соединения»
- •Углеводы
- •Контрольные вопросы по теме
- •Карбоновые кислоты и их производные
- •Контрольные вопросы по теме «Карбоновые кислоты и их производные»
- •Ароматические амины
- •Контрольные вопросы по теме «Ароматические амины»
- •Рекомендуемая литература
Контрольные вопросы по теме «Карбоновые кислоты и их производные»
Назовите лабораторный способ получения уксусной кислоты. Напишите уравнение реакции.
Какие свойства уксусной кислоты проявляются при взаимодействии её с магнием. Напишите уравнение реакции.
Какую реакцию применяют для удаления ионов Fe(III) из раствора. Напишите уравнение реакции.
Какие особенности в строении имеет муравьиная кислота? Напишите уравнение реакций серебряного зеркала, окисление перманганатом калия и разложения муравьиной кислоты.
Сравните кислотные свойства щавелевой кислоты и уксусной. Какая кислота сильнее?
Напишите уравнения реакций разложения и окисления щавелевой кислоты.
Напишите уравнения реакции образования уксусно-этилового эфира. В чем заключается роль концентрированной серной кислоты? Рассмотрите механизм реакции этерификации.
Напишите уравнения реакций гидролиза уксусно-этилового эфира в разных средах. Рассмотрите механизм реакций гидролиза уксусно-этилового эфира в разных средах.
Приведите уравнения реакций, доказывающих непредельный характер олеиновой кислоты.
Сравните кислотные свойства молочной кислоты и уксусной. Какая кислота сильнее?
Напишите уравнения реакций разложения и окисления молочной кислоты.
Сравните реакционную способность бензойной и салициловой кислот по отношению к бромной воде, способности к окислению, отношению к нагреванию.
Напишите уравнения реакций бромирования салициловой кислоты при избытке брома. Напишите уравнение реакции, протекающей при нагревании салициловой кислоты.
Ароматические амины
Опыт № 1. Образование и разложение соли анилина
К 5-6 каплям анилина добавляют 2-3 мл воды и смесь сильно встряхивают. В полученную эмульсию опускают красную лакмусовую бумагу. Окраска индикатора не меняется.
Эмульсию анилина делят на две части. К одной части прибавляют по каплям при встряхивании концентрированную соляную кислоту. Постепенно эмульсия превращается в однородную жидкость. При прибавлении к ней раствора гидроксида натрия жидкость мутнеет. К другой части эмульсии анилина прибавляют по каплям при встряхивании серную кислоту. Выпадает белый осадок. При добавлении раствора гидроксида натрия осадок растворяется и жидкость мутнеет.
Анилин, как и все амины, является основанием. Однако непосредственно связанное с аминогруппой ароматическое ядро резко ослабляет основные свойства ароматических аминов. Анилин гораздо более слабое основание, чем, например, аммиак. Водный раствор анилина не окрашивает красный лакмус в синий цвет.
Анилин образует соли только с сильными минеральными кислотами:


Большинство солей анилина хорошо растворимы в воде, хуже растворим сульфат. Соли анилина в водном растворе сильно гитдролизованы, эти растворы имеют резко кислую реакцию.
Опыт № 2. Бромирование анилина
К 5 мл воды приливают 2-3 капли анилина и смесь сильно встряхивают. К полученной эмульсии по каплям прибавляют бромную воду. Смесь обесцвечивается, и выпадает белый осадок триброманилина.
Введение в ароматическое кольцо аминогруппы резко повышает подвижность атомов водорода при атомах углерода бензольного кольца, поэтому анилин очень легко бромируется даже в разбавленном водном растворе с образхованием малорастворимого в воде 2,4,6-триброманилина:
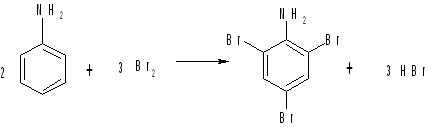
В результате бромирования слабые основные свойства анилина еще больше ослабевают, и триброманилин почти не растворим в разбавленных кислотах.
Опыт № 3. Окисление анилина
К 1 мл анилиновой воды добавляют 2-3 капли раствора бихромата калия и 0,5 мл раствора разбавленной серной кислоты. Жидкость окрашивается в интенсивный темно-зеленый цвет, переходящий в синий, а затем в черный.
Окисление анилина протекает очень легко, и в зависимости от условий и характера окислителя образуются различный соединения: азобензол, азооксибензол, нитробензол, бензохинон и т.д. В условиях описанного опыта анилин при окислении дает различные слодные окрашенные соединения, содержащие хиноидную группу:
П родукт
окисления анилина бихроматом калия –
черный анилин – очень стоек к кислотам
ищелочам. Его часто применяют для
крашения волокна, а также в лабораториях
для окрашивания рабочих столов.
родукт
окисления анилина бихроматом калия –
черный анилин – очень стоек к кислотам
ищелочам. Его часто применяют для
крашения волокна, а также в лабораториях
для окрашивания рабочих столов.
Опыт № 4. Получение ацетанилида
В пробирке сильно взбалтывают смесь 1 мл анилина и 3 мл воды. К полученной эмульсии приливают 1 мл уксусного ангидрида. Пробирку закрывают пробкой и сильно встряхивают. Выделяются кристаллы ацетанилида, и смесь застывает в густую массу. Химизм процесса:

