
биохимия краткий курс часть 2
.pdfГосударственное бюджетное образовательное учреждение высшего профессионального образования «ИРКУТСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ
УНИВЕРСИТЕТ» Министерства здравоохранения Российской Федерации
И. Э. Егорова, А. И. Суслова, В. И. Бахтаирова
БИОХИМИЯ
Часть II
Учебное пособие для студентов
Рекомендовано Учебно-методическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия
для студентов, обучающихся по основным профессиональным образовательным программам с высшего образования – программам специалитета по специальности Фармация № 117/ 05.05-20 от 02.04 2014
Иркутск
ИГМУ
2014
1
УДК 612.015.(075.8)
ББК 28.902я73 Е 30
Авторы:
И. Э. Егорова – канд. мед. наук, доцент кафедры химии и биохимии ГБОУ ВПО ИГМУ Минздрава России,
А. И. Суслова – канд. мед. наук, доцент кафедры химии и биохимии ГБОУ ВПО ИГМУ Минздрава России,
В. И. Бахтаирова –зав. кафедрой химии биохимии, канд. мед. наук, доцент ГБОУ ВПО ИГМУ Минздрава России
Рецензенты:
А. Б. Салмина – д-р мед.наук, профессор, зав. кафедрой биологической химии с курсом медицинской, фармацевтической и токсикологической химии Красноярского государственного медицинского университета имени
В. Ф. Войно-Ясенецкого Л. П. Никитина – профессор кафедры химии и биохимии ГБОУ ВПО ЧГМА
Минздрава России, канд. мед. наук
Егорова, И. Э.
Е 30 Биохимия. Часть II. : учебное пособие для студентов / И. Э. Егорова, А. И. Суслова, В. И. Бахтаирова, ГБОУ ВПО ИГМУ Минздрава России. – Иркутск : ИГМУ, 2014. – 83с.
Пособие «Биохимия. Часть II» предназначено для обучающихся как учебный материал, помогающий более полно усвоить учебную дисциплину «Биологическая химия». В данном пособии отражены следующие разделы: обмен нуклеотидов и нуклеиновых кислот, гормоны и сигналтрансдукторные системы, регуляция водно-минерального обмена, роль печени в пигментном обмене, фармацевтическая биохимия. В пособии представлен теоретический материал, химизм некоторых биохимических процессов, а также имеются тестовые задания для проверки усвоения темы.
Учебное пособие предназначено для обучающихся по основным профессиональным образовательным программам с высшего образования – программам специалитета по специальности «Фармация».
УДК 612.015.(075.8), 2013 ББК 28.902я73, 2013
©Егорова И. Э., Суслова А. И., Бахтаирова В. И., 2014
©ГБОУ ВПО ИГМУ Минздрава России, 2014
2
|
СОДЕРЖАНИЕ |
|
|
Список сокращений……………………………………………………. |
4 |
|
Введение…………………………………………………………………. |
6 |
1. |
Нуклеотиды. Матричные синтезы…………………………………… |
7 |
1.1. |
Обмен нуклеотидов……………………………………………………… |
7 |
1.2.Репликация……………………………………………………………….. 10
1.3.Транскрипция……………………………………………………………. 12
1.4.Биосинтез белка………………………………………………………….. 14
1.5. |
Медицинские аспекты матричных синтезов…………………………… |
16 |
1.6 |
Молекулярная медицина и фармация |
19 |
1.7.. |
Тестовые задания ………………………………....................................... |
23 |
2. |
Гормоны и сигнал-трансдукторные системы………………………. |
25 |
2.1. |
Классификация гормонов и рецепторов……………………………...... |
25 |
2.2. |
Механизмы действия липофильных гормонов………………………… |
27 |
2.3. |
Быстрые системы………………………………………………………… |
28 |
2.4. |
Основные системы вторых посредников………………………………. |
30 |
2.5. |
Нейропептиды. Гормоны гипоталамуса и гипофиза…………………... |
35 |
2.6. |
Инсулин и сахарный диабет……………………………………………... |
37 |
2.7. |
Катехоламины и йодтиронины………………………………………….. |
42 |
2.8 |
Стероидные гормоны и эйкозаноиды....................................................... |
47 |
2.9.. |
Тестовые задания………………………………….................................... |
53 |
3. |
Водно-минеральный обмен и его регуляция………………………... |
55 |
3.1. |
Ионные каналы и транспортные АТФазы……………………………… |
55 |
3.2. |
Антидиуретический гормон в норме и при патологии………………… |
56 |
3.3. |
Ренин-ангиотензин-альдостероновая система…………………………. |
57 |
3.4 |
Обмен кальция и фосфата.......................................................................... |
59 |
3.5.. |
Тестовые задания………………………………………………………… |
62 |
4. |
Роль печени в пигментном обмене. Желтухи |
64 |
4.1. |
Тестовые задания………………………………………………………… |
66 |
5. |
Фармацевтическая биохимия………………………………………… |
68 |
5.1. |
Классификация лекарств........................................................................... |
68 |
5.2. |
Биохимические аспекты фармакокинетики…………………………… |
71 |
5.3. |
Метаболизм лекарств и других ксенобиотиков……………………….. |
74 |
5.4 |
Индукция защитных систем… |
77 |
5.5.. |
Тестовые задания………………………………………………………… |
78 |
|
Эталоны ответов к тестовым заданиям……………………………… |
81 |
|
Рекомендуемая литература……………………………………………. |
82 |
3
СПИСОК СОКРАЩЕНИЙ
А– Адреналин
АД |
– |
Артериальное давление |
АДГ |
– |
Антидиуретический гормон |
АКТГ |
– |
Адренокортикотропный гормон |
АлАТ |
– |
Аланинаминотрансфераза |
АМФ |
– |
Аденозинмонофосфат |
цАМФ |
– |
Циклический АМФ |
АсАТ |
– |
Аспартатаминотрансфераза |
АПФ |
– |
Ангиотензинпревращающий фермент |
АТ |
– |
Ангиотензин |
АТФ |
– |
Аденозинтрифосфат |
АХ |
– |
Ацетилхолин |
АЦ |
– |
Аденилилциклаза |
БР |
– |
Билирубин |
ВИЧ |
– |
Вирус иммунодефицита человека |
ВМО |
– |
Водно-минеральный обмен |
Г |
– |
Гуанин |
ГАМК |
– |
Гамма-аминомасляная кислота |
ГКС |
– |
Глюкокортикостероиды |
ГМФ |
– |
Гуанозинмонофосфат |
цГМФ |
– |
Циклический ГМФ |
ГНГ |
– |
Глюконеогенез |
ГТ |
– |
Глутатионтрансфераза |
ГТФ |
– |
Гуанозинтрифосфат |
ГЦ |
– |
Гуанилилциклаза |
ГЭБ |
– |
Гематоэнцефалический барьер |
ДА |
– |
Дофамин |
ДАГ |
– |
Диацилглицерин |
ДНК |
– |
Дезоксирибонуклеиновая кислота |
ДОФА |
– |
Диоксифенилаланин |
ДЦ |
– |
Дыхательная цепь |
ЖКТ |
– |
Желудочно-кишечный тракт |
ИБС |
– |
Ишемическая болезнь сердца |
ИЛ |
– |
Интерлейкин |
ИМФ |
– |
Инозинмонофосфат |
ИН |
– |
Инсулин |
ЙТ |
– |
Йодтиронины |
ИФ3 |
– |
Инозитолтрифосфат |
ИФР |
– |
Инсулиноподобный фактор роста |
КА |
– |
Катехоламины |
КМ |
– |
Кальмодулин |
КОМТ |
– |
Катехол-О-метилтрансфераза |
КСБ |
– |
Ксенобиотики |
КЩР |
− |
Кислотно-щелочное равновесие |
ЛДГ |
– |
Лактатдегидрогеназа |
ЛПВП |
– |
Липопротеины высокой плотности |
ЛПНП |
– |
Липопротеины низкой плотности |
МАО |
– |
Моноаминоксидаза |
МЛУ |
– |
Множественная лекарственная устойчивость |
НА |
– |
Норадреналин |
НАДФ |
– |
Никотинамидадениндинуклеотидфосфат |
НДФ |
– |
Нуклеозиддифосфат |
НК |
– |
Нуклеиновые кислоты |
НМФ |
– |
Нуклеозидмонофосфат |
|
|
4 |
НПВП |
– |
Нестероидные противовоспалительные препараты |
НТФ |
– |
Нуклеозидтрифосфат |
НУП |
– |
Натрийуретические пептиды |
НЭЖК |
– |
Неэстерифицированные жирные кислоты |
ОКТ |
– |
Орнитинкарбамоилтрансфераза |
ОМФ |
– |
Оротидинмонофосфат |
ОЦК |
– |
Объем циркулирующей крови |
ПАУ |
– |
Полициклические ароматические углеводороды |
ПК |
– |
Протеинкиназа |
ПОЛ |
– |
Перекисное окисление липидов |
ППЦ |
– |
Полипептидная цепь |
ПТГ |
− |
Паратиреоидный гормон (паратирин) |
ПЦР |
– |
Полимеразная цепная реакция |
РААС |
– |
Ренин-ангиотензин-альдостероновая система |
РНК |
– |
Рибонуклеиновая кислота |
аа-тРНК |
– |
Аминоацил-транспортная РНК |
мРНК |
– |
Матричная РНК |
тРНК |
– |
Транспортная РНК |
Р-ГП |
– |
Р-гликопротеин |
РЭС |
– |
Ретикуло-эндотелиальная система |
СД |
– |
Сахарный диабет |
СЖК |
– |
Свободные жирные кислоты |
СПИД |
– |
Синдром приобретенного иммунодефицита |
ССС− Сердечно-сосудистая система
СТГ |
– |
Соматотропный гормон |
СТС |
– |
Сигнал-трансдукторная система |
Т– Тимин
Т3 |
– |
Трийодтиронин |
Т4 |
– |
Тетрайодтиронин |
ТГФК |
– |
Тетрагидрофолиевая кислота |
ТК |
– |
Тирозиновая киназа |
ТМФ |
– |
Тимидинмонолфосфат |
ТТГ |
– |
Тиреотропный гормон |
ТФ |
– |
Транскрипционный фактор |
У– Урацил
УМФ |
– |
Уридинмонофосфат |
УТФ |
– |
Уридинтрифосфат |
УФЛ |
– |
Ультрафиолетовые лучи |
ФДЭ |
– |
Фосфодиэстераза |
ФИ |
– |
Фосфатидилинзитид |
ФИФ2 |
– |
Фосфатидилинозитидбисфосфат |
ФИФ3 |
|
Фосфатидилинозитидтрисфосфат |
ФРК |
– |
Факторы роста клеток |
ХС |
– |
Холестерин |
Ц– Цитозин
ЦОГ |
– |
Циклооксигеназа |
ЦК |
− |
Цитокины |
ЦНС |
– |
Центральная нервная система |
ЦТК |
– |
Цикл трикарбоновых кислот |
ЦТФ |
– |
Цитидинтрифосфат |
ЭПР |
– |
Эндоплазматический ретикулум |
ЭФР |
– |
Эндотелиальный фактор роста |
ЮГА |
– |
Юкстагломерулярный аппарат |
5
ВВЕДЕНИЕ
Биологическая химия – это наука, которая изучает химическую природу веществ, входящих в состав живых организмов, их превращения и связь этих превращений с функциями клеток, тканей, органов и организма в целом. Она является базовой основой для глубокого понимания того, что происходит на всех уровнях организации живой материи. Познание биохимических процессов, протекающих в организме здорового человека, позволяет понять в дальнейшем природу различных заболеваний, поскольку они представляют собой, в большинстве случаев, отклонения в биохимических реакциях, происходящих в организме.
Изучение биологической химии на фармацевтическом факультете тесно связано с проблемами химии, биологии, медицины и фармации в целом. Велика роль биохимии в понимании сути патологических процессов и молекулярных механизмов действия лекарственных веществ. Одной из задач биологической химии является изучение молекулярных основ взаимодействия живых организмов с физическими (излучения), химическими (ксенобиотики), биологическими (вирусы) факторами окружающей среды.
Наиболее глубокие знания действия лекарств и токсических веществ основываются на исследовании места их вторжения в процессы обмена веществ. Эти знания необходимы не только для понимания их механизмов действия, но и для разработки рациональной лекарственной формы, учета возможной несовместимости лекарств, оценки эффективности лекарств на основе изучения их метаболизма, особенностей транспорта, избирательного накопления, анализа в процессе производства и хранения лекарств, стандартизации и контроля их качества.
Понимание биохимических закономерностей в организме здорового человека и при патологии позволит более успешно усвоить последующие дисциплины, понять молекулярные механизмы возникновения устойчивости к лекарствам бактерий и вирусов. Эти знания позволят уяснить причины возникновения мультилекарственной устойчивости у онкобольных, создадут мотивацию к поиску и разработке новых лекарственных средств.
В предлагаемом учебном пособии представлены материалы по следующим разделам: обмен нуклеотидов и нуклеиновых кислот, гормоны и сигнал-трансдукторные системы, регуляция водно-минерального обмена, роль печени в пигментном обмене, фармацевтическая биохимия.
Учебное пособие призвано скоординировать наиболее актуальные вопросы в быстро развивающихся разделах биологической химии, имеющих значение для развития фармакогенетики и фармакогеномики. А также обратить внимание обучающихся на то, что 2/3 современных лекарств воздействуют на сигнал-трансдукторные системы.
6
1. НУКЛЕОТИДЫ. МАТРИЧНЫЕ БИОСИНТЕЗЫ
1.1. ОБМЕН НУКЛЕОТИДОВ
Несмотря на то, что некоторое количество нуклеозидов и свободных азотистых оснований образуется при гидролизе полинуклеотидов пищи, большая часть включающихся в нуклеиновые кислоты нуклеотидов синтезируется заново.
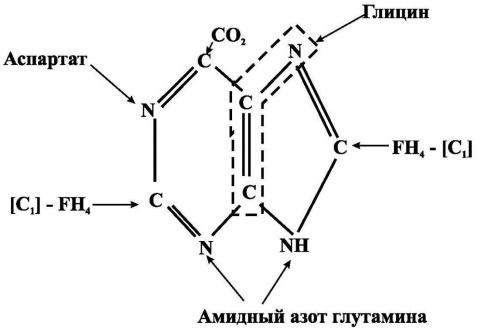
Синтез пуриновых нуклеотидов начинается с того, что к рибозо5 фосфату поэтапно присоединяются различные соединения, из которых формируется пуриновое кольцо. Предшественниками пуринового кольца являются: аспартат, глутамин, СО2, глицин, кроме того два атома углерода поставляет тетрагидрофолат (рис.1). Первым синтезированным пуриновым нуклеотидом является ИМФ, из него затем образуются АМФ и ГМФ. Печень является основным местом образования пуриновых нуклеотидов. Она снабжает пуринами ткани, не способные к их синтезу: клетки крови и частично мозг.
Рис. 1. Предшественники пуринового кольца
У пиримидиновых нуклеотидов (в отличие от пуриновых) сначала из предшественников собирается пиримидиновое кольцо, а затем к готовому кольцу присоединяется рибозо5фосфат. Источниками пиримидинового кольца являются аспартат и карбамоилфосфат. Первым синтезированным пиримидиновым нуклеотидом является оротидинмонофосфат. Из него при декарбоксилировании образуется УМФ; из УТФ при воздействии глутамина – ЦТФ. Для синтеза ТМФ из дезоксиУМФ необходим тетрагидрофолат.
Для синтеза нуклеиновых кислот необходимы НТФ, которые образуются из НМФ при участии АТФ: НМФНТФ. Для синтеза ДНК необходимы дезоксиНТФ, которые образуются путем восстановления НДФ в дезоксиНДФ при участии фермента
7

рибонуклеотидредуктазы (рис. 2). Непосредственным восстановителем НДФ является глутатион или белок тиоредоксин, сульфгидрильные группы которых в ходе этой реакции окисляются.
Рис. 2 . Синтез дезоксирибонуклеотидов
Катаболизм пуриновых нуклеотидов происходит без разрыва пуринового кольца и приводит к образованию мочевой кислоты, которая плохо растворима (рис.3).При повышении концентрации мочевой кислоты в плазме крови возникает гиперурикемия, которая может явиться причиной развития подагры.
Катаболизм пиримидинов (рис. 4.) происходит с разрывом пиримидинового кольца, конечными продуктами его являются аммиак, СО2, β-аланин (образуется при катаболизме урацила и цитозина) и β-аминоизомасляная кислота (образуется при катаболизме тимина).
Нуклеиновые кислоты представляют собой полинуклеотиды. ДНК и РНК содержат разный набор нуклеотидов. ДНК содержит тимин, цитозин, гуанин, аденин, РНК вместо тимина содержит урацил. В образовании РНК принимают участие рибонуклеотиды, а ДНК дезоксирибонуклеотиды. Функции, выполняемые разными видами нуклеиновых кислот, также различны: все виды РНК участвуют в биосинтезе белка, а ДНК участвует в сохранении, передаче наследственной информации и делении клетки. Первичная структура нуклеиновых кислот представляет собой определенную последовательность НМФ, соединенных фосфодиэфирными связями. Вторичная структура РНК представляет одиночную спираль с участками удвоения, а вторичная структура ДНК представляет двойную спираль (дуплекс), у которой цепи антипараллельны и комплементарны на всем протяжении, т.е. напротив аденина (А) одной цепи стоит тимин (Т) в другой цепи, напротив гуанина (Г) стоит цитозин (Ц).
8

Рис. 3. Катаболизм пуринов
Поэтому, согласно правилу Чаргаффа, число пуринов (А+Г) равно числу пиримидинов (Т+Ц). Между комплементарными азотистыми основаниями возникают водородные связи, которые удерживают обе цепи дуплекса (между А и Т две связи, между Г и Ц– три). Комплементарные основания уложены в стопку в сердцевине спирали. Между основаниями двухцепочечной молекулы в стопке возникают гидрофобные взаимодействия, стабилизирующие двойную спираль.
Рис. 4. Катаболизм пиримидинов
9

Третичная структура ДНК представляет собой суперспираль, благодаря которой длина ДНК укорачивается в 10000 раз. Суперспирализация осуществляется с помощью разнообразных белков, т.е. с химической точки зрения ДНК – это нуклеопротеин (комплекс белков и ядерной ДНК называют хроматином). Структурной единицей хроматина являются нуклеосомы, которые образуются путем «накручивания» молекулы ДНК вокруг «нуклеосомного кора», состоящего из 8 молекул гистоновых белков типа Н2 Н4.
Вклетке существуют разные виды РНК, которые выполняют разные функции. Рибосомальная РНК участвует в образовании рибосом, на которых происходит биосинтез белка. Матричная РНК передает информацию с ДНК на синтезируемый белок, транспортная РНК участвует в активации аминокислот и передает их на рибосомы. Малые некодирующие РНК выполняют каталитическую и регуляторную функции.
Воснове всех матричных биосинтезов лежит принцип комплементарности. Для матричных биосинтезов необходима матрица (нуклеиновая кислота), с которой будет считываться информация; активированные мономеры или субстраты для синтезов (НТФ или аминоацил-РНК), катализаторы (в их роли выступают ферменты и рибозимы), а также различные белковые факторы матричных биосинтезов.
1.2. РЕПЛИКАЦИЯ
Живые организмы в течение S-фазы клеточного цикла, которая предшествует делению клетки, удваивают содержание ДНК таким образом, что каждая дочерняя клетка после деления получает ДНК, идентичную родительской клетке. Процесс удвоения ДНК называют репликацией. При репликации каждая цепь родительской ДНК служит матрицей для синтеза новой комплементарной цепи. Причем матрица воспроизводится на всем ее протяжении. Вновь синтезированная ДНК имеет одну исходную (родительскую) и одну вновь синтезированную (дочернюю) цепь (рис.5). Субстратами для синтеза дочерней цепи служат дезоксиНТФ, для репликации необходимы ферменты: топоизомераза, хеликаза, праймаза, ДНКполимераза, ДНКлигаза.
|
–Т–А–Т–C–С–A–G– |
–Т–А –Т–С–С–А –G– |
|
|
● ● ● ● ● ● ● |
|
|
–А–Т –А–G–G–Т –С – |
–Т –А –Т–С–С–А –G– |
|
|
● ● ● ● ● ● ● |
|
|
–А –Т –А–G–G–Т –С – |
|
|
|
|
–Т–А –Т–С–С–А –G– |
|
|
● ● ● ● ● ● ● |
|
–A–T–A–G–G–T–C– |
–А–Т –А–G–G–Т –С – |
Исходная молекула ДНК |
Разошедшиеся цепи ДНК, |
Две молекулы ДНК, |
|
матрицы биосинтеза ДНК |
идентичные исходной |
|
Рис. 5. Механизм репликации ДНК. |
|
|
10 |
|
