
- •Направление
- •110300 Агроинженерия
- •Уфа 2011
- •Предисловие
- •Условные обозначения
- •1 Основы технической термодинамики
- •Задачи к разделу 1.
- •2 Смеси идеальных газов
- •2.1 Массовый состав смеси
- •Задачи к разделу 2
- •3 Теплоемкость газов
- •Задачи к разделу 3.
- •4 Термодинамические процессы газов
- •Задачи к разделу 4
- •5 Водяной пар. Диаграмма h,s водяного пара. Исследование паровых процессов по диаграмме h,s
- •6 Влажный воздух
- •Задачи к разделу 6.
- •Библиографический список
2 Смеси идеальных газов
В практике очень часто приходится встречаться с газовыми смесями. Например, рабочее тело тепловых двигателей, компрессоров, других теплотехнических устройств, дымовые газы представляют собой смесь газов.
При рассмотрении газовых смесей исходят из того, что смесь состоит из идеальных химически не взаимодействующих между собой газов. При этом каждый газ, входящий в состав смеси, ведет себя так, как будто бы он один при данной температуре занимает весь объем смеси и оказывает на стенки сосуда свое давление, называется парциальным.
По закону Дальтона давление смеси рсм равно сумме парциальным давлений газов, входящих в состав смеси:
Рсм=
Р1+Р2+…+Рп=![]() j,
2.1.
j,
2.1.
Где Pι – пропорциональное давление компонента, входящего в смесь.
Состав смеси может задан одним из следующих способов.
2.1 Массовый состав смеси
В абсолютных единицах массы
mсм=m1+
m2+…+
mn=![]() , 2.2
, 2.2
m1, m2, mn –массы отдельных компонентов смеси
в относительных массовых долях
![]() =q1+
q2
+…+ qn=1;
2.3
=q1+
q2
+…+ qn=1;
2.3
![]() ,
2.4
,
2.4
где qι=mι/mсм – массовая доля отдельного компонента смеси.
Объемный состав смеси
Vсм=V1+
V2+…+
Vn=![]() 2.5
2.5
где V1, V2 и тд. – приведены объемы отдельных компонентов смеси, м3;
в относительных объемных долях
![]() =1;
2.6
=1;
2.6
![]() 2.7
2.7
где
![]() - объемная доля отдельного компонента.
- объемная доля отдельного компонента.
Задание состава смеси числом молей соответствует заданию состава смеси по объему, так как мольная доля компонента равна его объемной доле.
Между массовыми и объемными долями смеси существует следующая зависимость
![]() ,
2.8
,
2.8
Следовательно,
![]() =qι
ρсм/ρι
2.9
=qι
ρсм/ρι
2.9
На основании следствия закона Авагадро
![]() и
и
![]() 2.10
2.10
Соответственно
![]() ,
2.11
,
2.11
Кажущая молекулярная масса газовой смеси
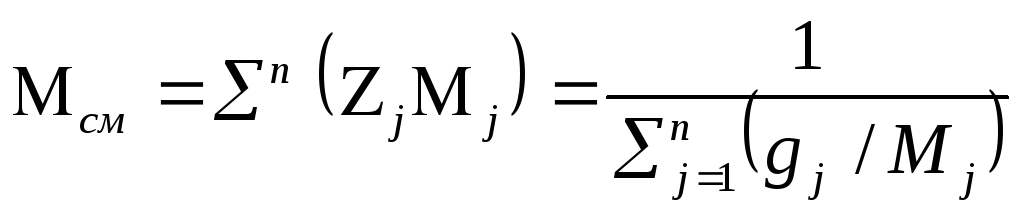 ,
2.12
,
2.12
Газовая постоянная смеси может быть определена по составу смеси и газовым постоянным отдельных компонентов:
Rсм=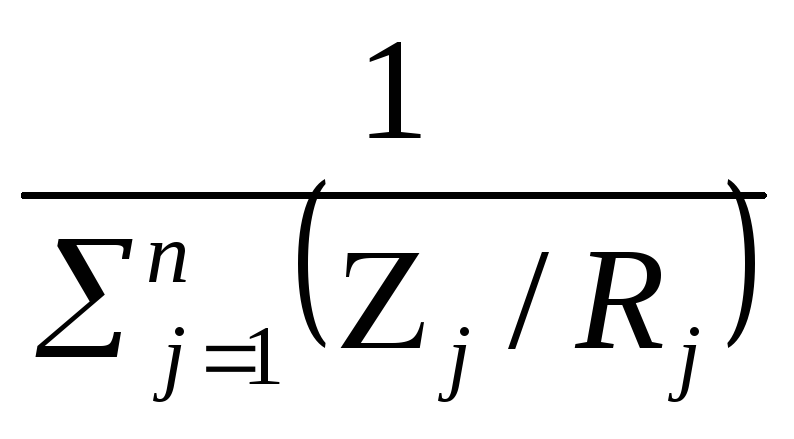
![]() ,
2.13
,
2.13
Или же по кажущейся молекулярной массе и универсальной газовой постоянной
Rсм=![]() ,
2.14
,
2.14
Теплоемкость смеси газов определяется по ее составу. Массовая теплоемкость смеси газов
ссм=q1с1+
q2с2+····+qnсn=
![]() 2.15
2.15
где С1, С2····Сn – массовые теплоемкости отдельных компонентов
q1, q2····qn – массовые доли отдельных компонентов.
Парциальное давление отдельного компонента.
Рι=![]() 2.16
2.16
Задачи к разделу 2
Задача 2.1. Определить массовый состав сухого воздуха, его удельную газовую постоянную, кажущуюся относительную молекулярную массу и плотность при абсолютном давлении 110 кПа и температуре 20% кислорода и 79% азота.
Решение.
Между массовыми и объемными составами
газовой смеси существует зависимость
![]()
Кажущуюся молекулярную массу газовой смеси можно определить по формуле 2.11
мсм==![]()
![]() 0М0+
0М0+![]() NМN=0,21·32+0,79·28=28,84
NМN=0,21·32+0,79·28=28,84![]()
Тогда
gN=![]() ·МN/Мсм=0,79
·28/28,84=0,767
·МN/Мсм=0,79
·28/28,84=0,767
g0=1-gN=1-0,767=0,233
Удельная газовая постоянная смеси определяется по формуле 2.14
Rсм=8314,3/Мсм=8314,3/28,84=288,3 кДж/(кг·K)
Плотность газовой смеси определяем из формулы
![]() см
=
см
=![]() =
=![]() 1,182
кг/м3.
1,182
кг/м3.
Задача 2.2. Смесь двух объемов водорода и одного объема кислорода называют гремучим газом. Определить кажущуюся молекулярную массу, газовую постоянную и массовый состав гремучего газа.
Задача 2.3. Смесь газов состоит из 1,0 м3 генераторного газа и 1,5 м3 воздуха, взятых при нормальных физических условиях. Определить газовую постоянную смеси газов и парциальные давления составляющих смеси. Плотность генераторного газа ρ2 принять равной 1,2 кг/м3.
Задача 2.4. В цилиндр газового двигателя засасывается газовая смесь, состоящая из 20 массовых долей воздуха и одной доли коксового газа в смеси.
Задача 2.5. Анализ продуктов сгорания, произведенный с помощью газоанализатора показал их следующий объемный состав: СО2=12,2%; О2=7,1%; СО=0,4%; N2=80,3%. Определить массовый состав входящих в смесь газов.
Задача
2.6. Определить
объем смеси газов при абсолютном давлении
100 кПа и температуре 900С,
образовавшийся при смешивании 100 кг
топочных газов с 50 кг воздуха. Массовый
состав топочных газов ![]() со=0,18;
qНо=0,08;
qо=0,02,
и qN=0,72.
со=0,18;
qНо=0,08;
qо=0,02,
и qN=0,72.
