
- •Производные п-аск, о-абк, м-абк, фенилуксусной и фенилпропионовой кислот Производные парааминосалициловой кислоты
- •Фп Натрия пара-аминосалицилат (паск-Nа) Natrii рага- aminosalicylas
- •Химические свойства
- •Подлиннность
- •Реакции подлинности
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Формы выпуска
- •Нфп Кислота мефенамовая (мефенаминовая)
- •Количественное определение
- •1.Алкалиметрия в ацетоне (растворитель), индикатор - тимоловый синий. Титруют NаОн от желтого до синего окрашивания
- •Производные арилалифатических кислот – фенилуксусной и фенилпропионовой
- •Diclofenac – Natrium (Ortophenum, Voltaren)
- •Описание
- •Растворимость
- •Реакции подлинности
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Ibuprofenum – Ибупрофен (Нурофен, Миг)
- •Описание
- •Чистота
- •Количественное определение
Производные п-аск, о-абк, м-абк, фенилуксусной и фенилпропионовой кислот Производные парааминосалициловой кислоты
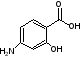 п-аминосалициловая
кислота
п-аминосалициловая
кислота
В 40х годах была установлена фармакологическая активность этого вещества. Натриевая соль ПАСК была одним из первых противотуберкулезных ЛС в связи с выраженным бактериостатическим действием в отношении микобактерий туберкулеза.
Фп Натрия пара-аминосалицилат (паск-Nа) Natrii рага- aminosalicylas
Натриевая соль п-аминосалициловой кислоты
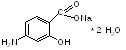
ФГ в структуре вещества: NН2 - первичная ароматическая аминогруппа, ОН - фенольный гидроксил, СООН - карбоксильная группа
Противотуберкулезное средство, антагонист п-аминобензойной кислоты
Получение – синтез, источник – м-аминофенол.
Процесс синтеза складывается из трех стадий:
Карбоксилирование м-аминофенола.
Выделение пара-аминосалициловой кислоты.
Получение натрия п-аминосалицилата
На первой стадии происходит карбоксилирование м-аминофенола по методу Кольбе-Шмидта (получение салициловой кислоты). Процесс идет под давлением диоксида углерода при to =103-105оС в присутствии гидрокарбоната калия. На второй стадии под действием 50% серной кислоты происходит выделение ПАСК. На третьей стадии ПАСК нейтрализуется гидрокарбонатом натрия и образуется ПАС-натрия.

Специфической примесью является м-аминофенол
Источником синтеза может быть нитробензол:

Описание: белый или белый с желтоватым оттенком или розоватый мелкокристаллический порошок. Легко растворим в воде, растворы при стоянии темнеют. Трудно растворим в спирте.
Химические свойства
Обусловлены полифункциональностью соединения, т.е. входящими в структуру лекарственного вещества ФГ:
ароматической аминогруппой,
фенольным гидроксилом и
карбоксильной группой.
На их свойствах основаны реакции подлинности и количественного определения, высокая лабильность ЛВ.
Подлиннность
УФ-спектрофотометрия.
УФ-спектр 0,001% водного раствора ПАСК-Nа, который имеет 2 максимума поглощения– 265нм и 299нм (свидетельствует о наличии фенольного гидроксила и ПАА).
ФС Соотношение оптических плотностей при длинах волн 265 и 299 нм должно быть в пределах 1,50-1,56 (указывает на отсутствие поглощающих при данных длинах волн примесей).
Величины удельных показателей поглощения при максимумах поглощения равны соответственно 736 и 483.
2. Температура плавления Т°пл=122оС.
Реакции подлинности
1. ФС Реакция на фенольный гидроксил – в кислой среде с раствором хлорида железа (III): образуется комплексное соединение (фиолетово-красное окрашивание).

В этой реакции, как и всегда в реакциях с солями тяжелых металлов, важна определенная реакция среды. Водные растворы ПАС-натрия имеют рН 6,5-8,5, в этой среде с хлоридом железа образуется комплекс коричнево-красного цвета. Поэтому проводят подкисление разведенной хлороводородной кислотой.
Эта реакция является фармакопейной реакцией подлинности на ПАС-натрия, доказывающей наличие фенольного гидроксила. Однако, у этой реакции есть еще одно значение. Мы имеем дело с очень редким случаем, когда реакция подлинности является одновременно и реакцией обнаружения примеси. Это токсичное, фармакологически неактивное вещество – м-аминосалицилат натрия:

Он образует с хлоридом железа комплекс такого же цвета, как и ПАС-натрия, однако со временем выпадает осадок коричневого цвета. По фармакопее после появления фиолетово-красного окрашивания раствор оставляют на 3 часа. Не должно наблюдаться появления осадка коричневого цвета.
2.ФС Реакция образования азокрасителя, основанная на наличии в структуре: первичной ароматической аминогруппы и фенольного гидроксила.
А) В методике ФС после диазотирования раствором нитрита натрия в кислой среде проводят азосочетание с β-нафтолом в щелочной среде, появляется красное окрашивание (ЛВ диазосоставляющая):
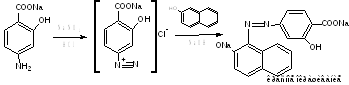
Б) в методике МФ-II после диазотирования ЛВ в качестве азосоставляющей берется α-нафтиламин. Реакция проводится в кислой среде. Образуется красное окрашивание, переходящее в оранжевое при добавлении раствора гидроксида натрия (ЛВ диазосоставляющая):

В) следующий вариант образования азокрасителя основан на наличии фенольного гидроксила. Следовательно, при добавлении диазореактива происходит азосочетание в одну стадию, в орто- или пара- положении по отношению к фенольному гидроксилу (ЛВ азосоставляющая по -ОН):

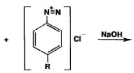 (
дописать самостоятельно)
(
дописать самостоятельно)
Г) есть еще один вариант, основанный на том, что ПАС-натрия имеет в структуре одновременно ПАА и фенольный гидроксил. Вначале проводят диазотирование по ПАА, затем азосочетание с ПАС-натрия (ЛВ диазо- и азосоставляющая). В щелочной среде сочетается как фенол:
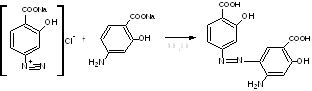
В кислой среде ПАС-натрия сочетается как амин, присоединение идет в 3-положении (пара- к ПАА).
3.На ион натрия –окрашивает пламя горелки в желтый цвет ФС.
При взаимодействии с цинкуранилацетатом образуется осадок желтого цвета.
(реакцию написать самостоятельно)
4. Реакция на карбоксильную группу – выделение свободной ПАСК (слабая к-та) из ее соли минеральной кислотой:
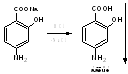
5. Реакция на карбоксильную и гидроксильную группы – с солями тяжелых металлов (с меди (II) сульфатом образует травянисто-зелёное окрашивание). (реакцию написать самостоятельно)
