
Тут есть жесткость воды
.pdf
как органическую, так и минеральную части сланцев. Сланцы содержат также ряд редких элементов - уран, ванадий, молибден, рений и др.
Таблица 2.8. Средний элементный состав органического вещества кукерсита
Химический элемент |
Символ |
Содержание, % |
Углерод |
C |
77,0 |
Водород |
H |
9,7 |
Кислород |
O |
10,6 |
Азот |
N |
0,4 |
Сера |
S |
1,6 |
Таблица 2.9.Техническая характеристика эстонских сланцев
Показатель |
Значение |
|
|
Содержание влаги, масс. % |
8-10 |
Содержание золы, масс. % |
45-48 |
Содержание минерального СО2, масс. % |
18-21 |
Содержание органического вещества на |
29-38 |
сухую массу, масс. % |
|
Теплота сгорания, МДж/кг |
8-11 |
Выход смолы на органическое вещество, % |
65,5 |
Выход смолы на сухую массу сланца, % |
13-15 |
Выход смолы на сухую массу сланца после |
18-20 |
обогащения, % |
|
Гранулометрический состав сланца, мм |
25-125 |
|
|
Кукерсит залегает в виде тонких (0,03 – 0,6 м) слоёв, разделённых прослоями известняков и мергелей (осадочная горная порода глинисто-карбонатного состава).
Рис. 2.31. Строение промышленного пласта (Каттай, 2000)
Промышленный пласт Эстонского месторождения образуют восемь слоёв кукерсита А, A', B, C, D, E, F1, F2 и пять разделяющих их прослоёв известняка D/E, C/D, B/C, A'/D, A/A' (рис. 2.30.). В сланцевых шахтах видно чередование слоев сланца и известняка (рис. 2.31.).
60

Сланец добывают открытым (в карьерах) и подземным (в шахтах) способами. Открытым способом сланец добывают с глубины до 30 метров, в шахтах – на глубине 40 – 70 метров.
Рис. 2.32. Промышленный пласт шахты Кохтла.
Следует отметить, что размещение сланцевого месторождения между Финским заливом и Чудским озером создает особые требования к защите окружающей среды. Финский залив охраняется Международной конвенцией по охране вод Балтийского моря (HELCOM). Чудское же озеро является крупнейшим водоемом чистой пресной воды, богатым рыбой.
Внастоящее время существуют три основных направления использования горючих сланцев:
полукоксование для получения жидкого топлива и химического сырья;
газификация для получения энергетического газа и синтез-газа;
прямое сжигание для выработки электрической и тепловой энергии.
Проводятся опытные работы по гидрогенизации обогащённого кукерсита с целью превращения органической массы сланца в жидкие продукты.
В перспективе самое важное направление использования горючих сланцев – получение из них жидкого, в первую очередь моторного топлива. По мере истощения запасов нефти это направление становится всё более актуальным.
Сланцевая смола, полученная при термической переработке сланца в газогенераторах, наряду с углеводородами содержит много кислородсодержащих соединений: фенолов, кетонов, сложных эфиров. Это значит, что из сланцевой смолы можно получать такие вещества и продукты, которые из другого сырья получить сложно, а то вовсе нельзя.
Кукерсит используется в основном как энергетическое топливо, в меньших масштабах для получения жидкого топлива и различных химических продуктов. Зола кукерсита пригодна для производства строительных материалов (например, цемента) и для известкования кислых почв.
61

Диктионемовый сланец
В Эстонии есть и другая разновидность сланца – диктионемовый сланец (аргиллит). Залежи диктионемовых сланцев находятся в северной и северо-восточной части Эстонии на площади свыше 11 тыс. км2, и их запасы оценивают в 64 млрд. тонн. Диктионемовые сланцы содержат 10-20% органического вещества, имеют низкую теплоту сгорания (5-7 МДж/кг) и выход смолы 2 – 3,5%. Кроме того, в них высокое содержание пирита FeS2 (2,4 -6,0%), который при горении вызовет загрязнение окружающей среды соединениями серы. Из редких элементов, содержащихся в диктионемовых сланцах, интерес представляют уран, молибден и ванадий, содержание которых в аргиллите в десятки раз превышает их среднее содержание в земной коре. С 1946 по 1952 год аргиллит добывали в Силламяэ как урановое сырьё. В настоящее время диктионемовые сланцы промышленного значения как топливо и как технологическое сырьё не имеют.
2.7.2. Торф
Торф является вторым по значению горючим ископаемым Эстонии. Запасы торфа составляют около 2 млрд. тонн. Торф образуется в результате биохимического разложения болотных растений в условиях повышенной влажности и при недостатке кислорода.
По происхождению торф подразделяют на два вида (рис. 2.32):
хорошо разложившийся торф низинного болота, используется преимущественно как топливо; составляет 85% от общего запаса;
торф верхового болота, используется в сельском хозяйстве; составляет 15% от общего запаса.
Рис. 2.32. Плохо разложившийся торф верхового болота (слева) и хорошо разложившийся торф низинного болота (справа).
Природный торф отличается высокой влажностью – 88-92%. Органическое вещество торфа содержит 50-60% углерода, 5-7% водорода, 30-40% кислорода, 2-3% азота, 0,1-1,5% серы, менее 0,2% фосфора. Содержание минерального вещества в торфе не превышает 35%.
Основными группами органических соединений торфа являются гуминовые вещества, битумы, целлюлоза, водорастворимые и легкогидролизуемые вещества, лигнин. Различные виды торфа дают различный выход этих соединений. Так, содержание битумов в верховом торфе может находиться в пределах 1,2-17,7%, водорастворимых и легкогидролизуемых соединений в пределах 7-63% и резко снижается с увеличением степени разложения. С
62
увеличением степени разложения в торфе растёт содержание гуминовых кислот, которое колеблется в пределах 5-55%.
Распределение запасов торфа в Эстонии неоднородно. Крупнейшие из них находятся в южной части Ида-Вирумаа, Пярнумаа и центральной Эстонии.
Торф применяют в сельском хозяйстве и животноводстве, энергетике, медицине, биохимии.
Использование торфа как топлива обусловлено его составом: большим содержанием углерода, малым содержанием серы, низкой зольностью. Основными недостатками являются относительно низкая калорийность и высокая влажность. С развитием современных технологий сжигания и использования экологически чистых процессов получения энергии использование торфа как топлива оценивается учёными как одно из перспективных направлений в энергетике.
Применяя различные способы термической и химической обработки торфа (например, сухую перегонку, газификацию, экстракцию) можно получить ряд ценных продуктов: торфяной кокс, смолу, активированный уголь, генераторный газ, гуминовые кислоты и др.
Торф может быть использован в качестве адсорбента, поскольку он способен впитывать в себя масла, нефть и нефтепродукты.
Значительная часть торфа используется в сельском хозяйстве для улучшения структуры почв. В торфе содержатся гуминовые кислоты – стимуляторы роста и развития и аминокислоты, необходимые для питания растений. Торф обладает бактерицидными свойствами, полезными для любых видов почв. Внесение торфа активизирует микробиологические процессы в почве и повышает естественное плодородие.
Несмотря на относительно богатые запасы, роль торфа как энергетического сырья невелика. Торф не выдерживает конкуренции с горючим сланцем. Для производства электроэнергии торф не используется, он применяется в качестве бытового топлива, главным образом в виде торфобрикета, а также в сельском хозяйстве как удобрение на полях и подстилка на животноводческих фермах.
2.7.3. Фосфориты
Эстония обладает значительными запасами фосфоритов (по разным оценкам от 3 до 8 млрд. тонн). Из них исследованные запасы, пригодные для промышленной добычи, составляют 300 млн. тонн.
Фосфориты – осадочные породы, основным компонентом которых является фторапатит Ca5(PO4)3F. Эстонские фосфориты относятся к ракушечным фосфоритам. Ракушечные фосфориты состоят преимущественно из раковин морских животных и их обломков, сцементированных кварцевым песком (рис. 2.33). Фосфоритовые руды образуют пластовые залежи, мощность пластов от нескольких десятков см до 1-2 метров. Руды бедные, содержание полезного компонента пятиокиси фосфора P2O5 в фосфоритном пласте составляет от 3-4 до 20%, но они легко обогащаются. Обогащение руд флотационным методом позволяет получать концентрат с содержанием P2O5 до 27-30%. Такой концентрат пригоден для получения фосфорных удобрений.
63

Рис. 2.33. Ракушечные фосфориты
Наиболее крупными являются месторождения Раквере и Тоолсе (рис. 2.34). Раквереский фосфоритоносный пласт залегает на глубине от 40 м на севере и до 200 м на юге.
Рис. 2.34. Фосфоритные месторождения Эстонии.
Впервые в Эстонии фосфориты начали разрабатывать в 1922 году. После Второй мировой войны в Маарду (недалеко от Таллина) был построен химический комбинат, выпускавший фосфоритную муку (молотый фосфорит) и простой суперфосфат. В конце восьмидесятых завод был закрыт. Промышленные запасы месторождения Маарду почти полностью отработаны. Начиная с 1991 года, фосфориты в Эстонии не добывают.
2.7.4. Известняк
Известняк (плитняк) – широко распространённая осадочная порода, образовавшаяся при участии живых организмов в морских бассейнах. Известняк состоит преимущественно из карбоната кальция СаСО3 в форме кристаллов кальцита. Известняк обычно светло-серого цвета, но может быть белым, голубоватым, желтоватым или зеленоватым в зависимости от состава примесей.
64

Рис. 2.35. Добыча технологического известняка в карьере.
Известняки имеют чрезвычайно многообразные области применения. Известняк является строительным камнем. До сегодняшнего дня в Эстонии сохранилось множество строений из плитняка: каменные ограды, надгробия, крепостные стены, жилые дома и промышленные здания. В настоящее время основное количество добываемого известняка идёт на производство щебня.
В Эстонии добывают и т.н. технологический известняк, который служит сырьём для различных производств (рис. 2.35). Основными потребителями технологического известняка являются цементная промышленность и производство извести.
2.7.5. Другие полезные ископаемые
Перечень полезных ископаемых будет неполным, если не упомянуть о запасах глины, песка, гравия, гранита. На севере Эстонии имеются крупные запасы кембрийской синей глины - превосходного материала для производства цемента и различных керамических изделий. Гравий и песок встречаются почти на всей территории республики и используются в строительстве. Особое место среди строительного песка занимает стекольный песок, месторождения которого имеются на юге Эстонии.
65

2.8.РАСХОДНЫЕ КОЭФФИЦИЕНТЫ
Расходным коэффициентом называют отношение количества сырья, материалов, топлива и энергии, затраченных на проведение химико-технологического процесса, к количеству полученного целевого продукта. В общем виде можно записать:
где |
Q – количество затраченного сырья, материалов, топлива, энергии; |
|
B – количество полученного продукта. |
Расходные коэффициенты показывают количество сырья, материалов, топлива и энергии, затраченных на производство единицы продукции. Их выражают в тоннах на тонну (т/т), килограммах на тонну (кг/т), кубических метрах на тонну (м3/т), для энергии - в киловаттчасах на тонну (кВт·ч/т) и т.д.
Различают теоретический и практический расходный коэффициент.
Теоретические расходные коэффициенты рассчитывают на основании стехиометрических соотношений, по которым происходит превращение сырья в целевой продукт.
Для реакции
aA + bB → rR +sS
с целевым продуктом R теоретические расходные коэффициенты реагентов А и В равны:
где МА, МВ, МR – мольные массы веществ А, В и R.
Если сырьё содержит примеси, то
где ωА – массовая доля компонента А в сырье.
Практический расходный коэффициент учитывает производственные потери на всех стадиях процесса, а также побочные реакции, если они имеют место. При расчёте практических расходных коэффициентов учитывают степень превращения сырья 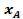 , выход продукта
, выход продукта  , селективность
, селективность 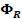 :
:
Практический расходный коэффициент всегда больше теоретического ηпракт > ηтеор. В производственных условиях с целью уменьшения расходных коэффициентов стремятся достичь наиболее высоких значений степени превращения сырья, выхода продукта, селективности процесса.
66

2.8.1. Расчёт расходных коэффициентов
ПРИМЕР 1. Рассчитайте расходные коэффициенты в производстве карбида кальция, содержащего 90% СаС2, если сырьё – антрацит с содержанием углерода 96% и негашёная известь с содержанием СаО 85%.
Решение. Карбид кальция получают по реакции, выражаемой уравнением:
СаО + С → СаС2 + СО
Мольные массы: М(СаС2) = 64 кг/кмоль, М(СаО) = 56 кг/кмоль; М(С) = 12 кг/кмоль.
По условию содержание СаС2 в продукте составляет 90%, таким образом, 1 т продукта содержит
1000кг · 0,90 = 900 кг СаС2.
Рассчитаем расходный коэффициент извести:
Найдём расходный коэффициент антрацита:
Ответ: на получение 1 т карбида кальция, содержащего 90% СаС2, требуется 926,47 кг извести с содержанием СаО 85% и 527,34 кг антрацита с содержанием углерода 96%.
ПРИМЕР 2. Рассчитайте практический расходный коэффициент по природному газу в производстве ацетилена методом окислительного пиролиза, если известно, что объёмная доля метана в природном газе составляет 94%, селективность по ацетилену 34%, а степень конверсии метана 95%. Расчёт вести на 1 т ацетилена.
Решение. Запишем реакцию окислительного пиролиза метана:
Мольная масса М(С2Н2) = 26 кг/кмоль, мольный объём VM = 22,4 м3/кмоль.
Рассчитаем практический расходный коэффициент метана по формуле
Ответ: на получение 1 тонны ацетилена требуется 5675 м3 природного газа.
67
2.9.ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ ПО ТЕМЕ «СЫРЬЕ И ЭНЕРГЕТИЧЕСКИЕ РЕСУРСЫ»
По каким признакам классифицируют сырьё химической промышленности?
Назовите основные виды сырья химической промышленности.
Что такое вторичные материальные ресурсы? Приведите примеры.
Что такое комплексное использование сырья? Приведите примеры.
С какой целью проводится комплексная переработка сырья?
Что такое обогащение сырья и для чего его проводят?
Основные методы обогащения твёрдого сырья. Сущность каждого метода, Аппаратура.
Для каких целей используется в химической промышленности вода?
Что такое оборотная вода? Нарисуйте схему оборотного водоснабжения.
Для каких целей используется в химической промышленности воздух?
Какова роль энергии и топлива в проведении технологических процессов?
Основные виды энергии, применяемые в химической промышленности.
Каковы основные виды энергетических ресурсов? Какие из них являются наиболее перспективными?
Назовите возобновляемые и невозобновляемые энергетические ресурсы.
Что такое вторичные энергетические ресурсы? Как их классифицируют по виду энергии?
Какова роль вторичных энергетических ресурсов в экономии топлива и энергии?
Какие способы применяют для эффективного использования вторичных энергетических ресурсов?
В чём состоит сущность энерготехнологии?
Приведите примеры энерготехнологических схем переработки твёрдых топлив.
Приведите примеры использования в энерготехнологических системах теплоты химических реакций.
Назовите полезные ископаемые Эстонии и области их применения.
Охарактеризуйте эстонские горючие сланцы: состав, калорийность, основные направления применения.
Какие перспективные виды сырья есть на территории Эстонии?
Задача 1. Рассчитайте расходные коэффициенты в производстве метанола, если исходные реагенты: 98%-ный оксид углерода (II) и 96%-ный водород.
68
Задача 2. Рассчитайте расходный коэффициент технического ацетальдегида (99%-ной чистоты) для получения 1 тонны уксусной кислоты, если выход кислоты по альдегиду 93,5%.
Задача 3. Рассчитайте расходный коэффициент природного газа (содержание метана составляет 96%) в объёмных единицах для получения 1000 м3 ацетилена 99%-ной чистоты.
Задача 4. Рассчитайте объём синтез-газа (СО : 2Н2, н.у.), необходимого для получения 1 тонны метанола 98%-ной чистоты, если выход метанола составляет 87%.
Задача 5. Вычислите расходный коэффициент на 1 тонну уксусной кислоты для карбида кальция, содержащего 85% СаС2.
Задача 6.Рассчитайте расход технической серы с массовой долей основного вещества 99,7% на получение 1 тонны серной кислоты концентрацией 93%, если степень использования серы составляет 95%.
Задача 7. Рассчитайте расходный коэффициент серного колчедана FeS2 в производстве серной кислоты. Массовая доля серы в колчедане 45%, степень использования серы 94%.
Задача 8. Рассчитайте объёмный расход аммиака с объёмной долей основного вещества 99,9% для получения 1 тонны азотной кислоты концентрацией 55%. Степень использования сырья 80%.
Задача 9. Рассчитайте объёмный расход азота и водорода для получения 1 тонны аммиака с массовой долей основного вещества 99,6%. Степень превращения сырья в продукт 0,2.
Задача 10.Рассчитайте объёмный расход этан-этиленовой фракции с объёмной долей этилена 60% для получения 1 тонны этилового спирта, если селективность по этанолу составляет 95%.
69
