
- •Химия (органическая химия)
- •050100.62–«Естественнонаучное образование» профиля «Химия»,
- •Оглавление
- •Предисловие
- •Лекция №1. Введение. Предмет органической химии. Основные этапы ее развития
- •Лекция № 2. Классификация и номенклатура органических соединений
- •Классификация органических соединений:
- •Лекция № 3. Химическая связь. Взаимное влияние атомов в органических соединениях
- •Лекция № 4. Изомерия
- •1. Структурная изомерия
- •2. Пространственная изомерия (стереоизомерия)
- •Лекция № 5. Классификация органических реакций и реагентов. Органические кислоты и основания
- •Кислотно-основные взаимодействия
- •Лекция 6.
- •1. Промышленные способы получения:
- •2. Лабораторные способы получения:
- •1. Реакции радикального замещения (sr)
- •2. Окисление
- •5. Дегидрирование:
- •Лекция 7. Непредельные углеводороды
- •1. Алкены
- •2. Геометрическая:
- •1. Реакции электрофильного присоединения(ае)
- •2. Алкадиены
- •2. Геометрическая изомерия:
- •3. Алкины
- •1. Структурная
- •Лекция 8. Арены (ароматические углеводороды)
- •Лекция № 9. Галогенпроизводные углеводородов.
- •2. Реакции отщепления (е).
- •Лекция 10. Спирты. Фенолы
- •1. Предельные одноатомные спирты (алканолы).
- •2. Многоатомные спирты
- •3. Фенолы
- •4. Простые эфиры
- •Лекция № 11. Карбонильные соединения
- •Лекция № 12. Карбоновые кислоты и их производные
- •Лекция № 13. Гетерофункциональные соединения
- •1. Гидроксикислоты
- •2. Оксокислоты
- •Лекция № 14. Углеводы
- •Лекция № 15. Амины
- •Лекция № 16. Аминокислоты. Пептиды
- •Лекция № 17. Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом:
- •Шестичленные азотсодержащие гетероциклы с одним и двумя гетероатомами:
5. Дегидрирование:
![]()
![]()
ЗНАЕТЕ ЛИ ВЫ, ЧТО
-Химик-органик Михаил Иванович Коновалов в 1888 году открыл реакцию нитрования, его имя реакция носит и поныне. По словам Н.Д. Зелинского, М.И. Коновалов «оживил химических мертвецов».
-Академик Н.Н. Семенов (Россия) и С.-Н. Хиншелвуд (Англия) за цикл работ по разработке теории цепных реакций в 1956 году удостоены Нобелевской премии.
-Метан - болотный, рудничный газ, основной компонент природного и нефтяного газа, применяется как высококалорийное топливо и сырье для промышленных синтезов: водорода, ацетилена, нитрометана, синтез-газа и т. д. Составляет основу атмосферы некоторых планет, например, Сатурна, Юпитера.
-Пропан С3Н8 и бутан С4Н10 легкосжижаемые газы, используются в быту в виде баллонного газа. Пропан - автомобильное топливо, бутан - сырье для получения каучуков.
-Парафин - смесь твердых алканов С18-С35, без запаха, цвета, вкуса, жирный на ощупь продукт, получаемый из нефти.
-Вазелин - мазеобразная масса без вкуса и запаха, получаемая расплавлением парафина в минеральном масле.
-Озокерит - горный воск-минерал, состоящий из углеводородов предельного ряда, желтого, зеленого или бурого цвета, применяется в лакокрасочной, парфюмерной промышленности, медицине.
-Загрязнение атмосферы, почвы, водоемов, подземных вод происходит при добыче, транспортировке жидких и газообразных углеводородов, переработке, производстве, применении алканов.
-При галогенировании при температуре более 3000С на 1 квант света образуется несколько тысяч молекул хлорметана.
- Добавление тетраэтилсвинца в бензин снижает способность детонировать (антидетонатор). Для удаления его с внутренних стенок цилиндра добавляют 1,2-дибромэтан, при этом образуется летучий тетрабромид свинца, который удаляется с выхлопными газами, является сильным ядом. Более безопасный, но дорогой, антидетонатор - циклопентадиенилпентакарбонил марганца С5Н5Мп(СО)5, повышает октановое число топлива до135.
Лекция 7. Непредельные углеводороды
План
1. Алкены:
а) гомологический ряд, номенклатура, получение;
б) изомерия, строение;
в) свойства.
2. Алкадиены.
3. Алкины.
К непредельным (ненасыщенным) углеводородам относятся соединения, в составе которых присутствуют кратные углерод-углеродные связи: двойные С=С или тройные С≡ С (алкены, диены, алкины). Термин «непредельные» связан со способностью этих соединений вступать в реакции присоединения с разрывом кратных связей и с образованием соединений предельного (насыщенного) характера.
1. Алкены
Алкены (олефины) – это углеводороды состава СnH2n, содержащие в молекуле одну двойную связь С=С.
Гомологический ряд:
этен - СН2= СН2
пропен - СН3-СН=СН2
бутен-1 - СН3-СН2-СН=СН2
пентен-1 - СН3-СН2-Н2-СН=СН2 и т. д.
Номенклатура. Названия алкенов образуют от названий алканов, заменяя суффикс -ан на -ен.
Простейшие углеводороды имеют не систематические названия с суффиксом -илен: СН2= СН2 - этилен, СН3-СН=СН2 - пропилен.
Названия некоторых радикалов непредельных углеводородов:
СН2=СН - винил, СН2=СН-СН2 - аллил.
По рациональной номенклатуре алкенам дают названия как производным этилена, полученным в результате замещения одного или нескольких атомов водорода на алкильные радикалы. Например,
пропен СН2=СН-СН3 по рациональной номенклатуре будет иметь название - метилэтилен.
Нахождение в природе. Алкены в природе встречаются в составе нефтяного газа и горючих сланцев. Алкенами являются многие природные соединения растительного и животного происхождения, играющие важную биологическую роль. Например, в составе ненасыщенных и полиненасыщенных кислот растительных жиров, феромонов (половые аттрактанты, выделяемые насекомыми для привлечения особей противоположного пола).
Основные области применения алкенов указываются при рассмотрении свойств этих соединений.
Получение алкенов.
1. Крекинг алканов
![]()
2. Дегидрирование алканов
![]()
3. Дегидратация спиртов
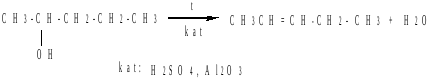
4. Дегидрогалогенирование галогеналканов
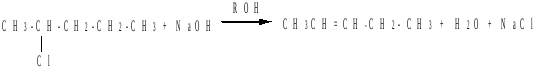
Дегидратация спиртов и дегидрогалогенирование галогеналканов протекают по правилу Зайцева.
5. Дегалогенирование вицинальных дигалогенидов
![]() Изомерия.
1.
Структурная
(на
примере углеводорода состава С5Н10):
Изомерия.
1.
Структурная
(на
примере углеводорода состава С5Н10):
а) различное строение углеродной цепи (для углеводородов с числом атомов углерода ≥ 4) CH3-CH=CH-CH2-CH3 пентен-2 и
![]()
2-метилбутен-2
б) различное расположение кратной связи
CH2=CH-CH2-CH2-CH3 пентен-1
в) межклассовая
Алкены и циклоалканы с одинаковым числом атомов углерода являются
изомерами.
Например, одним из изомеров будет
циклопентан ![]()
