
- •Федеральное государственное бюджетное образовательное учреждение высшего
- •Рецензент:
- •Общие методические указания
- •Лабораторная работа №1 Тема: Правила безопасности при работе в лаборатории общей химии. Элементы техники лабораторных работ. Весы и взвешивание
- •1.1 Техника безопасности при работе в лаборатории общей химии
- •1.2 Помощь при несчастных случаях
- •1.3 Правила обращения с реактивами
- •1.4 Химическая посуда и оборудование. Элементы техники лабораторных работ
- •1.4.1 Весы и взвешивание
- •1.4.2 Правила обращения с весами
- •1.4.3 Взвешивание цинка на аналитических весах
- •1.5 Необходимый уровень подготовки студентов
- •1.6 Вопросы для самоконтроля
- •Лабораторная работа №2 Тема: Определение молярной массы эквивалента цинка
- •2.1 Теоретические пояснения
- •2.2 Методика проведения опыта
- •2.3 Обработка результатов опыта
- •2.4 Примеры решения задач
- •2.5 Необходимый уровень подготовки студентов
- •2.6 Задания для самоконтроля
- •Тема: Основные классы неорганических соединений: оксиды, основания и амфотерные гидроксиды
- •3.1 Теоретические пояснения
- •3.2 Методика проведения опытов
- •3.2.1 Оксиды их получение и свойства
- •3.2.2 Гидроксиды, их получение и свойства
- •Лабораторная работа №4 Тема: Основные классы неорганических соединений: кислоты и соли
- •4.1 Теоретические пояснения
- •4.2 Методика проведения опытов
- •4.2.1 Кислоты, их получение и свойства
- •4.2.2 Соли, их получение и свойства
- •Опыт 5: Получение солей взаимодействием двух солей
- •4.3 Необходимый уровень подготовки студентов
- •4. Уметь писать уравнения реакций, отражающие химические свойства оксидов, гидроксидов, солей. Знать условия протекания до конца реакций ионного обмена
- •4.4 Задания для самоконтроля
- •Лабораторная работа №5 Тема: Кинетика химических реакций
- •5.1 Теоретические пояснения
- •5.2 Методика проведения опытов
- •5.3 Примеры решения задач
- •5.4 Необходимый уровень подготовки студентов
- •5.5 Задания для самоконтроля
- •Лабораторная работа №6 Тема: Химическое равновесие
- •6.1 Теоретические пояснения
- •6.2 Методика проведения опыта
- •6.3 Примеры решения задач
- •6.4 Необходимый уровень подготовки студентов
- •6.5 Задания для самоконтроля
- •Лабораторная работа №7 Тема: Синтез и исследование свойств координационных соединений
- •7.1 Теоретические пояснения
- •7.2 Методика проведения опытов
- •7.3 Необходимый уровень подготовки студентов
- •7.4 Задания для самоконтроля
- •Лабораторная работа №8 Тема: Приготовление растворов заданной концентрации
- •8.1 Теоретические пояснения
- •8.2 Методика проведения опыта
- •8.3 Примеры решения задач
- •8.4 Необходимый уровень подготовки студентов
- •8.5 Задания для самоконтроля
- •Лабораторная работа № 9 Тема: Гидролиз солей
- •9.1 Теоретические пояснения
- •Смещение равновесия в процессах гидролиза солей
- •9.2 Методика проведения опытов
- •8.3 Задания для самоконтроля
- •8.4 Примеры решения задач
- •8.5 Необходимый уровень подготовки студентов
- •Лабораторная работа №10 Тема: Окислительно-восстановительные реакции
- •10.1 Теоретические пояснения
- •10.2 Методика проведения опытов
- •10.3 Необходимый уровень подготовки студентов
- •10.4 Задания для самоконтроля
- •Лабораторная работа №11 Тема: Электрохимический ряд напряжений металлов
- •11.1 Теоретические пояснения
- •11.2 Методика проведения опытов
- •11.4 Задания для самоконтроля
- •Лабораторная работа № 12 Тема:Гальванический элемент
- •12.1 Теоретические пояснения
- •12.2 Методика проведения опыта
- •12.3 Необходимый уровень подготовки студентов
- •12.4 Задания для самоконтроля
- •Лабораторная работа №13 Тема: Изучение свойств азотной, серной и ортофосфорной кислот
- •13.1 Теоретические пояснения
- •13.2 Методика проведения опытов
- •13.3 Необходимый уровень подготовки студентов
- •13.4 Задания для самоконтроля
- •Лабораторная работа №14 Тема: Электролиз солей
- •14.1 Теоретические пояснения
- •14.2 Методика проведения опыта
- •14.3 Необходимый уровень подготовки студентов
- •14.4 Задания для самоконтроля
- •Лабораторная работа № 15 Тема: Коррозия металлов. Защита металлов от коррозии
- •15.1 Теоретические пояснения
- •15.2 Методика проведения опыта
- •Опыт 7: Пассивация алюминия.
- •15.3 Необходимый уровень подготовки студентов
- •15.4 Задания для самоконтроля
- •Лабораторная работа №16 Тема: Криоскопический метод определения молекулярной массы растворенного вещества
- •16.1 Теоретические пояснения
- •16.2 Методика проведения опыта
- •4. Толстостенный стакан
- •6,7. Мешалки
- •8. Крышка
- •16.3 Примеры решения задач
- •16.4 Необходимый уровень подготовки студентов
- •16.5 Задания для самоконтроля
- •Лабораторная работа №17 Тема: Определение кажущейся степени диссоциации хлорида калия криоскопическим методом
- •17.1 Теоретические пояснения
- •17.2 Методика проведения опыта
- •4. Толстостенный стакан
- •6,7. Мешалки
- •8. Крышка
- •17.3 Примеры решения задач
- •17.4 Необходимый уровень подготовки студентов
- •17.5 Задания для самоконтроля
- •Содержание
- •Лукашов Сергей Викторович
- •Методические указания по выполнению лабораторных работ
- •241037. Г. Брянск, пр. Станке Димитрова, 3, редакционно-издательский
8.2 Методика проведения опыта
Опыт 1 : Приготовление раствора с заданной массовой долей соли.
Получите у преподавателя задание и рассчитайте, сколько граммов соли и миллилитров воды потребуется для приготовления раствора заданной концентрации.
Покажите расчеты преподавателю и получите разрешение на проведение опыта.
Взвесьте на технохимических весах нужную массу соли и высыпьте ее в коническую колбу на 250 мл. Отмерьте цилиндром необходимый объем воды и влейте его в колбу с солью. Перемешивайте содержимое колбы до полного растворения соли.
Перелейте в цилиндр приготовленный раствор. При помощи ареометра измерьте его плотность рэксп.. Найдите по табл. 1 плотность раствора ртабл., соответствующую заданной концентрации.
Вычислите относительную ошибку опыта:
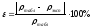
Рассчитайте молярную концентрацию, молярную концентрацию эквивалента, моляльную концентрацию и титр приготовленного раствора. Результаты опыта и расчетов сведите в табл. 2.
Таблица 2 – Результаты опыта 1
|
Формула соли
|
Масса соли, г
|
V раствора,мл
|
Vводы,мл
|
ртабл., г/см3
|
рэксп., г/см3
|
ω% |
СМ
|
CН
|
Сb
|
Т
|
|
|
|
|
|
|
|
|
|
|
|
|
8.3 Примеры решения задач
Пример 1: Массовая доля растворенного вещества.
Определите массовую долю в (%) хлорида калия в растворе, содержащем 0,053 кг KCI в 0,5 л раствора, плотность которого 1063 кг/м3.
Решение:
Массовую долю вещества находим по формуле
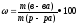 %
%
где m(в-ва), масса вещества, г ;
m(р-ра), масса раствора, г.
Масса раствора равна произведению объема раствора V на его плотность ρ
m=Vρ,
тогда

массовая доля хлорида калия в растворе равна:
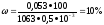 .
.
Пример 2: Молярная концентрация раствора.
Какова масса NaOH, содержащегося в 0,2 л раствора, если молярная концентрация раствора 0,2 моль/л?
Решение:
Молярную концентрацию вещества находят по формуле

где ν(в-ва), количество вещества, моль;
V(р-ра), объем раствора, л.
Количество вещества ν вычисляют по формуле
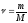
где m, масса вещества, г;
М, молярная масса вещества, г/моль.
Тогда масса NaOH, содержащегося в растворе, равна

8.4 Необходимый уровень подготовки студентов
1. Знать способы выражения концентрации растворов.
2. Уметь определять плотность раствора при помощи ареометра.
3. Уметь пользоваться таблицами зависимости плотности растворов от массовой доли растворенного вещества.
4. Уметь производить расчеты, необходимые для приготовления растворов заданной концентрации, выраженной различными способами.
5. Уметь готовить растворы заданной концентрации из сухого вещества и воды; из более концентрированного раствора и воды.
6. Уметь находить массу или количество растворенного вещества, исходя из концентрации раствора.
7. Уметь производить расчеты, связанные с переходом от одного способа выражения концентрации раствора к другому.
