
- •Химия общая химия
- •Содержание
- •Тема 1. Строение атома. Периодический закон и периодическая система химических элементов д. И. Менделеева
- •Тема 2. Химическая связь
- •Тема 3. Химические реакции
- •5.1 Понятие химической реакции. Признаки классификации химических реакций
- •Тема 4. Основные положения химической кинетики
- •6.2.1 Зависимость скорости реакции от природы реагирующих веществ
- •6.2.2 Зависимость скорости реакции от концентрации реагирующих веществ
- •6.2.3 Зависимость скорости реакции от температуры
- •6.3 Химическое равновесие
- •6.4 Смещение химического равновесия. Принцип Ле-Шателье
- •Тема 5. Ионно-молекулярные реакции
- •7.1 Понятие электролитической диссоциации. Истинные и потенциальные электролиты
- •8.1 Ионные реакции
- •8.3 Буферные растворы
- •9.1 Гидролиз. Степень гидролиза. Константа гидролиза
- •Тема 6. Окислительно-восстановительные реакции
- •10.3 Составление уравнений овр методом электронного баланса
- •11.1 Типичные окислители и восстановители
- •11.2 Поведение в окислительно-восстановительных реакциях некоторых типичных окислителей и восстановителей
- •Тема 7. Основные классы неорганических соединений
- •12.1 Основные классы неорганических соединений
- •1 Взаимодействие оксидов с водой
- •12.6 Физические и химические свойства оснований
- •1 Диссоциация оснований
- •2 Взаимодействие оснований с кислотами
- •1 Диссоциация кислот
- •3 Взаимодействие кислот с основными оксидами:
- •4 Взаимодействие кислот с металлами:
- •5 Взаимодействие кислот с солями
- •1 Взаимодействие простого вещества с водородом
- •2 Взаимодействие оксида с водой
- •3 Взаимодействие кислоты с солью
- •14.2 Физические и химические свойства средних солей
- •14.3 Способы получения средних солей
- •1 Диссоциация солей
1 Диссоциация солей
Кислые соли диссоциируют ступенчато. При диссоциации кислых солей в растворе вначале образуются катионы металла и сложные анионы кислотного остатка, которые в свою очередь подвергаются вторичной диссоциации с образованием протонов водорода.
2 Действие оснований на соли
Так как кислые соли содержат атомы водорода, способные замещаться металлом, то они могут взаимодействовать с основаниями, превращаясь в средние или другие кислые соли с меньшим числом атомов водорода. Например:



3 Разложение солей
Кислые соли обычно бывают термически неустойчивыми. При нагревании они отщепляют воду и превращаются либо в средние соли той же кислоты, либо в средние соли кислоты с большим содержанием ангидрида:
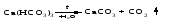

Химические свойства основных солей
1 Диссоциация солей
Основные соли диссоциируют ступенчато. При диссоциации основных солей вначале образуются анионы кислотного остатка и сложные катионы, состоящие из металла и гидроксильной группы. Эти сложные катионы подвергаются вторичной диссоциации с образованием гидроксид-ионов.
2 Действие кислот на соли
Основные соли содержат гидроксогруппы, которые могут участвовать в реакции нейтрализации, поэтому они могут реагировать с кислотами, превращаясь в средние или в другие основные соли с меньшим числом гидроксогрупп. Например:

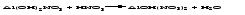
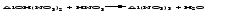
3 Разложение солей
Основные соли при нагревании могут терять воду, образуя оксосоли:
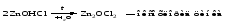
Если основные соли – вещества промежуточные по составу между средними солями и основаниями, то оксосоли – вещества промежуточные по составу между средними солями и оксидами. Как и основные соли, оксосоли при действии кислот можно перевести в средние соли:

14.5 Способы получения кислых и основных солей
Кислые соли можно получить при реакциях:
1) Взаимодействия кислоты с основанием (недостаток основания):
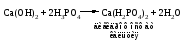
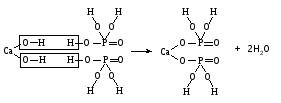
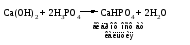
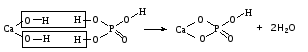
2) Взаимодействия средней соли с кислотой:
а) для реакции можно взять ту же кислоту, которая образует соль:
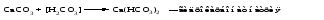
б) может участвовать другая кислота (отличная от кислоты, образовавшей среднюю соль):
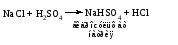
Гидролиз средних солей, образованных слабой многоосновной кислотой и сильным основанием:

Основные соли можно получить при реакциях:
1) Взаимодействия кислоты с основанием (недостаток кислоты):
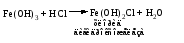
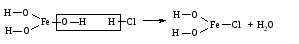
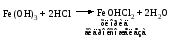

2) Взаимодействия средней соли со щелочью:
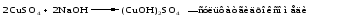
3) Гидролиз средних солей, образованных слабым многокислотным основанием и сильной кислотой:
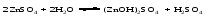
Список использованных источников
1 Глинка, Н.Л. Общая химия. – М. : Интеграл-Прес, 2003. – 728 с.
2 Семенов, И.Н. Химия: учебник для вузов. – СПб.: Химиздат, 2000. – 656 с.
3 Ахметов, Н.С. Общая и неорганическая химия. – М. : Высшая школа, 2006. – 743 с.
Учебное издание
ХИМИЯ
ОБЩАЯ ХИМИЯ
Конспект лекций
Составители:
Картель Наталья Владимировна
Степурко Елена Николаевна
Редактор А.А. Щербакова
Технический редактор Т.В. Багуцкая
Подписано в печать 27.11.2012. Формат 60×84 1/16.
Бумага офсетная. Гарнитура Таймс. Ризография.
Усл. печ. 5,6 л. Уч.-изд. 6,0 л.
Тираж 113 экз. Заказ 150.
Учреждение образования
«Могилевский государственный университет продовольствия».
ЛИ № 02330/630 от 31.01.2012 г.
Пр-т Шмидта, 3, 212027, Могилев.
Отпечатано в учреждении образования
«Могилевский государственный университет продовольствия».
Пр-т Шмидта, 3, 212027, Могилев.
