
- •Методы анализа органических соединений
- •Качественный элементный анализ
- •Отношение органического вещества к нагреванию
- •Открытие углерода и водорода в органическом веществе
- •Открытие азота, серы и галогенов в органическом веществе
- •Проба на серу
- •Проба на азот
- •Проба на галогены
- •Проба Бейльштейна на галогены
- •Качественный функциональный анализ
- •Кратная связь
- •Реакция с бромом
- •Реакция с перманганатом калия
- •Гидроксильная группа
- •Реакция на одноатомные спирты
- •Реакция на фенолы
- •Реакция на гликоли и многоатомные спирты
- •Карбонильная группа
- •Реакция с солянокислым гидроксиламином
- •Реакции с 2,4-динитрофенилгидразином
- •Реакция Толленса на альдегидную группу
- •Реакция с реактивом Фелинга
- •Карбоксильная группа
- •Реакция на кислотность среды
- •Реакция с гидрокарбонатом натрия
- •Качественная реакция -оксикислот с хлоридом железа (III)
- •Качественная реакция бензойной кислоты с хлоридом железа (III)
- •Обнаружение сложного эфира
- •Углеводы
- •Реакция на углеводы с -нафтолом (реакция Молиша)
- •Реакция Троммера на альдозы
- •Реакция Селиванова на кетозы
- •Кислотный гидролиз сахарозы
- •Реакция крахмала с йодом
- •Обнаружение аминогруппы по реакции с 2,4-динитрохлорбензолом
- •Исследование основности аминов
- •Биуретовая реакция на белки
- •Обнаружение жиров
- •Определение непредельных кислот в жирах
- •Определение кислотности жиров
- •Определение перекисного числа жира
- •Задача на идентификацию неизвестного органического вещества
- •Предварительное исследование вещества
- •Качественный элементный анализ
- •Качественный функциональный анализ (открытие функциональных групп)
- •Оформление отчета по лабораторной работе
- •Приложение а
- •Методы анализа органических соединений Лабораторная работа № __
- •Список использованных источников и рекомендуемой литературы
Качественный функциональный анализ
Данные элементного анализа недостаточны для отнесения вещества к определенному классу органических соединений. Эта задача решается с помощью функционального анализа, т.е. определения группировок атомов, обладающих характерной реакционной способностью, – так называемых функциональных групп (например, –ОН, С=О, –СООН, кратных связей и др.).
Для качественных проб на функциональные группы выбирают реакции, при которых происходит изменение окраски или разделение фаз (выпадение осадка, выделение газа). Большое значение при этом имеет избирательность и чувствительность реакций.
Реакций, характерных только для какой-либо одной функциональной группы, известно немного, и для того, чтобы установить, к какому классу соединений относится данное вещество, нужно проделать несколько качественных реакций.
Вывод, сделанный на основании качественных проб и физико-химических данных, обычно подтверждают получением производных.
Производными органических соединений называют вещества, которые получают в результате химических изменений в функциональной группе соединений. Например, R2C=NOH(оксимы) иR2C=NHC6H5(фенилгидразоны) – производные карбонильных соединений;RCONH2(амиды) – производные кислот.
Получение производных – важный этап в анализе органических соединений. Каждому представителю данного класса соединений соответствует производное с определенной температурой плавления. Например, температура плавления амида уксусной кислоты 82С, а амида пропионовой кислоты 79С, амида масляной кислоты 115С. По температуре плавления производного можно сделать заключение о строении соответствующего ему вещества, если оно было ранее описано.
Выбор реактива для получения производного определяется доступностью и устойчивостью реактива, простотой, удобством, скоростью реакции, выходом и четкой температурой плавления производного.
Кратная связь
Реакция с бромом
Подавляющее большинство соединений, содержащих кратную связь (двойную, тройную, их комбинации, за исключением ароматических систем), легко присоединяют бром:
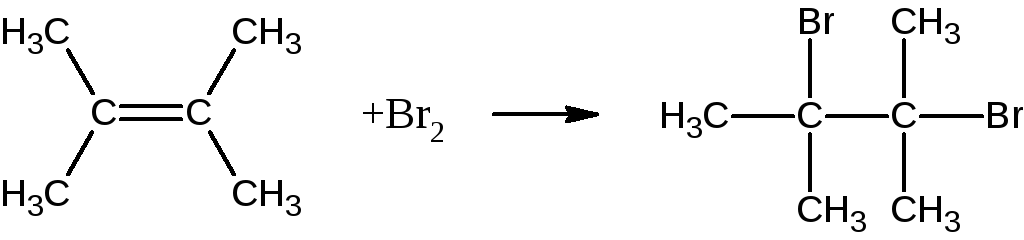
Методика проведения. Реакцию проводят обычно в уксусной кислоте или четыреххлористом углероде. К раствору 0,1г или 0,1см3вещества в 2-3 см3ледяной(100%-ной) уксусной кислоты, помещенному в пробирку, добавляют по каплям, встряхивая, 1%-ный раствор брома вледянойуксусной кислоте. При наличии в веществе кратной связи раствор обесцвечивается. Для реакции удобно использовать олеиновую или итаконовую кислоту, аллиловый спирт, циклогексадиен, алкены.
В отдельных случаях соединения, содержащие водород, легко замещающийся на бром (анилин, фенол, некоторые третичные углеводороды), также обесцвечивают раствор брома. Однако при этом выделяется бромистый водород, который легко определяется с помощью влажной лакмусовой или универсальной индикаторной бумаги:
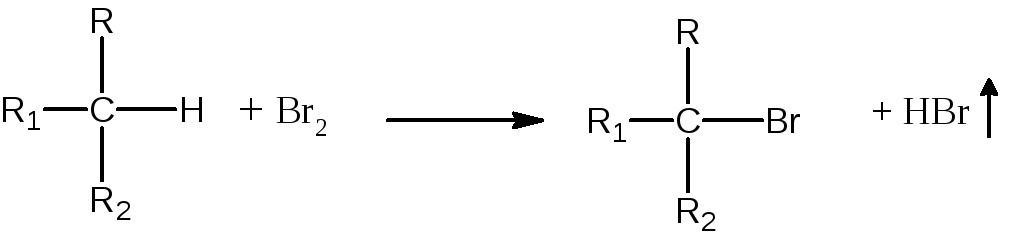
В этом случае реакцию удобнее проводить в ССl4, в котором НВrнерастворим.
Реакция с перманганатом калия
В слабощелочной среде КMnO4окисляет двойную связь в большинстве соединений до гликольной группировки (реакция Вагнера), восстанавливаясь при этом в диоксид марганца:

Наиболее подходящие растворители (если вещество не растворимо в воде) – чистые пиридин и ацетон.
Методика проведения: к раствору 0,1 см3вещества в 2-3 см3или 0,1 г вещества в 2-3 см3растворителя (вода, ацетон или пиридин), помещенному в пробирку, прибавляют, встряхивая, по каплям 0,2%-ный раствор перманганата калия. При наличии в исследуемом веществе кратных связей фиолетовая окраска исчезает и появляется черно-коричневая муть диоксида марганца. Некоторые насыщенные соединения (малоновый эфир, альдегиды, ароматические амины и др.) тоже обесцвечивают перманганат, но в этих случаях реакция протекает значительно медленнее.
