
- •1. Основные положения мкт.
- •2. Кристаллическая решётка. Виды связей между частицами решётки.
- •1. Основные положения мкт.
- •2. Элементы квантовой статистики.
- •1. Основное уравнение мкт идеального газа.
- •2. Фермионы. Распределение Ферми-Дирака.
- •1. Молекулярно-кинетическое толкование термодинамической температуры. Средняя квадратическая скорость.
- •2. Бозоны, распределение Бозе-Эйнштейна.
- •1. Барометрическая формула. Распределение Больцмана.
- •1. Распределение молекул по кинетическим энергиям. Распределение Максвелла-Больцмана.
- •1. Явление переноса. Теплопроводность.
- •2. Элементы зонной теории кристаллов.
- •1. Явление переноса. Внутренне трение (вязкость).
- •2. Деление кристаллов на диэлектрики, металлы и полупроводники.
- •1. Физические основы термодинамики. Термодинамические системы. Равновесные состояния и равновесные процессы.
- •2. Собственная проводимость полупроводников.
- •1. Внутрення энергия идеального газа. Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы.
- •2. Примесные полупроводники.
- •1. Работа и теплота. Первое начало термодинамики.
- •2. P-n переход.
- •1. Работа газа при изменении объёма. Теплоёмкость.
- •2. Понятие о сверхпроводимости.
- •1. Применение первого начала термодинамики к изохорическому и изобарическому процессам.
- •2. Ядерные силы и их свойства.
- •1 P1v1t1 p2v2t1 q1. Цикл Карно.
- •2. Радиоактивность.
- •1. Энтропия в термодинамике.
- •2. Радиоактивность.
- •1. Энтропия с кинетической точки зрения. Третье начало термодинамики.
- •2. Ядерные реакции.
- •1 F f u d d. Силы и потенциальная энергия межмолекулярных взаимодействий.
- •2. Элементарные частицы, взаимопревращаемость частиц.
- •1 F f u d d. Силы и потенциальная энергия межмолекулярных взаимодействий.
- •2. Классификация элементарных частиц.
- •1 F u d. Реальные газы. Уравнение Ван-Дер-Ваальса.
- •2. Античастицы.
- •1 A c d V p p теоретическая. Изотермы Ван-дер-Ваальса.
- •2. Кварки. Проблемы современной физики.
- •1. Уравнение состояния идеального газа.
- •2. Фазы и фазовые переходы.
- •1. Основное уравнение молекулярно-кинетической теории газа.
- •2. Работа и теплота. Первое начало термодинамики.
- •1. Круговые процессы (циклы).
- •2. Закон радиоактивного распада.
- •1 P1v1t1 p2v2t1 q1. Цикл Карно.
- •2. Строение атомных ядер.
1. Явление переноса. Теплопроводность.
Теплопроводность – перенос энергии от одной части тела к другой или от тела к телу при их непосредственном контакте. Переноса вещества при этом не происходит.
![]()
![]() - закон Фурье
- закон Фурье
сорри, но ничего больше в конспекте нет(((
2. Элементы зонной теории кристаллов.
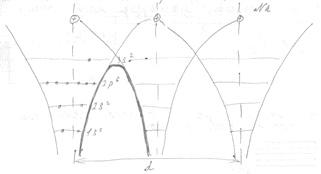
![]()
d>>a
Когда атомы находятся на большом расстоянии друг от друга, т.е. не взаимодействуют, то каждый электрон имеет строго определённое значение энергии и принадлежит данному атому. При «сжатии» расстояние между атомами становится равно параметру кристаллической решётки. Атомы взаимодействуют друг с другом. При образовании кристалла уменьшается высота потенциального барьера между атомами, в результате чего валентные электроны беспепятственно переходят от одного атома к другому, т.е. обобществляются, образуя электронный газ.
При образовании кристалла не только уменьшается потенциальный барьер, но и качественно изменяются энергетические уровни.
![]()
∆t – время нахождения электрона в состоянии с энергией от Е до Е+∆Е.
∆Е определяет ширину энергетической зоны.
Энергетические уровни электронов при образовании кристаллов расщепляются в энергетическую зону.

При «сближении» расширяются лишь уровни валентных электронов, наименее свзанных с ядром и имеющих большую энергию, а также более высокие уровни, которые в основном состоянии атома вообще не заняты.
Уровни внутренних электронов не расщепляются, либо расщепляются слабо.
Энергетическая зона представляет собой систему дискретных уровней. Число уровней в зоне определяется произведением числа атомов в кристалле на кратность энергетического уровня, из которого образуется зона.
Кратность – число электронов, которые могут находиться на этом уровне в соответствии с принципом Паули.
Билет №12.
1. Явление переноса. Внутренне трение (вязкость).
Внутренне трение (вязкость) – возникновение силы трения между двумя слоями жидкости или газа, движущимися с различными скоростями.
Перенос импульса.
![]()
![]()
![]() закон Ньютона
закон Ньютона
2. Деление кристаллов на диэлектрики, металлы и полупроводники.
Степень заполнения энергетических уровней в зоне определяется степенью заполнения соответствующего атомного уровня.

![]()
kT = 10—4 эВ
kT > ∆E полупроводник
kT <∆E диэлектрик.
P.S. Как впёрлось лично мне, типа у металлов (они же проводники) нет запрещённой зоны, поэтому они всегда проводят электрический ток.
Билет №13.
1. Физические основы термодинамики. Термодинамические системы. Равновесные состояния и равновесные процессы.
Внутренняя энергия – кинетическая энергия хаотического движения частиц и энергия их взаимодействия. Она включает в себя энергию электронных оболочек атомов и ионов и внутриядерную энергию.
К внутренней энергии не относится кинетическая энергия движения системы как целого и потенциальная энергия системы во внешнем поле сил.
Фаза – совокупность всех частей т/д системы, обладающих одинаковым химическим составом, находящихся в одинаковом состоянии и ограниченных поверхностями раздела.
Различные вещества, наименьшее количество которых необходимо для образования всех фаз, называются компонентами т/д системы.
Зависимость между числом компонентов (N) и числом фаз определяется правилом Гиббса.
![]()
Переход вещества из одной фазы в другую при изменении внешних условий - фазовый переход.
Существует два вида фазовых переходов:
Ф.п. 1 рода сопровождается скачкообразным изменением внутренней энергии и плотности. Связан с выделением или поглощением энергии (плавление и отвердевание).
Ф.п. 2 рода происходит без изменения плотности и внутренней энергии, и осуществляется без выделения или поглощения теплоты. При нём наблюдается изменение теплоёмкости (из пара- в ферромагнетик; в сверхпроводящее состояние; в сверхтекучесть у гелия).
Если система однокомпонентна, то существует три агрегатных состояния. Условия их существования определяются внешними параметрами – давление и температура. Эта зависимость отображается кривой в координатах Р и Т – диаграммой состояний. Она задаёт зависимость между температурой фазового перехода и давлением.

С – сублимация; П – плавление; И – испарение.
Точка, в которой сходятся кривые равновесия, - тройная точка. Каждое вещество имеет только одну тройную точку.
Для двухфазной системы зависимость давления от температуры задаётся уравнением Клапейрона-Клаузиуса.
![]()
α – скрытая теплота фазового перехода; Т – температура перехода; (V2-V1) – изменение объёма при фазовом переходе
