
- •1. Основные положения мкт.
- •2. Кристаллическая решётка. Виды связей между частицами решётки.
- •1. Основные положения мкт.
- •2. Элементы квантовой статистики.
- •1. Основное уравнение мкт идеального газа.
- •2. Фермионы. Распределение Ферми-Дирака.
- •1. Молекулярно-кинетическое толкование термодинамической температуры. Средняя квадратическая скорость.
- •2. Бозоны, распределение Бозе-Эйнштейна.
- •1. Барометрическая формула. Распределение Больцмана.
- •1. Распределение молекул по кинетическим энергиям. Распределение Максвелла-Больцмана.
- •1. Явление переноса. Теплопроводность.
- •2. Элементы зонной теории кристаллов.
- •1. Явление переноса. Внутренне трение (вязкость).
- •2. Деление кристаллов на диэлектрики, металлы и полупроводники.
- •1. Физические основы термодинамики. Термодинамические системы. Равновесные состояния и равновесные процессы.
- •2. Собственная проводимость полупроводников.
- •1. Внутрення энергия идеального газа. Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы.
- •2. Примесные полупроводники.
- •1. Работа и теплота. Первое начало термодинамики.
- •2. P-n переход.
- •1. Работа газа при изменении объёма. Теплоёмкость.
- •2. Понятие о сверхпроводимости.
- •1. Применение первого начала термодинамики к изохорическому и изобарическому процессам.
- •2. Ядерные силы и их свойства.
- •1 P1v1t1 p2v2t1 q1. Цикл Карно.
- •2. Радиоактивность.
- •1. Энтропия в термодинамике.
- •2. Радиоактивность.
- •1. Энтропия с кинетической точки зрения. Третье начало термодинамики.
- •2. Ядерные реакции.
- •1 F f u d d. Силы и потенциальная энергия межмолекулярных взаимодействий.
- •2. Элементарные частицы, взаимопревращаемость частиц.
- •1 F f u d d. Силы и потенциальная энергия межмолекулярных взаимодействий.
- •2. Классификация элементарных частиц.
- •1 F u d. Реальные газы. Уравнение Ван-Дер-Ваальса.
- •2. Античастицы.
- •1 A c d V p p теоретическая. Изотермы Ван-дер-Ваальса.
- •2. Кварки. Проблемы современной физики.
- •1. Уравнение состояния идеального газа.
- •2. Фазы и фазовые переходы.
- •1. Основное уравнение молекулярно-кинетической теории газа.
- •2. Работа и теплота. Первое начало термодинамики.
- •1. Круговые процессы (циклы).
- •2. Закон радиоактивного распада.
- •1 P1v1t1 p2v2t1 q1. Цикл Карно.
- •2. Строение атомных ядер.
1. Работа и теплота. Первое начало термодинамики.
Певрое начало т/д:
![]() или
или ![]()
Теплота (∆Q), сообщённая системе, расходуется на увеличении внутренней энергии системы (∆U) и на совершение работы над внешними телами (∆A).
Внутренняя энергия – кинетическая энергия хаотического движения частиц и энергия их взаимодействия. Она включает в себя энергию электронных оболочек атомов и ионов и внутриядерную энергию.
К внутренней энергии не относится кинетическая энергия движения системы как целого и потенциальная энергия системы во внешнем поле сил.
Внутренняя энергия есть функция состояния, т.е. величина определяется состоянием системы и не зависит от пути, которым она в это состояние пришла.
Для элементарного изменения состояния:
δQ=dU+δA
dU – полный дифференциал, а δA и δQ – нет, т.к. не являются функцией состояния.
dU – полный дифференциал, т.к. не зависит от пути и круговой ∫dU=0.
![]()
![]()
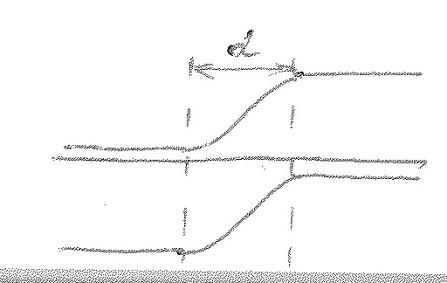
2. P-n переход.
T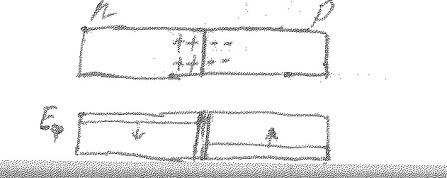
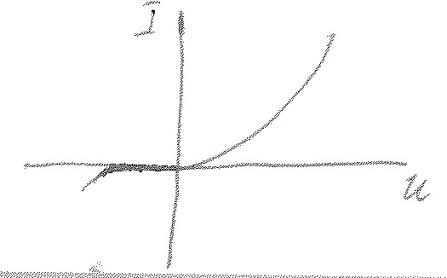
Билет №16.
1. Работа газа при изменении объёма. Теплоёмкость.

∆h
![]()
Теплоёмкость – величина, равная количеству теплоты, которое необходимо, чтобы повысить температуру тела на 1К.
[C] = Дж/К
![]()
![]()
![]()
![]()
2. Понятие о сверхпроводимости.
Электроны в металле кроме отталкивания испытывают притяжение, которое в сверхпроводящем состоянии преобладает над отталкиванием. В результате образуется пара электронов с антипараллельными спинами. Спин пары равен нулю, следовательно, это бозоны, которые накапливаются в основном состоянии (наименьшая энергия) и остаются в нём достаточно долго.
Согласованное движение таких пар – ток проводимости.
Сильное магнитное поле разрушает сверхпроводящее состояние.
спс – сверпроводящее состояние.
При пропускании сильного тока по сверхпроводнику сверхпроводящее состояние разрушается - критический ток. Это связано с действием на сверхпроводящее состояние магнитного поля тока.
Билет №17.
1. Применение первого начала термодинамики к изохорическому и изобарическому процессам.
Изозорический процесс – процесс, происходящий при постоянном объёме (V=const, ∆V=0).
![]()
![]()
![]()
![]() - теплоёмкость при постоянном объёме.
- теплоёмкость при постоянном объёме.
Изобарический процесс – процесс, происходящий при постоянном давлении (P=const, ∆P=0).
![]()
![]()
![]()
![]()
![]() – уравнение Майера.
– уравнение Майера.
2. Строение атомных ядер.
Атомное ядро состоит из протонов и нейтронов.
![]() – протон. q=1,6*10-19
– протон. q=1,6*10-19
![]() – нейтрон. q=0.
– нейтрон. q=0.
mn=1,675*10-27 кг
![]()
![]() – антинейтрино
– антинейтрино
![]()
Z – зарядовое число (количество протонов)
A – массовое число (количество нейтронов + количество протонов)
X – обозначение элемента
Я дра с одинаковыми Z – изотопы.
Я
B

![]()
Плотность ядерного вещества:
![]()
![]()
Билет №18.
1. Применение первого начала термодинамики к изотермическому и адиабатическому процессам.
Изотермический процесс – процесс, происходящий при постоянной температуре (T=const, ∆T=0).
∆Q=∆A
![]()
![]()
А
P
Q1 1
∆Q=0; ∆A=-∆U
∆U+∆A=0
![]()
![]()
V
Q2 2![]()
![]()
![]()
![]() - коэффициент Пуассона
- коэффициент Пуассона
Уравнение адиабаты:
![]()
![]()
![]()
2. Дефект масс и энергия связи ядра.
![]()
![]()
![]() –
дефект масс
–
дефект масс
М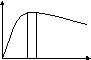 аксимальная
энергия связи достигается у элементов
с номерами 50-60 в таблице Менделеева.
аксимальная
энергия связи достигается у элементов
с номерами 50-60 в таблице Менделеева.
Билет №19.
1. Круговые процессы (циклы).
Процесс, который может быть проведён в обратном направлении через те же состояия, что и при прямом ходе, но в обратной последовательности, называется обратимым.
Обратимыми являются изопроцессы, все остальные процессы необратимы.
Процесс, при котором система после ряда изменений возвращается в исходное состояние, называется круговым(циклом).
Н
P2V2T2
P1V1T1
Если часть Q превращрется в A, то прямой цикл (по часовой стрелке). Цикл, в котором затрачивается механическая работа, - обратный цикл (холодильная машина).
Отношение совершённой в цикле работы к полученной теплоте – коэффициент полезного действия.
![]()
![]()
Отношение отнятого тепла Q2 к работе на приведение машины в действие – холодильный коэффициент.
