
Roytberg_G_E__Strutynskiy_A_V_Serdechno-sosu
.pdf
ишемии. Чаще наблюдается смещение сегмента RS–Т ниже изоэлектрической линии (на 1,0 мм и более), что свидетельствует о возникновении субэндокардиальной ишемии миокарда. У больных с нестабильным течением спонтанной (вариантной) формы стенокардии во время ангинозного приступа, сопровождающегося, как известно, динамической окклюзией КА (выраженным спазмом), можно обнаружить подъем сегмента RS–Т выше изолинии, указывающий на наличие преходящей трансмуральной ишемии миокарда.
Характерно, что в группе больных с НС существенно чаще, чем у больных со стабильным течением заболевания, обнаруживаются суточные колебания сегмента RS–T и преходящие желудочковые аритмии высоких градаций. Особенно неблагоприятным признаком является безболевая ишемия миокарда, не сопровождающаяся возникновением приступа стенокардии. Наличие безболевой ишемии миокарда существенно повышает риск внезапной сердечной смерти и острого ИМ. Прогноз остается неблагоприятным даже в тех случаях, когда под влиянием антиангинальной терапии уменьшается количество спонтанных болевых приступов стенокардии, но число эпизодов безболевой ишемии сохраняется прежним.
 Запомните
Запомните
1.Чем больше частота возникновения у больных НС транзиторных ишемических изменений сегмента RS–T и их продолжительность, тем выше риск развития ИМ и внезапной сердечной смерти.
2.Особенно неблагоприятным признаком у больных НС является наличие безболевой ишемии миокарда, не сопровождающейся приступами стенокардии.
Функциональные нагрузочные тесты. У больных НС с низким риском ИМ и внезапной смерти непосредственно перед выпиской из стационара и не раньше чем через 7–10 дней после приступа ангинозной боли, проводят стресс-тесты (с физической нагрузкой или фармакологические) с целью объективной оценки степени риска заболевания. Главным условием их проведения является отсутствие повторных эпизодов болевой или безболевой (по данным ЭКГ или холтеровского мониторирования) ишемии миокарда в покое. Низкая толерантность к нагрузке и выраженные ишемические изменения ЭКГ во время проведения теста служат показанием для осуществления коронароангиографии и решения вопроса о целесообразности реваскуляризации (см. ниже).
Лабораторные тесты
Биохимический анализ крови у больных НС дает возможность:
оценить активность кардиоспецифических ферментов и других маркеров некроза с целью дифференциальной диагностики НС и острого ИМ;
оценить выраженность и характер нарушений липидного, углеводного и других видов обмена.
Активность кардиоспецифических ферментов (КФК, МВ КФК, АсАТ, ЛДГ, ЛДГ1) при НС в большинстве случаев не отличается от нормы. Лишь изредка при тяжелом течении заболевания на фоне длительной и необратимой ишемии миокарда может произойти некротизация отдельных кардиомиоцитов. В этих случаях наблюдается небольшое повышение активности указанных ферментов, но не более чем на 40% от верхней границы нормы.
В то же время следует иметь в виду, что такое же повышение активности КФК, ЛДГ, МВ КФК и других ферментов может быть и при отсутствии некротизации сердечной мышцы (при различных заболеваниях внутренних органов, повреждении скелетных мышц, после кардиоверсии и т.д.). В этих случаях диагноз уточняется при проведении сцинтиграфии
с 99mТс (технецием пирофосфатом) и при тщательном анализе всей клинической картины заболевания.
Определение современных маркеров некроза (тропонины I и Т) имеет важное значение для выделения группы больных НС с высоким риском ИМ и внезапной смерти. В настоящее время уровень тропонинов в сыворотке крови считается наиболее специфическим
ичувствительным лабораторным тестом для диагностики некроза кардиомиоцитов
идифференциальной диагностики НС и острого ИМ. На рис. 6.11 видно, что у больных с НС
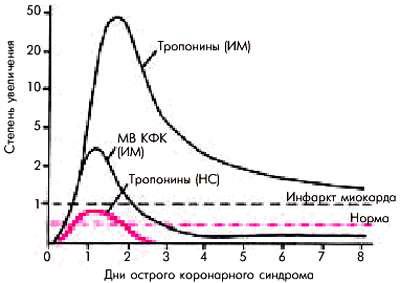
ивысоким риском развития ИМ или внезапной смерти нередко наблюдается небольшое повышение уровня тропонинов, что свидетельствует о наличии у этих пациентов микронекрозов в сердечной мышце и плохом прогнозе заболевания. Повышение уровня тропонинов при классическом ИМ существенно отличается от результатов, полученных у больных НС: амплитуда и продолжительность повышения тропонинов оказываются значительно более выраженными.
Рис. 6.11. Изменение уровня тропонинов при нестабильной стенокардии (кривая красного цвета) и инфаркте миокарда. Для сравнения приведена кривая повышения уровня МВ КФК у больного острым инфарктом миокарда
Нарушения углеводного и инсулинового обмена могут значительно ухудшать ближайший
иотдаленный прогноз НС, так как существенно повышают риск возникновения ИМ
ивнезапной сердечной смерти. Так же, как при стабильной стенокардии напряжения, гиперлипидемия выявляется у значительной части больных НС. Имеется определенная зависимость между уровнем общего ХС, ХС ЛНП и количеством пораженных КА, толерантностью к физической нагрузке и глобальной систолической функцией ЛЖ (Е.П. Кохан с соавт., 2000).
Нарушения в системе гемостаза, закономерно выявляющиеся у больных НС, играют важную роль как в дестабилизации ИБС (в формировании ―осложненной‖ атеросклеротической бляшки), так и в определении исходов НС. Поэтому у каждого больного с НС целесообразно по возможности более тщательно изучить состояние всех трех звеньев этой системы: 1) сосудисто-тромбоцитарного гемостаза; 2) системы коагуляционного гемостаза; 3) системы фибринолиза. С этой целью необходимо определение следующих показателей:

активированное время рекальцификации (АВР); активированное частичное тромбопластиновое время (АЧТВ); фибриноген плазмы; фибринолитическая активность крови; свободный гепарин крови;
адгезивность и агрегация тромбоцитов, агрегация эритроцитов; протромбиновый индекс;
антитромбин III; аутокоагуляционный тест; время свертывания цельной крови; тромбиновое время; показатели вязкости крови; тромбоэластограммы.
Базисные методы определения состояния системы свертывания крови позволяют оценить следующие признаки гиперкоагуляции у больных НС.
1.Укорочение времени свертывания цельной крови (меньше 5 мин).
2.Укорочение времени рекальцификации плазмы (менее 60–120 с при использовании кальция хлорида и менее 50–70 с — при использовании каолина).
3.Уменьшение активированного частичного тромбопластинового времени (АЧТВ) — кефалин-каолиновое время меньше 35–50 с.
4.Увеличение протромбинового индекса более 100% (или уменьшение протромбинового времени).
5.Изменение основных показателей тромбоэластограммы: укорочение времени реакции (R) и времени коагуляции (К) и увеличение максимальной амплитуды (Мa) тромбоэластограммы
(рис. 6.12).
6.Дефицит антитромбина III — важнейшего физиологического антикоагулянта.
7.Повышение адгезии и агрегации тромбоцитов.
8.Увеличение концентрации фибриногена (более 2–4 г/л).
9.Появление в плазме растворенных фибрин-мономерных комплексов с фибриногеном
(РФМК).
10. Повышение продуктов деградации фибрина (ПДФ) — более 0,015 г/л.
Увеличение последних двух показателей — признак усиливающегося свертывания крови, сопровождающегося активацией фибринолитической системы (см. ниже).
В реальной клинической практике бывает достаточно определения времени АЧТВ, которое служит в качестве контрольного теста при лечении больных антитромбиновыми препаратами.
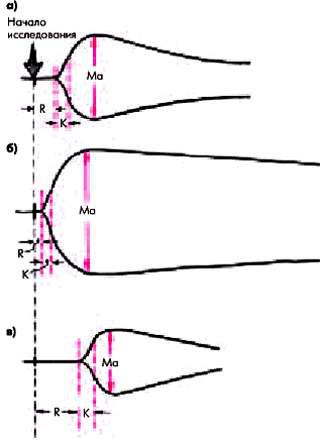
Рис. 6.12. Тромбоэластограмма в норме (а); при гиперкоагуляции (б) и гипокоагуляции (в). Схема
Эхокардиография
Эхокардиографическое исследование у больных НС дает возможность количественно оценить степень систолической и диастолической дисфункции ЛЖ, а также выявить признаки нарушения локальной сократимости, обусловленные как острым ишемическим повреждением кардиомиоцитов, так и наличием у некоторых больных НС постинфарктного кардиосклероза.
Нарушения глобальной систолической функции ЛЖ оцениваются по величине ФВ, степени укорочения переднезаднего размера ЛЖ в систолу (%DS) и другим показателям (КДО, КСО, МО, СИ, размеры ЛП). Прогностическое значение имеет снижение ФВ меньше 40%, которое выявляется более чем у половины больных НС, чаще у пациентов с длительным анамнезом ИБС и больных, перенесших в прошлом ИМ. В то же время даже у относительно молодых пациентов с ВВС примерно в 1/4–1/3 случаев также можно обнаружить снижение систолической функции ЛЖ, обусловленное ишемическим повреждением миокарда. Под влиянием лечения, направленного на восстановление перфузии миокарда, происходит уменьшение признаков систолической дисфункции ЛЖ, что подтверждает ишемический генез снижения сократимости ЛЖ.
Выявление у больных НС локальных нарушений сократимости ЛЖ с помощью двухмерной ЭхоКГ имеет особое диагностическое и прогностическое значение. Как известно, асинергия ЛЖ у больных ИБС может быть обусловлена 4 основными причинами: 1) острым ИМ; 2)
постинфарктным кардиосклерозом; 3) кратковременной преходящей болевой или безболевой ишемией миокарда и 4) постоянно действующей ишемией жизнеспособного миокарда
(гибернирующий миокард), а также существованием так называемого ―оглушенного‖ миокарда.
При остром трансмуральном ИМ с зубцом Q или постинфарктном кардиосклерозе эхокардиографические признаки локальных нарушений сократимости ЛЖ (чаще акинезия или дискинезия) сохраняются длительное время, как правило, в течение всей жизни больного и соответствуют электрокардиографическим маркерам острого или перенесенного ИМ (патологический зубец Q или комплекс QS).
Участки гипокинезии ЛЖ, обнаруживаемые у больных с кратковременной преходящей ишемией миокарда, вызванной очередным приступом стабильной стенокардии или индуцированной функциональным нагрузочным тестом (велоэргометрия, тредмил-тест, фармакологические пробы), как правило, через несколько минут после прекращения нагрузки или купирования приступа стенокардии не выявляются. На этом основана диагностика ИБС с помощью метода стресс-эхокардиографии.
Более чем у половины больных с НС гипокинезия ЛЖ может сохраняться от одного до нескольких дней после купирования болевого приступа, свидетельствуя о более серьезных нарушениях коронарного кровообращения и более глубоком ишемическом повреждении миокарда. Это является важным диагностическим признаком НС, отличающим эту форму ИБС от приступов стабильной стенокардии.
Причиной таких локальных нарушений сократимости ЛЖ, сохраняющихся у больных НС в течение нескольких дней от начала дестабилизации болезни, могут являться дистрофические изменения и даже некрозы кардиомиоцитов в ограниченных участках сердечной мышцы, расположенных в бассейне нарушенного коронарного кровообращения.
Кроме того, следует иметь в виду еще два возможных механизма снижения локальной сократимости ЛЖ, которые особенно часто наблюдаются у больных НС.
1.Феномен гибернирующего (―спящего‖) миокарда, находящегося в условиях хронического снижения коронарной перфузии.
2.Феномен ―оглушения‖, выявляющийся после восстановления исходной перфузии тканей (реперфузии).
Оба феномена были описаны в главе 5. Напомним, что феномен гибернации миокарда (hybernatio, ―спячка‖) заключается в нарушении локальной сократимости ЛЖ, возникающем при выраженном и продолжительном снижении его перфузии и не сопровождающемся иными признаками ишемии. Феномен гибернации является своеобразной формой клеточного анабиоза, обеспечивающего выживаемость кардиомиоцитов в условиях дефицита кислорода. Важно помнить, что гибернирующий миокард реагирует на введение катехоламинов: например, под влиянием малых доз добутамина временно восстанавливается сократимость миокарда, что доказывает его жизнеспособность. Феномен ―оглушенного‖ миокарда (stunning) — это преходящее постишемическое нарушение локальной сократимости ЛЖ, возникающее после восстановления исходного коронарного кровообращения (реперфузии)
и прекращения действия ишемии. Оба феномена очень характерны для больных с ―обострением‖ ИБС, в том числе для пациентов с НС, хотя встречаются и при стабильном течении заболевания.

 Запомните
Запомните
1.Примерно у половины больных НС обнаруживаются эхокардиографические признаки снижения глобальной систолической функции ЛЖ, в частности, уменьшение ФВ ниже 40%.
2.Нарушения локальной сократимости ЛЖ у больных НС, как правило, сохраняются
в течение нескольких дней после ангинозных приступов, свидетельствуя о наличии более значительных нарушений коронарного кровотока и метаболизма кардиомиоцитов.
3. Основной причиной относительно продолжительного снижения локальной сократимости ЛЖ у больных НС являются:
гибернирующий (―спящий‖) миокард, сохранивший свою жизнеспособность в условиях резкого и длительного падения коронарной перфузии за счет уменьшения энерготрат и сократительной функции;
―оглушенный‖ миокард, медленно восстанавливающий энергоресурсы и сократительную функцию после восстановления перфузии сердечной мышцы;
ишемическое повреждение сердечной мышцы в виде очаговой дистрофии миокарда и микронекрозов.
Добавим, что нарушения локальной сократимости в области заднедиафрагмальной стенки ЛЖ свидетельствуют, как правило, о стенозировании (органическом или динамическом) правой коронарной артерии, а соответствующие нарушения переднеперегородочной и верхушечной локализации — об ограничении коронарного кровотока в бассейне ЛКА.
Если у больных НС, несмотря на интенсивную антиангинальную и антитромбоцитарную терапию, нарастают симптомы коронарной недостаточности и сохраняется высокий риск возникновения ИМ и ВCС, должен быть решен вопрос о целесообразности хирургической реваскуляризации зон ишемии. В этих случаях больной должен быть переведен в специализированные кардиохирургические центры, где проводится КАГ и уточняется
характер поражения КА, локализация и распространенность патологического процесса, а также состояние коллатерального кровообращения, после чего решается вопрос о выборе способа реваскуляризации.
Сцинтиграфия миокарда
Сцинтиграфия миокарда с 201Т1, зарегистрированная в покое (без нагрузки), позволяет выявить у части больных НС дефекты накопления радиопрепарата в зонах нарушенной перфузии миокарда и оценить их локализацию и распространенность. Чем меньше времени прошло с момента ангинозного приступа, тем больше шансов обнаружить эти дефекты. Если перфузия миокарда полностью восстановлена, ―холодные‖ зоны локального снижения радиоактивности на сцинтиграммах больше не выявляются. В отличие от этого при остром

ИМ или постинфарктном кардиосклерозе ―холодные‖ зоны резкого снижения или отсутствия радиоактивности обнаруживаются в течение длительного времени.
Таким образом, у части больных НС сцинтиграфия миокарда с 201Т1 позволяет визуализировать зоны локального снижения перфузии миокарда, определить их распространенность и локализацию.
Коронароангиография (КАГ)
Проведение КАГ у больных НС позволяет уточнить локализацию, распространенность и характер поражения коронарного русла, а также оценить выраженность коллатерального кровообращения. Эти данные необходимы, прежде всего, для решения вопроса о
целесообразности проведения чрескожной коронарной ангиопластики и особенно показаны у больных НС с высоким риском возникновения острого ИМ и внезапной сердечной смерти:
больным с повторными эпизодами ишемии миокарда (рецидивы боли или отрицательная динамика сегмента RS–T);
больным с повышенным содержанием в сыворотке крови тропонинов или МВ КФК; пациентам с нестабильной гемодинамикой (артериальная гипотензия или прогрессирующая сердечная недостаточность); больным с угрожающими нарушениями ритма (повторные эпизоды ЖТ или ФЖ); пациентам с ранней постинфарктной стенокардией.
Сужение КА обнаруживают примерно у 85–90% больных НС, из них примерно в 40% случаев на КАГ, зарегистрированных в первые сутки заболевания, можно обнаружить тромбы в КА. Только у 10–15% больных по данным КАГ сужение крупных венечных сосудов является гемодинамически незначимым или артерии остаются интактными, несмотря на наличие у этих пациентов типичных клинических, электрокардиографических и сцинтиграфических признаков локального нарушения перфузии миокарда, характерного для ИБС. В этих последних случаях речь идет, как правило, о динамическом стенозе или о метаболическом синдроме (―синдроме Х‖), в основе которого лежат серьезные нарушения микроциркуляторного сосудистого русла, обусловленные повреждением эндотелия мелких венечных сосудов и их склонностью к спазму и образованию микротромбов.
Почти у 2/3 больных НС выявляется гемодинамически значимый стеноз КА (сужение более 75% просвета КА), а еще у 1/4 — полная окклюзия одной из 3-х КА, в том числе у больных, перенесших в прошлом ИМ.
Однососудистое поражение обнаруживают примерно у 30% больных НС, причем чаще у пациентов относительно молодого возраста с впервые возникшей стенокардией. Двухсосудистое поражение коронарного русла встречается у 25–30% и, наконец, трехсосудистое — еще у 15–20% больных. Атеросклеротическое сужение трех крупных ветвей КА (ПМЖВ, ПКА и ОВ) наблюдается, как правило, у больных, длительно
страдающих ИБС и перенесших ИМ. Независимо от клинического варианта НС чаще всего поражается ПМЖВ ЛКА.
Главным отличием морфологических изменений коронарного русла у больных стабильной и нестабильной стенокардией является наличие у последних ангиографических признаков
―осложненной‖ атеросклеротической бляшки. Так, у большинства больных НС на коронарных ангиограммах можно выявить эксцентрическое (асимметричное) сужение просвета сосуда с неровной зазубренной кромкой (рис. 6.13). Такую неровность поверхности атеросклеротической бляшки объясняют ее разрывом или изъязвлением с формированием

пристеночного тромба, расположенного, как правило, в области этого повреждения. Иногда пристеночный тромб, неполностью закрывающий просвет сосуда, выглядит на коронарограммах как дефект наполнения, который как бы отделен от стенки сосуда.
Рис. 6.13. Фрагмент коронароангиограммы у больного с осложненной атеросклеротической бляшкой ПМЖВ. Асимметричное сужение артерии с неровными контурами обозначено стрелкой
В отличие от этого у больного со стабильной стенокардией в месте сужения КА кромка обычно ровная и незазубренная, что отражает наличие ―неосложненной‖ атеросклеротической бляшки, суживающей просвет КА. Значительно реже, чем при НС, выявляется эксцентрический характер сужения венечного сосуда.
Важное прогностическое значение у больных НС имеет ангиографическая оценка коллатерального кровообращения. Известно, что при хорошо развитой сети коллатеральных сосудов даже полная окклюзия одной КА длительное время может не сопровождаться развитием ИМ. Обычно при значительном и распространенном поражении КА и длительном течении ИБС при КАГ выявляется хорошо развитая сеть коллатералей, тогда как у больных с ―коротким‖ ишемическим анамнезом и стенозом одной КА коллатеральное кровообращение выражено хуже. Последнее обстоятельство имеет особое значение в случаях внезапного тромбоза, сопровождающегося, как правило, возникновением трансмурального некроза сердечной мышцы (например, у сравнительно молодых больных ИБС).
Внекоторых случаях у больных с типичной клинической картиной ИБС при обычном коронароангиографическом исследовании описанные изменения КА не выявлются вообще.
Вэтих случаях, как правило, речь идет о преобладании функциональных нарушений венечных сосудов или поражении более дистально расположенных микрососудов (преартериол и артериол).
Следует заметить, что больным НС присуща повышенная констрикторная активность в области ―осложненной‖ атеросклеротической бляшки, суживающей просвет венечного сосуда. Поэтому на КАГ нередко можно выявить заметную спастическую реакцию стенозированной КА, причем не только у пациентов с вазоспастической (вариантной) стенокардией Принцметала, но и у большинства больных НС.

 Запомните
Запомните
1.У большинства больных НС при КАГ обнаруживают гемодинамически значимое сужение (более 75% просвета) 1–3 КА. Наиболее часто выявляется атеросклеротическое сужение ПМЖВ.
2.У больных НС сужение просвета КА нередко имеет неровную зазубренную кромку, что отражает наличие разрывов, изъязвлений на поверхности атероматозной бляшки, а также формирование пристеночного тромба (осложненная атеросклеротическая бляшка).
3.Некоторые коронароангиографические признаки атеросклеротического поражения КА у больных НС имеют особо неблагоприятное прогностическое значение:
поражение ствола ЛКА;
трехсосудистое поражение КА (ПМЖВ, ПКА, ОВ);
критическое сужение просвета КА более 80–90%;
наличие тромба в КА;
слабое развитие коллатерального кровообращения.
4. Отсутствие у больных с типичной клиникой НС гемодинамически значимого сужения проксимальной КА не исключает наличия ИБС и НС, а лишь подчеркивает необходимость проведения дополнительных тестов с целью выявления повышенной спастической активности венечных сосудов или поражения мелких коронарных сосудов (Х-синдром).
6.3.4. Лечение
Основной целью лечения больных острым коронарным синдромом без стойкого подъема сегмента RS–T, который в дальнейшем трансформируется в НС, является снижение риска возникновения ИМ и внезапной смерти и уменьшение последствий острой распространенной ишемии миокарда ЛЖ (нарушений ритма и проводимости, прогрессирования СН и др.). Согласно рекомендациям Европейского кардиологического общества (2000 г.) и Российским рекомендациям комитета экспертов ВНОК (2001 г.), с этой целью могут использоваться следующие медикаментозные и немедикаментозные воздействия.
1. Антиишемические (антиангинальные) ЛС:

β-адреноблокаторы; нитраты;
блокаторы медленных кальциевых каналов.
2. Антитромбиновые препараты:
гепарины (нефракционированный и низкомолекулярные);] прямые ингибиторы тромбина.
3. Антитромбоцитарные агенты:
аспирин; антагонисты рецепторов к аденозиндифосфату (тиенопиридины);
блокаторы гликопротеиновых IIb/IIIа рецепторов тромбоцитов.
4. Коронарная реваскуляризация:
транслюминальная коронарная ангиопластика; аорто-коронарное шунтирование.
Лечение больных перечисленными способами должно быть начато незамедлительно, как только по клиническим данным и результатам ЭКГ-исследования в покое складывается впечатление о наличии острого коронарного синдрома без стойкого подъема сегмента RS–T (наиболее характерного для НС) и проведена клиническая оценка риска возникновения ИМ и внезапной смерти (см. раздел 6.3.2 и табл. 6.3). При возобновлении приступов болей показан прием нитроглицерина, включая его внутривенное введение, а при необходимости — применение внутривенных инфузий β-адреноблокаторов и наркотических анальгетиков. Методика купирования боли при остром коронарном синдроме подробно описана в разделе 6.4.
Следует подчеркнуть, что при остром коронарном синдроме без стойкого подъема сегмента RS–T, т.е. у подавляющего большинства больных НС, не рекомендуется применение тромболитической терапии, поскольку, увеличивая риск геморрагических осложнений, этот метод лечения не снижает смертность и частоту развития ИМ, а по некоторым данным даже увеличивает их. Совершенно иной подход прослеживается в отношении больных острым коронарным синдромом со стойким подъемом сегмента RS–T или ―новой‖ блокадой ножки пучка Гиса, при котором этот способ лечения является методом выбора (см. раздел 6.4).
β-адреноблокаторы
При отсутствии противопоказаний β-адреноблокаторы рекомендуется назначать всем больным НС. Положительный эффект от применения этих ЛС обусловлен преимущественно их отрицательным инотропным и хронотропным действием. Снижение потребности миокарда в кислороде и урежение сердечных сокращений, вызванное β-адреноблокаторами, обычно сопровождается отчетливым антиишемическим эффектом и примерно на 13% уменьшает риск последующего развития ИМ (подробнее — см. главы 2 и 5).
Поскольку отсутствуют доказательства большей эффективности того или иного β- адреноблокатора в лечении НС, выбор конкретного препарата должен основываться, прежде всего, на учете индивидуальной клинической ситуации: наличии сопутствующих заболеваний (АГ или артериальной гипотонии, сахарного диабета, заболеваний легких и т.д.), имеющихся у больного признаков дисфункции ЛЖ, наличии синусовой тахикардии
