
Roytberg_G_E__Strutynskiy_A_V_Serdechno-sosu
.pdf
Атеросклероз и связанные с ним поражения внутренних органов (ИБС, инфаркт миокарда, нарушения кровообращения мозга, нижних конечностей, органов брюшной полости и т.п.) вышел на первое место как причина заболеваемости, потери трудоспособности, инвалидности и смертности населения большинства экономически развитых стран, опередив в этом отношении онкологические, инфекционные заболевания, травмы и другие болезни. Атеросклероз обусловливает примерно половину всех смертных случаев и около 1/3 летальных исходов у лиц в возрасте 35–65 лет.
Атеросклероз является полиэтиологическим заболеванием, в возникновении и прогрессировании которого имеют значение многие внешние и внутренние факторы,
называемые факторами риска (ФР). В настоящее время известно более 30 факторов, действие которых увеличивает риск возникновения и развития атеросклероза и его осложнений. Наиболее значимыми из них являются следующие.
1. Немодифицируемые (неизменяемые) ФР:
возраст старше 50–60 лет; пол (мужской);
отягощенная наследственность.
2. Модифицируемые (изменяемые):
дислипидемии (повышенное содержание в крови холестерина, триглицеридов и атерогенных липопротеинов и/или снижение содержания антиатерогенных ЛВП); артериальная гипертензия (АГ); курение; ожирение;
нарушения углеводного обмена (гипергликемия, сахарный диабет); гиподинамия; нерациональное питание; гипергомоцистеинемия и др.
Современная концепция ФР атеросклероза и ИБС имеет важное значение для понимания патогенеза этих заболеваний и выработки стратегии и тактики проведения профилактических мероприятий в той или иной популяции. Строго говоря, каждый из перечисленных ФР не является причиной атеросклероза в прямом смысле этого слова, т.е. фактором, без которого невозможно его развитие. ФР следует рассматривать как важные (хотя и необязательные) условия, способствующие его возникновению и прогрессированию. Главным в современной концепции ФР атеросклероза является то, что каждый из них или их сочетание ассоциируется с существенно более высоким риском развития заболевания, а успешная коррекция модифицируемых ФР (уменьшение выраженности или их ликвидация) закономерно сопровождается снижением заболеваемости и частоты осложнений атеросклероза (В.И. Метелица, Р.Г. Оганов).
В настоящее время доказано, что к числу наиболее значимых ФР атеросклероза относятся дислипидемии, АГ, курение, ожирение и сахарный диабет.
4.1.1. Дислипидемии
Нарушения липидного обмена (дислипидемии), в первую очередь повышенное содержание в крови холестерина, триглицеридов и атерогенных липопротеинов (гиперлипидемии, ГЛП)
являются важнейшим фактором риска атеросклероза и патогенетически связанных с ним заболеваний сердечно-сосудистой системы (ИМ, хронических форм ИБС, мозгового инсульта, облитерирующего атеросклероза артерий нижних конечностей и др.). Показано, что концентрация в плазме крови общего холестерина (ХС) или его фракций, тесно коррелирует с заболеваемостью и смертностью от ИБС и других последствий атеросклероза. Самый низкий уровень смертности от ИБС наблюдается при концентрации общего ХС ниже 200 мг/дл (5,2 ммоль/л). При его концентрации в пределах 5,3–6,5 ммоль/л регистрируется умеренное повышение показателей смертности от ИБС. Более высокие концентрации общего ХС (свыше 7,8 ммоль/л) ассоциируются с резким увеличением числа летальных исходов.
На основании этих данных, содержание общего ХС ниже 5,2 ммоль/л считается оптимальным или, точнее, ―желательным‖ уровнем. Уровень общего ХС 5,3–6,5 ммоль/л считается пограничным, от 6,6 до 7,7 ммоль/л — повышенным, а выше 7,8 ммоль/л — высоким. В большинстве западных стран высокий уровень общего ХС встречается примерно у 25 % взрослого населения. Для ХС ЛНП ―желательный‖ уровень составляет менее 130 мг/дл (менее 3,4 ммоль/л), пограничный — 130–159 мг/дл (3,4–4,1 ммоль/л). За
―желательный‖ уровень триглицеридов (ТГ) принимают его значения меньше 1,7 ммоль/л или 130 мг/дл.
Поэтому исчерпывающая характеристика нарушений липидного обмена является обязательным условием эффективной профилактики сердечно-сосудистых заболеваний, определяющих по сути прогноз жизни, трудоспособность и физическую активность в быту большинства людей преклонного возраста во всех экономически развитых странах.
Напомним, что в плазме (сыворотке) крови присутствуют три основных класса липидов: 1) холестерин (ХС) и его эфиры; 2) триглицериды (ТГ) и 3) фосфолипиды (ФЛ). Наибольшее значение в атерогенезе имеют холестерин и триглицериды. Основной транспортной формой липидов являются, как известно, липопротеины (ЛП), в которых ХС, ТГ и ФЛ связаны с белками — апопротеинами.
Все ЛП имеют сходную структуру (рис. 4.1). Они состоят: 1) из центральной части (―ядра‖), содержащей нерастворимые в воде липиды (эфиры ХС, ТГ, жирные кислоты) и 2) из оболочки, состоящей из особых белковых молекул (апопротеинов) и растворимых в воде липидов — неэстерифицированного ХС и ФЛ. Молекулы апопротеинов играют роль своеобразного детергента. Они имеют неполярный гидрофобный участок, который связан с липидами, и полярный гидрофильный участок, расположенный на поверхности сферической частицы ЛП и обращенный к окружающей липопротеин водной среде (плазме
крови). Гидрофильный участок апопротеина образует водорастворимые связи с молекулами воды. Такая структура ЛП определяет их свойство быть частично водорастворимыми, а частично — жирорастворимыми.

Рис. 4.1. Структура липопротеинов (по Mc.Intyre,
Harry, 1991).
Следует подчеркнуть, что апопротеины, входящие в состав оболочки ЛП, играют важную роль не только в транспорте липидов к местам их утилизации, но и во многом определяют весь сложный метаболизм липидов. Так, апопротеины В и Е, входящие в состав оболочки атерогенных ЛП низкой и очень низкой плотности (ЛНП и ЛОНП), распознаются специфическими рецепторами гепатоцитов, которые осуществляют захват и поглощение этих липидных частиц. Апопротеины А-I и С-II, локализующиеся на поверхности ЛВП, ЛОНП и хиломикронов (ХМ), активируют некоторые ключевые ферменты липидного обмена, например липопротеинлипазу, которая гидролизует ТГ хиломикронов, ЛОНП и т.д.
В зависимости от плотности и размеров частиц ЛП различают несколько их классов
(рис. 4.2).
Рис. 4.2. Состав, размер и плотность частиц основных классов липопротеинов. Объяснение в тексте
 Запомните
Запомните
1.Чем выше содержание белка в ЛП и ниже содержание триглицеридов, тем меньше размер частиц ЛП и выше их плотность.
2.Основной транспортной формой триглицеридов являются хиломикроны и ЛПОНП, холестерина — ЛПНП, а фосфолипидов — ЛПВП.
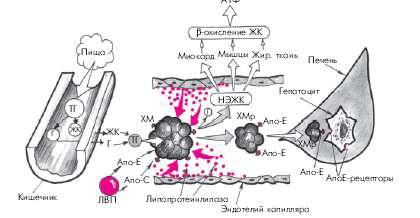
1. Хиломикроны (ХМ) почти полностью (на 80–95%) состоят из ТГ. Они являются основной транспортной формой экзогенных (пищевых) ТГ, перенося их из тонкого кишечника в скелетную мускулатуру, миокард и жировую ткань. В плазме крови они расщепляются под действием липопротеинлипазы до глицерина и свободных неэстерифицированных жирных кислот (НЭЖК). Последние используются в периферических органах в качестве энергетического субстрата (β-окисление жирных
кислот). Остатки ХМ (ремнанты) захватываются гепатоцитами и сравнительно быстро удаляются из кровотока: через несколько часов после приема пищи они уже не обнаруживаются в плазме крови (рис. 4.3).
Рис. 4.3. Упрощенная схема метаболизма хиломикронов.
ТГ — триглицериды; Г — глицерин; ЖК — жирные кислоты; НЭЖК — неэстерифицированные ЖК; ХМ — хиломикроны; ХМр — ремнанты (остатки) ХМ; ЛВП — липопротеины высокой плотности; Апо-Е, Апо-С —
апопротеины; АпоЕ-рецепторы — специфические рецепторы гепатоцитов, «захватывающие» остатки ХМ
2. Липопротеины очень низкой плотности (ЛОНП) — это крупные и ―рыхлые‖ ЛП,
содержащие около 55% ТГ, 19% ХС и только 8% белка (апопротеинов В-100, Е, С-I и С-II). Этот класс ЛП является главной транспортной формой эндогенных ТГ, синтезируемых в печени. Поступая в кровь, ЛОНП также подвергаются воздействию липопротеинлипазы, локализующейся в том числе на поверхности сосудистого эндотелия. В результате
происходит расщепление ТГ на глицерин и НЭЖК, которые также используются жировой тканью, миокардом и скелетной мускулатурой в качестве энергетического субстрата (рис. 4.4). Остатки ЛОНП превращаются в ЛП промежуточной плотности (ЛПП), которые
затем частично удаляются печенью из кровотока, а частично трансформируются в ЛП низкой плотности (ЛНП) и тоже удаляются из кровотока.

Рис. 4.4. Упрощенная схема метаболизма липопротеинов очень низкой плотности (ЛОНП).
ЛПП — липопротеины промежуточной плотности; ЛНП — липопротеины низкой плотности; остальные обозначения те же, что на рис. 4.3. Красными стрелками и кружочками обозначено действие
эндотелиальной липопротеинлипазы
3. Липопротеины низкой плотности (ЛНП) представляют собой более мелкие частицы, которые являются основной транспортной формой ХС. Они содержат около 6% ТГ, максимальное количество ХС (50%) и 22% белка. Примерно 2/3 быстрообменивающегося пула ХС синтезируется в организме, преимущественно в печени (эндогенный ХС), и только 1/3 поступает в организм с пищей (экзогенный ХС). Следует помнить, что ключевым ферментом, определяющим скорость синтеза эндогенного ХС, является гидроксил метил- глутарил-КоА-редуктаза (ГМГ-КоА-редуктаза).
Дальнейший метаболизм ЛНП может происходить двумя путями. Первый из них в норме значительно преобладает и заключается в захвате ЛНП специфическими рецепторами гепатоцитов, имеющими сродство к апопротеинам В и Е, расположенным на поверхности ЛНП (рис. 4.5). Захваченные печеночной клеткой частицы поглощаются гепатоцитами и подвергаются гидролизу с образованием свободного ХС, белка и жирных кислот, которые затем утилизируются клетками.
Рис. 4.5. Упрощенная схема метаболизма липопротеинов низкой плотности (ЛНП).
ХС — холестерин; скэвенджер-рецептор — «рецептор–мусорщик» макрофага, «захватывающий» модифицированные ЛНП; остальные обозначения те же, что на рис. 4.3. Красными кружочками внутри
макрофага и пенистой клетки обозначены внутриклеточные включения холестерина
Характерно, что уровень внутриклеточного свободного ХС является важнейшим фактором, регулирующим активность ГМГ-КоА-редуктазы и скорость синтеза специфических ЛНПрецепторов гепатоцитов, с помощью которых осуществляется захват новых частиц ЛНП, циркулирующих в крови (рис. 4.6). Так, при снижении содержания внутриклеточного ХС возрастает активность ГМГ-КоА-редуктазы и, соответственно, скорость синтеза эндогенного ХС. Одновременно увеличивается синтез ЛНП-рецепторов гепатоцита
и активизируется захват и поглощение ЛНП из кровотока и их внутриклеточный катаболизм. В результате содержание ХС внутри клетки восстанавливается. Наоборот, при высокой внутриклеточной концентрации свободного ХС замедляется синтез эндогенного ХС и ЛНПрецепторов и уровень внутриклеточного ХС постепенно нормализуется. Описанный принцип обратной связи между внутриклеточной концентрацией ХС и скоростью метаболических процессов успешно используется в настоящее время для лечения некоторых нарушений липидного обмена (см. ниже).
Второй путь катаболизма ЛНП — это свободнорадикальное перекисное окисление ЛНП.
Свободные радикалы, образующиеся в организме человека в процессе обмена веществ, являются, как известно, высокоактивными и нестабильными молекулами, которые легко окисляют ХС ЛНП. В результате образуются так называемые модифицированные (окисленные) ЛНП, которые плохо распознаются В- и Е-рецепторами гепатоцитов и поэтому не участвуют в описанном выше нормальном физиологическом пути катаболизма ЛНП. Окисленные ЛП захватываются макрофагами, которые при этом трансформируются в пенистые клетки, входящие в состав атеросклеротических бляшек (см. рис. 4.6). Кроме
того, модифицированные ЛНП вызывают повреждение сосудистого эндотелия, запуская целый каскад патологических реакций со стороны сосудистой стенки. В норме процессы перекисного окисления липидов слабо выражены. Они существенно усиливаются при различных заболеваниях сердечно-сосудистой системы, в частности, при атеросклерозе, являясь одним из важных этиологических факторов, способствующих возникновению и прогрессированию заболевания.

Рис. 4.6. Механизм саморегуляции синтеза эндогенного холестерина и ЛНП-рецепторов в гепатоците (механизм «обратной связи»). Объяснение в тексте
Таким образом, ЛНП относятся к наиболее атерогенной фракции ЛП. Увеличение общего содержания ЛНП, особенно модифицированных окисленных ЛП, ассоциируется с высоким риском возникновения атеросклероза и его осложнений.
4.Липопротеин (a), или ЛП (a), близок по своим физико-химическим свойствам к ЛНП, отличаясь от них наличием в оболочке дополнительного белка — апопротеина a. Последний близок по своим свойствам к плазминогену и поэтому может конкурировать с плазминогеном за места связывания на фибрине и, таким образом, ингибировать
фибринолитическую активность крови. ЛП (a) относятся к числу атерогенных ЛП: их повышенный уровень в крови почти всегда ассоциируется с развитием атеросклероза и ИБС, а также с высоким риском тромботических осложнений.
5.Липопротеины высокой плотности (ЛВП) — самые мелкие и плотные частицы ЛП. Они содержат всего 5% ТГ, 22% ХС и самое большое количество белка (40%) — апопротеинов А- I, А-II и С и относятся к ЛП, обладающим антиатерогенными свойствами. Последние определяются участием ЛВП в катаболизме всех остальных ЛП, поскольку с помощью ЛВП осуществляется обратный транспорт ХС из периферических органов, в том числе из артериальной стенки, с поверхности хиломикронов и ЛОНП, макрофагов и гладкомышечных клеток, в печень, где происходят его утилизация и превращение в желчь. Синтез ―зрелых‖ частиц ЛВП как раз и осуществляется благодаря присоединению свободного ХС от других ЛП и периферических тканей к начальным (насцентным) формам ЛВП, имеющим форму дисков (рис. 4.7). Синтез полноценных сферических ЛВП происходит, таким образом, при обязательном участии ХМ, ЛОНП и ЛНП. Кроме того, ЛВП в процессе метаболизма ХМ, ЛОНП и ЛНП присоединяют к себе их апопротеины А и С, оказывающие влияние на активность многочисленных ферментных систем, участвующих в метаболизме липидов.

Рис. 4.7. Упрощенная схема метаболизма липопротеинов высокой плотности (ЛВП).
ЭХС — эстерифицированный ХС; ЛХАТ — лецитин-холестерин-ацилтрансфераза; остальные обозначения те же, что на предыдущих рисунках
Сама трансформация начальных (насцентных) дискоидных форм ЛВП, синтезированных в печени, в ―зрелые‖ сферические частицы происходит в результате поглощения
споверхности ХМ, ЛОНП и периферических тканей свободного ХС и его эстерификации. Образование эфиров ХС, поглощаемых ЛВП, осуществляется при обязательном участии фермента лецитин-холестерин-ацилтрансферазы (ЛХАТ), присутствующей в начальных дискоидных формах ЛВП. В последующем часть эстерифицированного ХС переносится
сЛВП на остатки (ремнанты) ЛОНП, ХМ и ЛПП, которые захватываются и поглощаются гепатоцитами.
Таким образом, ЛВП как бы защищают сосудистую стенку и другие периферические ткани от избыточного содержания ХС, поддерживая высокую скорость обмена липидов. Снижение содержания ЛВП в плазме крови, наряду с увеличением уровня ЛНП, сопровождается значительным увеличением риска развития атеросклероза и его последствий.
Факторами, способствующими снижению уровня ЛПВП, являются (А.Н. Климов
иН.Г. Никульчева): 1) принадлежность к мужскому полу; 2) ожирение; 3) гипертриглицеридемия; 4) высокое потребление углеводов; 5) диабет у взрослых; 6) курение. Высокий уровень антиатерогенных ЛПВП связывают с принадлежностью к женскому полу, высоким уровнем эстрогенов, высокой физической активностью, снижением массы тела
иумеренным потреблением алкоголя.

 Запомните
Запомните
1.Решающее значение для возникновения и прогрессирования атеросклероза имеет соотношение липопротеинов различных классов: ЛНП, ЛОНП и ЛП (a) обладают отчетливым атерогенным, а ЛВП — антиатерогенным действием. Наиболее высокий риск развития атеросклероза наблюдается у лиц с высоким содержанием ЛНП и ЛОНП и низким
— ЛВП.
2.Повышение уровня ЛНП и ЛП (a) и их атерогенности обусловлены:
нарушением синтеза специфических ЛНП-рецепторов гепатоцитов, что препятствует элиминации ХС печеночными клетками; нарушением структуры и функции апопротеинов, например дефектом апо-В (снижение
возможности захвата ЛНП гепатоцитами) или дефицитом апо-А и апо-СII (уменьшение активности липопротеинлипазы) и т.п.; увеличением синтеза эндогенного ХС;
увеличением количества модифицированных (окисленных) форм ЛНП и ЛП (a), образующихся, например в результате перекисного окисления липидов.
3. Снижение уровня ЛВП ассоциируется с несколькими причинами:
принадлежностью к мужскому полу; преклонным возрастом больных;
наличием сопутствующего ожирения и гипертриглицеридемии; высоким потреблением углеводов и наличием диабета взрослых; курением.
4.1.2. Артериальная гипертензия
Важность повышения АД в качестве ФР ИБС, сердечной недостаточности и цереброваскулярной болезни для мужчин и женщин была показана в ряде эпидемиологических исследований. Это связано прежде всего с высокой
распространенностью АГ среди населения экономически развитых стран (более 20%).
Мета-анализ 9 проспективных исследований выявил наличие тесной связи между уровнем диастолического АД и частотой развития инсульта и ИБС. Так, диастолическое АД 105 мм рт. ст. и выше ассоциируется с увеличением в 4 раза риска ИБС. Важность повышения систолического АД как ФР была показана в исследовании MRFIT. Имеются убедительные данные о влиянии АГ на смертность от ИБС и мозговых инсультов.
Артериальная гипертензия оказывает существенное влияние на скорость прогрессирования атеросклероза. Причем имеет значение как систолическая, так и диастолическая АГ. Следует подчеркнуть, что в последние годы особое значение придается ―мягкой‖ форме АГ с уровнем АД от 140/90 до 159/99 мм рт. ст., что связано прежде всего с высокой частотой выявления именно этой формы заболевания (см. главу 7).
Риск возникновения клинических проявлений атеросклероза у больных с АГ, в целом, примерно в 3–4 раза выше, чем у пациентов без сопутствующей артериальной гипертензии. По-видимому, высокое АД оказывает повреждающее действие на эндотелий артериальных сосудов. Кроме того, известно, что гипертоническая болезнь ассоциируется с нарушением функции эндотелия, которое сопровождается увеличением местной выработки вазоконстрикторных факторов (эндотелин, ангиотензин II и др.) и уменьшением синтеза

простациклина, брадикинина и окиси азота (подробнее см. главу 7). Эти изменения могут иметь решающее значение в повреждении эндотелиальной стенки и пропитывании липидами интимы крупных сосудов.
4.1.3. Курение
По современным представлениям степень риска, связанного с курением сигарет, сопоставима с риском гиперлипидемии и АГ. Вместе с тем значение курения как ФР ИБС особенно велико в связи с широким распространением среди населения этой вредной привычки (около 40–50%). Риск развития сердечно-сосудистых заболеваний у курящих примерно в 2–3 раза выше, чем у некурящих. Как показали современные исследования, курение прежде всего ассоциируется с дисфункцией эндотелия, являющейся пусковым фактором развития и прогрессирования атеросклероза. Кроме того, курение оказывает
обратимое протромботическое влияние, повышая уровень фибриногена в крови и адгезию тромбоцитов, приводит к снижению уровня ЛВП и повышению тонуса сосудистой стенки. Доказано, что прекращение курения может привести к снижению риска обострения ИБС в течение 1 года на 50%.
4.1.4. Ожирение
К числу наиболее значимых и в то же время наиболее легко модифицируемых ФР атеросклероза и ИБС относится ожирение. В настоящее время получены убедительные данные о том, что ожирение является не только независимым ФР сердечно-сосудистых заболеваний, но и одним из звеньев — возможно, пусковым механизмом — других ФР, например АГ, ГЛП, инсулинорезистентности и сахарного диабета. Так, в ряде исследований была выявлена прямая зависимость между смертностью от сердечно-сосудистых заболеваний и массой тела (МТ).
Анализ результатов Фремингемского исследования показал, что на протяжении 26 лет частота сердечно-сосудистых заболеваний в целом, ИБС, ИМ и внезапной сердечной смерти возрастала в зависимости от величины избыточной МТ как у мужчин, так и у женщин. Даже у женщин, индекс массы тела (ИМТ) которых не выходил за пределы общепринятых нормальных значений (меньше 25 кг/м2) и составил 23–25 кг/м2, риск возникновения ИБС на 50% выше, чем у пациенток с ИМТ ниже 21 кг/м2. При увеличении ИМТ до 25,0–29 кг/м2 относительный риск ИБС возрастал в 2 раза, а при ИМТ выше 29 кг/м2 — в 3 раза.
В США больные с ИМТ более 30,0 кг/м2 ежегодно проводят в стационаре на 3 дня дольше, чем пациенты с ИМТ менее 23,0 кг/м2, что соответствует 70 миллионам ―лишних‖ койкодней в год.
Важно подчеркнуть, что повышенный риск сердечно-сосудистых заболеваний характерен не только для ожирения как такового, но и для самого процесса прибавки массы тела. Этот факт был убедительно продемонстрирован во Фремингемском исследовании, показавшем высокую степень корреляции величины прибавки массы тела после 25 лет с риском сердечно-сосудистых заболеваний. Похудание, напротив, уменьшало степень риска.
Во всех современных эпидемиологических исследованиях, посвященных изучению ФР ИБС и атеросклероза, подчеркивается тесная связь, существующая между ожирением и такими ФР как АГ, ГЛП и сахарный диабет. Именно эта взаимосвязь, наряду с независимым влиянием ожирения как такового, играет главную роль в увеличении степени риска сердечно-сосудистых заболеваний у лиц, страдающих избыточной массой тела.
