
immunologia_zachet_1
.pdfапоптогенных иммунодефицитов [Ковальчук Л.В., Чередеев А.Н., 1998].
С другой стороны, проблема усиленной активации иммунной системы становится одной из важнейших в патогенезе многих заболеваний человека, включая ВИЧ-инфекцию, многие воспалительные процессы и другие патологии. Оказалось, что следствие приобретенной гиперактивации иммунной системы — иммунодефицит.
Для исследования пролиферативной активности иммунокомпетентных клеток используют тесты на определение:
•пролиферативной активности лимфоцитов в ответ на митогены: фито-гемагглютинин, конканалин А, ЛПС и др.;
•пролиферативного ответа лимфоцитов на специфические антигены и аллергены.
По пролиферативному ответу лимфоцитов на стимуляцию фитогемаг-глютинином и конканалином А судят о функции Т-клеток; по ответу на стимуляцию ЛПС — о функции В-лимфоцитов, а на стимуляцию митогеном лаконоса — о взаимодействии между Т- и В-клетками.
Для оценки эффекторных функций иммунокомпетентных клеток используют тесты на:
•клеточную цитотоксичность (Т-киллеры, NK-клетки и др.);
•образование иммуноглобулинов в культуре В-лимфоцитов in vitro;
•образование клетками иммунной системы иммуноцитокинов и ответ на них in vitro.
4. Методы оценки Т-звена иммунной системы
Цитотоксические тесты проводят, чтобы оценить способность Т-килле-ров, NK-клеток, макрофагов убивать соответствующие клетки-мишени in vitro.
В настоящее время важное значение придают оценке иммунорегуляторного звена. Хотя до сих пор методы оценки числа и функций регуляторных Т-клеток трудоемки, некоторые из них находят применение в практике клинической иммунологии. Более доступны методы определения:
•соотношения числа CD4+ и CD8+ Т-лимфоцитов;
•соотношения про- и противовоспалительных цитокинов в сыворотке и различных биологических жидкостях;
•количества регуляторных Т-клеток фенотипа CD4+ CD25MHOГО FoxP3+ и их функциональных свойств при совместном культивировании с клетками-мишенями in vitro.
Соотношения числа CD4+ и CD8+ Т-лимфоцитов в периферической крови называют иммунорегуляторным индексом. В норме иммунорегуля-торный индекс составляет 1,6-2,2. В зависимости от природы иммунопа тологии значения этого показателя могут изменяться в сторону снижения (характерно для приобретенных форм иммунодефицитов, в частности для прогрессирующей ВИЧ-инфекции) или повышения (например, при аутоиммунных и других иммунопатологиях). Возможные варианты соотношения иммунорегуляторных клеток были изображены авторами в виде «иммунологического компаса. Наиболее показательно соотношение между ИФН-у и ИЛ-4. При аллергопатологии обычно возрастает уровень ИЛ-4 (продуценты - Т h2-клетки), а при многих воспалительных заболеваниях — ИФН-у (продуценты — Th1-клетки). Изменившееся под влиянием самых разнообразных факторов направление стрелки «иммунологического
компаса» может служить важным показателем вмешательства в иммуно-регуляторные механизмы.
Для определения количества Т- клеток чаще используют метод розеткообразования с эритроцитами барана. Метод основан на родстве рецептора CD2 с белками мембраны эритроцитов барана. При смешивании лимфоцитов с эритроцитами барана образуются фигуры в виде розеток. Количество розеткообразующих клеток (Е- РОК) соответствует количеству Т- лимфоцитов (CD2+ клеток).
Для оценки функциональной активности Тклеточного звена иммунитета используют 4 группы методов.
1.Постановка кожных проб ГЗТ.
2.Стимуляция лимфоцитов in vitro в РБТЛ.
3.Функциональная оценка CD4-лимфоцитов.
4.Функциональная оценка CD8-клеток (киллерных клеток и т.д.).
Для постановки кожных проб используется: очищенный туберкулин (реакция Пирке), паротитный, стрептококковый, столбнячный, дифтерийный Аг, трихофитин, кандидин, стрептокиназа, динитрохлорбензол и др.
Стимуляция лимфоцитов в РБТЛ основана на способности лимфоцитов при определенных условиях превращаться, в увеличенные бластоподобные клетки, активно синтезирующие ДНК.
Для характеристики функции CD4-лимфоцитов мононуклеарные клетки крови инкубируют с поликлональным активатором лимфоцитов митогеном лаконоса и количественно измеряют индуцированную им продукцию иммуноглобулинов. Далее в систему вносят клетки с предполагаемой хелперной способностью и определяют прирост образования иммуноглобулинов.
Для оценки функции CD8-лимфоцитов воспроизводится описанная выше методика, но добавляют в культуру клетки с супрессорной активностью, регистрируя снижение суммарных иммуноглобулинов.
5.Оценка В-клеточной системы иммунитета (гуморального иммунитета)
1.Определение числа В-лимфоцитов (CD20+ или CD19+ ).
2.Определение количества неспецифических иммуноглобулинов (IgA, IgM, IgG, IgE).
3.Определение циркулирующих в крови иммунных комплексов.
4.Определение функциональной активности лимфоцитов с помощью реакции бластной трансформации лимфоцитов (РБТЛ) на В- клеточный митоген.
5.Дополнительные уточняющие методы:
- определение количества специфических иммуноглобулинов (IgA, IgM, IgG, IgE); - определение продукции интерлейкина-6;
- определение секреторного IgA.
6.Возрастные особенности иммунной системы ребенка.
1)Здоровый доношенный новорожденный ребенок имеет физиологическое ИДС.
2)С возрастом изменяется лейкоцитарная формула крови:
-у новорожденных соотношение нФ и лф такое же , как и у взрослых; -к 4-5 суткам соотношение нФ и лф = 45% - первый физиологический перекрест лейкоцитов;
-к моменту рождения сформированы механизмы адаптации (повышено содержание лц – обеспечивает защиту кожи и слизистых);
-среди циркулирующих лф преобладают наивные Т клетки (СD45RA), затем с возрастом возрастает уровень CD45RO Т-лф – клеток памяти;
-с 10 месяца до 2, 5 лет – максимальный физиологический лимфоцитоз (65%), происходит количественное увеличение лимфоидной ткани; -к концу 2 года может развиваться вторичный иммунный ответ;
К 4-5 году - повторное равновесие между лф и нФ – второй физиологический перекрест лейкоцитов; -в последующем происходит инволюция лимфоидной ткани, % лф снижается, нФ возрастает (как у взрослого);
Критические периоды:
I – период новорожденности:
-возрастание пропердина в течение 1 недели; -несовершенство барьеров кожи и слизистых; -ослаблена активация системы комплемента, дефицит С-5; -низкая опсонизирующая способность крови;
-незавершенный фагоцитоз (часто пневмонии); -слабая противовирусная активность (мало интерферонов); -мало NK-клеток(слабая противоопухолевая защита);
-снижена способность к антителообразованию(вирусные, бак. Инфекции); -снижен синтез IgA (снижена защита пищеварительной, дыхательной системы); -высокий уровень IgE(аллергопатологии);
-функционируют материнские IgG;
-функционируют Т-супрессоры(предупреждение аутоагрессии).
II – 3-6 месяцев:
-снижен уровень IgG;
-повышается секреция IgA, но еще недостаточно (ОРВИ, бронхиты , пневмонии); -физиологическая гипоиммуноглобулинемия; -снижен синтез интерферона(ОРВИ); -незавершенный фагоцитоз;
-развивается первичный иммунный ответ с IgM, стойкая иммунная память не формируется.
III-2-3 год:
-Характер первичного иммунного ответа; -дефицит IgG2,IgG4(вирусные инфекции);
-незрелость иммунных процессов в слизистых (инфекции ЛОР-органов); -созревает гуморальный иммунитет.
IV – 4-6 год:
-второй перекрест;
-формирование вторичного иммунного ответа; -IgM - к норме взрослого;
-недостаточность мукозального иммунитета;
-повышение IgE (иммунопатологические заболевания).
V – 12-13 лет:
-снижается масса лимфоидных образований; -у мальчиков – стимуляция секреции андрогенов (ингибирование клеточного иммунитета,
повышение чувствительность к микобактериям туберкулеза), облегчается течение аллергических, аутоиммунных заболеваний.
- у девочек – несовершенство соотношения эстрогенов, прогестеронов, снижение функции Т-супрессоров, утяжеление течения аллергических, аутоиммунных заболеваний.
7. Понятие о болезнях иммунной системы, патогенетическая классификация. Роль субпопуляций лимфоцитов в патогенезе иммунных заболеваний.
Иммунопатология - область иммунологии, изучающая патологические ПОЦССЫ (иммунопатогенез) и заболевания иммунной системы.
Аутоиммунные заболевания – болезни иммунной системы, обусловленные тем, что под влиянием генетических факторов и/или факторов внешней среды, утрачивается толерантность и АГ собственного организма.
Свойства АИЗ:
1)Иммунные процессы
2)Проявление зависит от механизмов:
a.Возможен клеточный ответ с участием ЦТЛ и Th1)
b.Возможен гуморальный ответ (с образованием аутоАГ)
3)Затяжной характер с признаками самоподдержания
4)Проявление АИЗ определяется локализацией аутоАГ в организме
Один из механизмов обеспечения аутоиммунной толерантности – элиминация аутоспецифичных колонов в период дифференцировки клеток в тимусе (стадия двойных позитивных Т-лимфоцитов – отрицательная селекция): важна роль отводится Е-клеткам-регуляторам, который блокируют функцию аутоагрессивных клонов.
В настоящее время выделяют ряд состояний и заболеваний, обусловленных нарушениями иммунной системы:
•заболевания, обусловленные ослаблением функций иммунной системы, — иммунодефициты (первичные и приобретенные, или вторичные);
•заболевания, обусловленные избыточным реагированием иммунной системы, аутоиммунные, аллергические;
•инфекционные заболевания иммунной системы, при котор ых возбудители избирательно
поражают лимфоциты (ВИЧ нфекция, инфекционный мононуклеоз и др.);
•лимфопролиферативные заболевания — опухоли иммунной системы: различные формы лейкоза, лимфогранулематоз, лимфома, лимфосаркома и др.;
•болезни иммунных комплексов;
•трансплантационная болезнь;
•иммунопатология репродуктивной системы;
•другие.
8. Основные типы иммунного повреждения тканей (1,2,3,4). Реакции ГНТ и ГЗТ. Характеристика каждого типа. Механизмы.
Иммунное повреждение тканей (реакции гиперчувствительности). Контакт организма с антигеном приводит не только к развитию защитного иммунного ответа, но и к появлению реакций, повреждающих ткани. Экзогенные антигены содержатся в пыли, пыльце растений, еде, лекарствах, микробах, химических веществах, во многих препаратах крови, используемых в клинической практике. Реакции гиперчувствительности могут быть инициированы взаимодействием антигена с антителом или клеточными иммунными механизмами, иммунные реакции, повреждающие ткани, могут быть связаны не только с экзогенными, но и эндогенными антигенами.
Болезни гиперчувствительности классифицируют на основе вызывающих их иммунологических механизмов. При I типе реакций гиперчувствительности иммунный ответ сопровождается освобождением вазоактивных и спазмогенных веществ. При II типе антитела участвуют в повреждении клеток, делая их восприимчивыми к фагоцитозу или лизису. При III типе реакций гиперчувствительности (иммунокомплексных болезнях) взаимодействие антител с антигенами приводит к образованию иммунных комплексов, активирующих комплемент. Фракции комплемента привлекают нейтрофилы, которые вызывают повреждение тканей. При IV типе реакций гиперчувствительности развивается клеточный иммунный ответ с участием сенсибилизированных лимфоцитов.
Таблица 8.1
Признак |
|
Гиперчувствительность |
|
|
|
|
|
|
|
|
|
|
|
|
|
Немедленного типа |
Замедленного |
типа |
||
|
|
|
|
|
|
|
Клинические проявления |
Анафилаксия, |
сывороточная |
Туберкулез, |
туляремия, |
|
|
|
болезнь, сенная лихорадка, |
бруцеллез, |
реакция |
на |
|
|
|
астма, феномен Артюса |
некоторые |
гаптены, |
|
||
|
|
|
трансплантационные реакции |
|
||
|
|
|
|
|
|
|
Антиген |
Сывороточные и |
другие |
Вирусы,некоторые |
бактерии, |
|
растворимые белки, пыльца |
трансплантационные |
||
|
растений и другие аллергены |
антигены, некоторые гаптены |
||
|
|
|
|
|
Антитела в крови |
Присутствуют |
|
Отсутствуют или |
не играют |
|
|
|
роли |
|
|
|
|
|
|
Сроки проявления |
Несколько минут |
|
Не ранее 6—8 ч |
|
|
|
|
|
|
I тип реакций гиперчувствительности (анафилактический тип, , реагиновый, ГНТ, классическая аллергия) может развиваться местно и быть системным. Системная реакция развивается в ответ на внутривенное введение антигена, к которому организм хозяина предварительно сенсибилизирован. Местные реакции зависят от места проникновения антигена и имеют характер отека кожи (кожная аллергия, крапивница), выделений из носа и конъюнктив (аллергические ринит и конъюнктивит), сенной лихорадки, бронхиальной астмы или аллергического гастроэнтерита (пищевая аллергия).
Реакции гиперчувствительности I типа проходят в своем развитии две фазы. Фаза инициального ответа развивается через 5—30 мин после контакта с аллергеном и характеризуется расширением сосудов, повышением их проницаемости, а также спазмом гладкой мускулатуры или секрецией желез. Поздняя фаза наблюдается через 2—8 ч без дополнительных контактов с антигеном и продолжается несколько дней. Она характеризуется интенсивной инфильтрацией тканей эозинофилами, нейтрофилами, базофилами и моноцитами, а также повреждением эпителиальных клеток слизистых оболочек.
Особенности реакций гиперчувствительности
Развитие I типа гиперчувствительности у человека обеспечивают IgE (схема 8.1) Сенсибилизированные Fc-фрагментом IgE тучные клетки и базофилы активируют компоненты комплемента СЗа и С5а (анафилотоксины). Секрецию тучных клеток стимулируют также цитокины макрофагов (ИЛ-8), некоторые лекарства (кодеин и морфин) и физические воздействия (тепло, холод, солнечный свет). Связывание молекул IgE инициирует дегрануляцию тучных клеток с выбросом первичных медиаторов, а также синтез de novo и выброс вторичных медиаторов, таких как метаболиты арахидоновой кислоты. С этими медиаторами связано появление новых симптомов реакции гиперчувствительности I типа.
Схема 8.
Реакция гиперчувствительности I типа
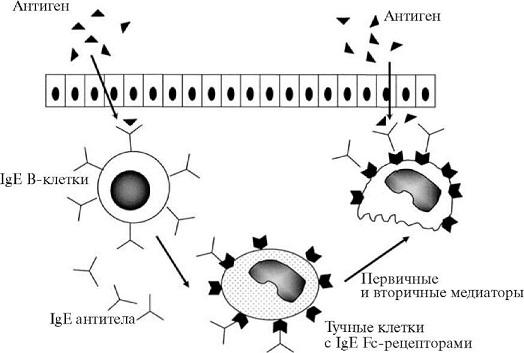
Гистамин и лейкотриены выделяются из сенсибилизированных тучных клеток и базофилов, обеспечивая немедленно развивающиеся реакции, характеризующиеся отеком слизистой оболочки, секрецией слизи, спазмом гладкой мускулатуры. Многие другие медиаторы, представленные фактором активации тромбоцитов (ФАТ), ФНОа, включаются в позднюю фазу ответа, увеличивая количество базофилов, нейтрофилов и эозинофилов. Среди клеток, которые появляются в позднюю фазу реакции, особенно важны эозинофилы. Их набор медиаторов так же обширен, как и в тучных клетках. Кроме того, они продуцируют главный основной белок и эозинофильный катионный белок, которые токсичны для эпителиальных клеток.
II тип реакций гиперчувствительности (цитотоксический, фиксированные антитела). При II типе гиперчувствительности в организме появляются антитела, направленные против компонентов собственных тканей, выступающих в роли антигенов (схема 8.2). Антигенные детерминанты могут быть связаны с плазмолеммой или представляют собой экзогенный антиген, адсорбированный на поверхности клетки. В любом случае, реакция гиперчувствительности возникает как следствие связывания антител с нормальными или поврежденными структурами клетки. Известны три антителозависимых механизма развития реакции этого типа.
Схема 8.
Реакция гиперчувствительности II типа, опосредованная антителами
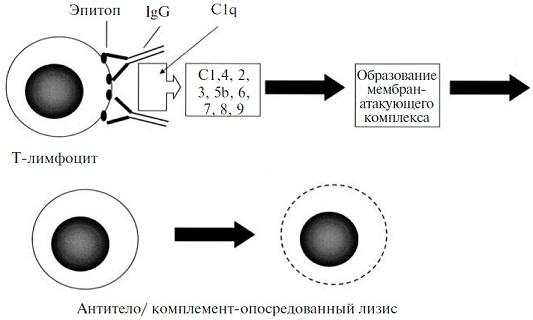
1. Комплемент-зависимые реакции. Существуют два механизма, с помощью которых антитело и комплемент могут вызывать гиперчувствительность II типа: прямой лизис и опсонизация. В первом случае, антитело (IgM или IgG) реагирует с антигеном на поверхности клетки, вызывая активацию системы комплемента. Оно приводит в действие мембранно-атакующий комплекс, который нарушает целостность мембраны. Во втором случае клетки фагоцитируются после фиксации антитела или компонента комплемента СЗb к поверхности клетки (опсонизация).
Клинически такие реакции возникают при: переливании крови несовместимого донора и реакции с антителами хозяина; эритробластозе плода и антигенных различиях между матерью и плодом, когда антитела (IgG) матери проникают сквозь плаценту и вызывают разрушение эритроцитов плода; аутоиммунной гемолитической анемии, агранулоцитозе и тромбоцитопении, когда происходит образование антител против собственных клеток крови, которые затем разрушаются; некоторых реакциях на лекарства, когда образующиеся антитела реагируют с препаратами и формируют комплексы с эритроцитарным антигеном.
2.Антитело-зависимая клеточная цитотоксичностъ не сопровождается фиксацией комплемента, однако вызывает кооперацию лейкоцитов. Клетки-мишени, покрытые IgG-антителами в низких концентрациях, уничтожаются несенсибилизированными клетками, обладающими Fc-рецепторами. Эти клетки связывают клетки-мишени с помощью рецепторов для Fc-фрагмента IgG, а лизис клеток происходит без фагоцитоза. В этом виде цитотоксичности участвуют моноциты, нейтрофильг, эозинофилы и NK. Этот вид цитотоксичности также имеет значение при реакции отторжения трансплантата.
3.Антитело-опосредованная дисфункция клеток. В некоторых случаях антитела, направленные против рецепторов на поверхности клеток, нарушают их функционирование, не вызывая повреждения клеток или развития воспаления. Например, при миастении антитела вступают в реакцию с ацетилхолиновыми рецепторами в двигательных концевых пластинках скелетных мышц, нарушая нервно-мышечную передачу и вызывая, таким образом, мышечную слабость.
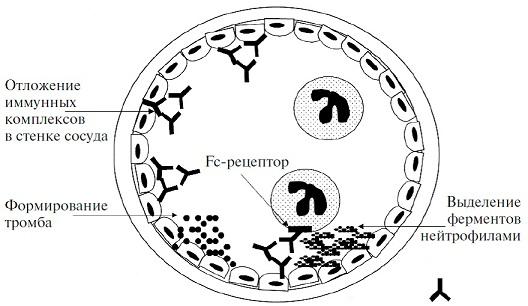
III тип реакций гиперчувствительности (иммунокомплексный – циркулирующие АТ). Развитие реакций гиперчувствительности III типа вызывают комплексы антиген-антитело, образующиеся в результате связывания антигена с антителом в кровеносном русле (циркулирующие иммунные комплексы) или вне сосудов (иммунные комплексы in situ) (схема 8.3). Циркулирующие иммунные комплексы вызывают повреждение при попадании в стенку кровеносных сосудов или в фильтрующие структуры (гломерулярный фильтр в почках). Известны два типа иммунокомплексных повреждений, которые формируются при поступлении в организм экзогенного антигена (чужеродный белок, бактерия, вирус) и при образовании антител против собственных антигенов. Заболевания, обусловленные иммунными комплексами, могут быть генерализованными, если иммунные комплексы образуются в крови и оседают во многих органах, или связанными с отдельными органами, такими как почки (гломерулонефрит), суставы (артрит) или мелкие кровеносные сосуды кожи (местная реакция Артюса) (табл.8.2).
Системная иммунокомплексная болезнь. Однойиз ее разновидностей является острая сывороточная болезнь, возникающая в результате многократного введения больших количеств чужеродной сыворотки крови, используемой для пассивной иммунизации.
Патогенез системной иммунокомплексной болезни складывается из трех фаз: образования в крови комплексов антиген-антитело; осаждения иммунных комплексов в различных тканях; воспалительной реакции (схема 8.4). Первая фаза начинается с попадания антигена в кровь и образования антител. Во вторую фазу эти
Схема 8.
Реакция гиперчувствительности III типа, опосредованная иммунными комплексами
Таблица 8.2
Антигены |
Заболевания, синдромы, реакции |
|
|
|
|
|
иммунного |
|
|
|
|
|
|
комплекса |
|
|
|
|
|
|
|
|
|
|
|
|
|
Источник |
Характер |
|
|
|
|
|
|
|
|
|
|
||
Эндогенные |
Ig-антигеныЯдерныеСпецифи |
Ревматоидный |
артрит, |
проявления |
||
|
ческиеклеточные |
смешанной |
|
криоглобулинемии, |
||
|
|
гипергаммаглобулинемия |
|
Системная |
||
|
|
красная |
волчанкаПараонкологические |
|||
|
|
синдромы, |
аутоиммунные реакции |
|||
|
|
|
|
|
||
Экзогенные |
ЯтрогенныеАнтигеныокружаю |
Сывороточная |
болезнь, |
лекарственная |
||
|
щейсредыАнтигены |
аллергияАллергический |
|
альвеолит, |
||
|
вирусовАнтигены |
герпетический |
дерматитВирусный |
|||
|
бактерийАнтигены |
гепатит, |
геморрагическая |
лихорадка |
||
|
простейшихАнтигены |
ДенгеСтрептококковый гломерулонефрит, |
||||
|
гельминтов |
бактериальный |
|
|
эндокардит, |
|
|
|
лепраМалярия, |
трипаносомозОнкоцеркоз, |
|||
|
|
альвеококкоз, шистозоматоз |
|
|||
|
|
|
|
|||
Неустановленны |
|
Хронический |
гломерулонефрит, |
|||
е |
|
первичные |
васкулиты, |
сухой синдром |
||
|
|
(болезнь) Шегрена |
|
|
||
|
|
|
|
|
|
|
Классификация |
иммунокомплексных болезней |
|
|
|
|
|
комплексы оседают в различных тканях. Дальнейшее течение болезни определяют два фактора: размеры иммунных комплексов и состояние системы мононуклеарных фагоцитов (СМФ). При значительном избытке антител образуются очень крупные комплексы, которые быстро удаляются из кровотока клетками СМФ и относительно безвредны. Наиболее патогенны комплексы мелких и средних размеров, которые образуются при незначительном избытке антител и долгое время остаются в кровотоке. Как только иммунные комплексы оседают в тканях, они инициируют острую воспалительную реакцию. В эту фазу (приблизительно через 10 дней после введения антигена) наблюдаются клинические проявления болезни, такие как лихорадка, крапивница, артралгии, увеличение лимфатических узлов и протеинурия. Вслед за осаждением иммунных комплексов происходит активация системы комплемента с образованием ее биологически активных компонентов. Активация комплемента сопровождается провоспалительными эффектами: выбросом СЗb-опсонина, способствующего фагоцитозу; образованием хемотаксических факторов, вызывающих миграцию полиморфноядерных лейкоцитов и моноцитов (С5); выбросом анафилотоксинов (СЗа и С5а), которые увеличивают проницаемость сосудов и вызывают сокращение гладких мышц; образованием комплекса (С5b-9), вызывающего разрушение клеточных мембран и цитолиз.
Схема 8.
Патогенез иммунокомплексной болезни
