
immunologia_zachet_1
.pdf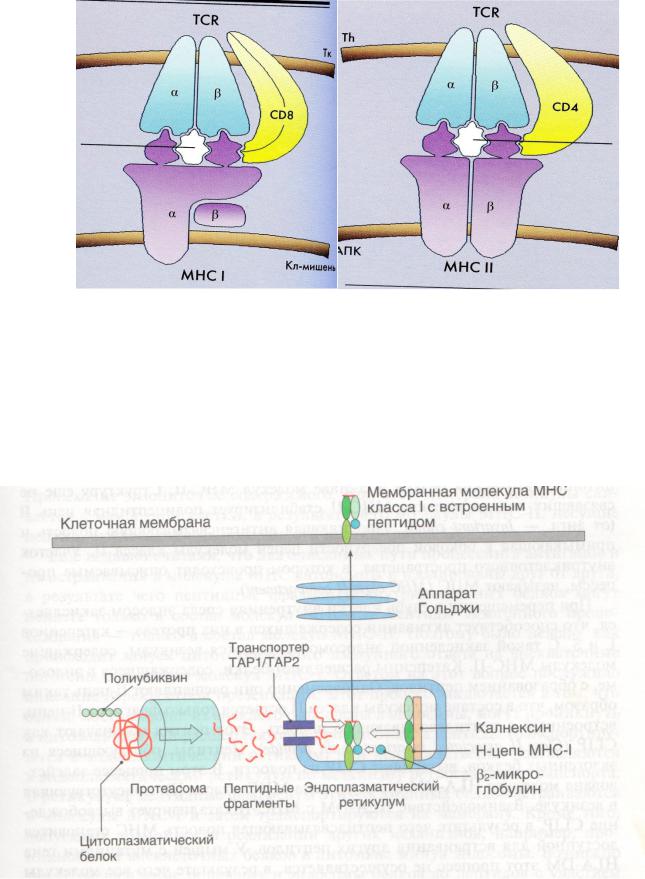
Феномен двойного распознавания - одновременное взаимодействие (распознавание) T-клеточного рецептора (TCR) с антигенным пептидом и молекулой MHC. TCR распознает комплекс АГ+MHC.
Презентация АГ
5 тема
1.. Рецепторы и маркеры лимфоцитов.
На поверхности Т- и В-лимфоцитов, как и других клеток, имеются многочисленные рецепторы - к отдельным белкам системы комплемента, регуляторам иммунной системы, к гормонам, и т.п.. Огромное значение имеют лимфоцитарные рецепторы к антигенам, с помощью которых клетка распознает антигены. Эти рецепторы синтезируются самими лимфоцитами.
Рецепторы к антигену, которые содержатся на поверхности В- лимфоцитов, имеют структуру, близкую к структуре рассмотренных нами выше иммуноглобулинов всех пяти классов, рецепторы имеют мономерную структуру, способны ассоциироваться с мембраной, их количество на поверхности клетки достигает 50-100 тыс. На поверхности индивидуальной клетки содержатся рецепторы одного класса иммуноглобулина и только к одному, редко - двум антигенам. В связи с этим количество клонов В-лимфоцитов (как и Т- лимфоцитов) очень велико и приближается к 1х105. Кроме рецепторов к антигену на поверхности В-лимфоцитов содержатся рецепторы к Fc-фрагменту IgG, к фракции С3 комплемента. Рецепторы Т-лимфоцитов также имеют иммуноглобулиновую природу, но их количество на поверхности клетки значительно меньше Антитела и иммуноглобулиновые рецепторы содержат активный центр, в котором происходит процесс присоединения антигена или гаптена. Активный центр можно считать антидетерминантой, она в пространстве комплементарна антигенной детерминанте, в результате чего происходит реакция антигенантитело. Во время реакции ковалентные, т.е.прочные связи не образуются АГ+АТ АГ-АТ. Возникают слабые физико-химические связи - водородные, гидрофобные, заряд-зарядные. Этих слабых связей много и потому комплекс АГАТ довольно стабильный. Реакция слабо экзотермическая. Равновесие реакции сдвинуто резко вправо. Диссоциацию
комплекса АГ-АТ можно вызвать лишь значительным
изменением рН
2. Стволовы́е кле́тки —
недифференцированные (незрелые) клетки, имеющиеся во всех многоклеточных организмах. Стволовые клетки способны самообновляться, образуя новые стволовые клетки, делиться посредством митоза и дифференцироваться в специализированные клетки, то есть превращаться в клетки различных органов и тканей.
Клетка-предшественник
(син. клетка стволовая) - общее название клеток кроветворной ткани, относящихся к начальному этапу развития клеток крови.
клетка-предшественник коммитированная - клетка кроветворной ткани, дифференцирующаяся только в определенном направлении; К.-л. к. являются родоначальными клетками ростков кроветворения.
клетка-хозяин - клетка, несущая вирус
Зрелые клетки – характеризуются максимальным развитием всех структур клетки, расцветом функциональной активности, они
уже не способны к делению.
3. ДИФФЕРЕНЦИРОВКА T-ЛИМФОЦИТОВ
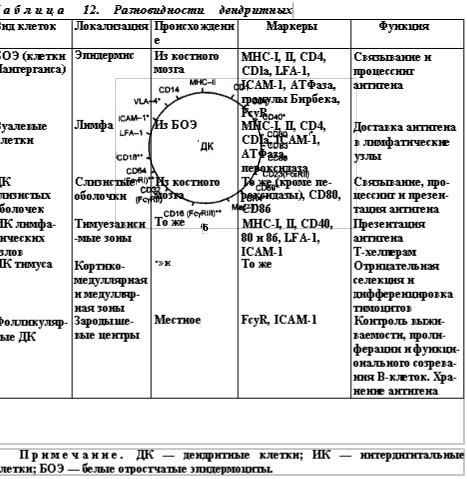
В основе выделения этапов развития Т-лимфоцитов лежит состояние рецепторных V-генов и экспрессии TCR, а также корецепторов и других мембранных молекул. Схема дифференцировки Т-лимфоцитов аналогична приведённой выше схеме развития В-лимфоцитов Приведены ключевые характеристики фенотипа и ростовых факторов развивающихся Т-клеток. Принятые обозначения стадий развития Т-клеток определяются экспрессией корецепторов: DN (от Double-Negative, CD4CD8) - двойные отрицательные, DP (от Double-Positive, CD4+CD8+) - двойные положительные, SP (от Single-Positive, CD4+CD8- и CD4CD8+) - одинарно положительные. Деление DNтимоцитов на стадии DN1, DN2, DN3 и DN4 основывается на характере
Развитие Т-лимфоцитов
экспрессии молекул CD44 и CD25. Другие условные обозначения: SCF (от Stem Cell Factor) - фактор стволовых клеток, lo (low; метка индекса) - низкий уровень экспрессии. Стадии реаранжировки: D-J - предварительный этап, соединение сегментов D и J (только в генах β- и δ-цепей TCR, см. рис. 6-2), V-DJ - завершающий этап, соединение зародышевого V-гена с объединённым сегментом DJ.
• Тимоциты дифференцируются из общей клетки-предшественника, которая ещё вне тимуса экспрессирует такие мембранные маркёры, как CD7, CD2, CD34 и цитоплазматическую форму CD3.
•Коммитированные к дифференцировке в T-лимфоциты клеткипредшественники мигрируют из костного мозга в субкапсулярную зону коры тимуса, где примерно в течение одной недели медленно пролиферируют. На тимоцитах появляются новые мембранные молекулы CD44 и CD25.
•Затем клетки перемещаются вглубь коры тимуса, молекулы CD44 и CD25 исчезают с их мембраны. В этой стадии начинается перестройка генов β-, γ- и δ-цепей TCR. Если гены γ- и δ-цепей успевают продуктивно, т.е. без сдвига рамки считывания, перестроиться раньше, чем гены β-цепи, то лимфоцит дифференцируется далее как γδT. В противном случае происходит экспрессия β-цепи на мембране в комплексе с pTα (инвариантной суррогатной цепью, заменяющей на этом этапе настоящую α-цепь) и CD3. Это служит
сигналом к прекращению перестройки генов γ- и δ-цепей. Клетки начинают пролиферировать и экспрессировать одновременно CD4 и CD8 - дважды позитивные тимоциты. При этом накапливается масса клеток с уже готовой β-цепью, но с ещё не перестроенными генами α-цепи, что вносит свой вклад в разнообразие αβ-гетеродимеров.
•На следующем этапе клетки перестают делиться и начинают перестраивать Vα-гены, причём несколько раз в течение 3-4 сут. Перестройка генов α-цепи приводит к необратимой делеции δ-локуса, расположенного между сегментами генов α-цепи.
•Происходят экспрессия TCR с каждым новым вариантом α-цепи и отбор (селекция) тимоцитов по силе связывания с комплексом MHC-пептид на мембранах эпителиальных клеток тимуса.
-Позитивная селекция: погибают тимоциты, не связавшие ни одного из доступных комплексов MHC-пептид. В результате позитивной селекции в тимусе погибает около 90% тимоцитов.
-Негативная селекция уничтожает клоны тимоцитов, связывающих комплексы MHC-пептид со слишком высокой аффинностью. Негативная селекция элиминирует от 10 до 70% клеток, прошедших позитивную селекцию.
-Тимоциты, связавшие какой-либо из комплексов MHC-пептид с правильной, т.е. средней по силе, аффинностью, получают сигнал к
выживанию и продолжают дифференцировку.
• На короткое время с мембраны тимоцитов исчезают обе корецепторные молекулы, а затем экспрессируется одна из них: тимоциты, распознавшие пептид в комплексе с MHC-I, экспрессируют корецептор CD8, а с MHC-II - корецептор CD4. Соответственно на периферию выходят (в соотношении около 2:1) T-лимфоциты двух типов: CD8+ и CD4+, функции которых в предстоящих иммунных ответах различны.
-CD8+ T-клетки играют роль цитотоксических T-лимфоцитов (ЦТЛ) - они распознают и непосредственно убивают клетки, модифицированные вирусом, опухолевые и другие «изменённые» клетки
-CD4+ T-клетки. Функциональная специализация CD4+
T-лимфоцитов более разнообразна. Значительная часть CD4+ T-лимфоцитов в процессе развития иммунного ответа становится T-хелперами (помощниками), взаимодействующими с В-лимфоцитами, Т-лимфоцитами и другими клетками
4.Основные этапы формирования TCR и субпопуляций T/T в тимусе
Определены основные этапы развития Т-лимфоцитов в тимусе
(Т-клеточный иммунопоэз) в соответствии с генетически обусловленной программой и в отсутствие антигенной стимуляции:
• формирование клоноспецифичных антигенраспознающих рецепторов, способных распознавать антигенные пептиды в комплексе с аутологичными молекулами HLA; • выбраковка Т-клеток, специфичных к аутоантигенам; • экспрессия корецепторных молекул CD4 или CD8 с формированием субпопуляций Т-хелперов и ЦТЛ, а также естественных (природных) регуляторных Т-клеток (Treg).
Дифференцировка в тимусе сопровождается сменой поверхностных маркеров Т-лимфоцитов. На рис. 3-12 представлена схема основных этапов дифференцировки Т-клеток. Она включает следующие стадии: • миграцию предшественников Т-клеток из костного мозга; • перегруппировку генов TCR и формирование полноценного рецептора; • положительную и отрицательную селекцию Т-клеток; • формирование зрелых субпопуляций CD4+ и CD8+ Т-лимфоцитов; • эмиграцию зрелых Т-клеток из тимуса.
5.Роль стромальных элементов,эпителиальных и дендритных клеток,гуморальных факторов тимуса в дифференцировки T -лимфоцитов.
Тимус, как и костный мозг, является центральным, или первичным орга-ном лимфоидной ткани. В составе тимуса имеются несколько долек, каждая из которых представлена эпителиальными клетками, дендритными клетками, макрофагами, лимфоцитами и другими клетками. Эпителиальные клетки ти-муса синтезируют такие пептидные гормоны, как тимолин, тимозины, тимо-поэтин. Крупные эпителиальные клетки коркового вещества выполняют роль «клеток-кормилиц» для лимфоцитов. Эпителиальные клетки коркового ве-щества имеют разветвленные отростки с большим

количеством молекул главного комплекса гистосовместимости. В то же время на поверхности от-ростков эпителиальных клеток мозгового вещества тимуса представлены мо-лекулы главного комплекса гистосовместимости классов II и I
6.Ar-независимый этап дифференцировки B-лимфоцитов
Процесс дифференцировки В-лимфоцитов начинается в конце эмбрионального и начальных этапах постнатального периодов, идет в два этапа: антигениезависимый и антигензависимый.
На первом этапе образуются различные по антигенной специфичности клоны клеток, каждый из которых детерминирован к иммунному ответу на строго определенный, специфический для данного клона В-лимфоцитов антиген. Сначала в эмбриональной печени, а затем в костном мозге (центральный орган дифференцировки В-лимфоцитов) из единого предшественника В-клеток под влиянием костномозгового гормоноподобного пептида происходит образование В-лимфоцитов: предшественники В-клеток —> Пре-В-клетка —> Вo-клетка —> В1-клетка —> Вm-клетка —> Вg-клетка. Пре-В-лимфоциты
и Вo-лимфоциты еще не способны к иммунному ответу, В-лимфоциты уже заселяют В-зависимые зоны периферических органов иммунной системы и способны отвечать пролиферацией на поликлональные митогены, способны к иммунному ответу, но только на тимуснезависимые антигены с образованием сывороточных lgM
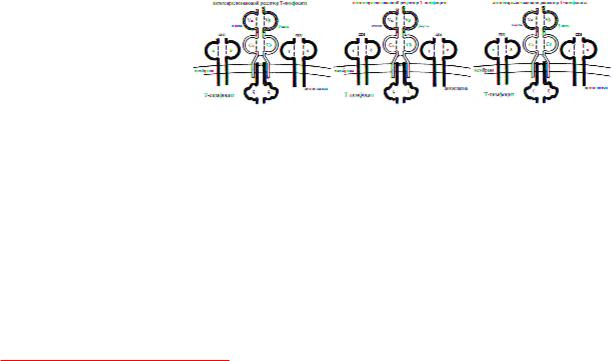
1. Антигенпредставляющие (презентирующие) клетки (АПК), захватывающие
антигены, перерабатывающие их и представляющие соответствующие антигенные детерминанты другим иммунокомпетентным клеткам, (к АПК относятся дендритные, и макрофаги, В—лимфоциты, клетки Лангерганса и кератиноциты кожи, эндотелиальные клетки сосудов и гломерул почек, β-клетки поджелудочной железы)
Функция этих типов клеток - представление ( презентация ) антигенных пептидов в комплексе с
молекулами MHC , т.е. придание проникшему антигену иммуностимулирующих свойств. Т-лимфоциты могут распознавать такие комплексы при помощи Т-клеточных рецепторов(англ. TCR). Антигенпредставляющие клетки процессируют антиген и представляют его Т-клеткам.
Макрофаги, дендритные клетки и В-лимфоциты называют профессиональными АПК, так как они более мобильны, активны и выполняют основной объем функций представления антигенов.
Большинство АПК образуется в костном мозге , хотя их гемопоэтический предшественник остается пока неизвестным.
Мембраные маркеры дендритных клеток
+ B-лимфоциты, которые несут на своей поверхности (как В-клеточный рецептор) и
секретируют специфичные антитела, а также могут захватывать антиген, связавшийся с В-клеточным рецептором,
процессировать его и представлять в комплексе с молекулами главного комплекса гистосовместимости II
класса. По отношению к другим видам антигенов В-лимфоциты неактивны как АПК
2. Макрофаги
Все начинается в костном мозге, где из делящихся стволовых клеток образуется клетка под названием монобласт. Стадии
дифференцировки: монобласт - промоноцит - моноцит крови - тканевой макрофаг. ) Макрофаги - долгоживущие клетки с хорошо развитыми митохондриями и шероховатым эндоплазматическим ретикулумом .
Виды макрофагов:
Макрофаги – тканевые фагоциты, и в разных типах тканей нередко живут свои собственные виды этих клеток. Вот несколько примеров их разновидностей, в зависимости от локализации.
1. Альвеолярные макрофаги – находятся в стенках альвеол легких, очищают вдыхаемый воздух от различных загрязняющих и вредоносных частиц.
