
PosobieTEOR.OSN.ORG.KHIM
.pdf
т.к. алкоксикарбонильная группа старшая. Поскольку в главную цепь вошло шесть атомов углерода и связи одинарные, основой для названия эфира будет название алкана с тем же числом атомов углерода - гексан. Перед названием ос-
новы приставками укажем наличие радикалов и ладших функциональных групп
(двух метильных радикалов и карбонильной группы) и цифрами – их положение в главной цепи. Для карбоновых кислот и их производных характерно окончание
–овая и слово кислота, которые в случае производных используется в родитель-
ном падеже. Тип производного (эфир) и название радикала, образующего это производное (метил) указываем перед названием кислоты, причем к названию радикала добавляем окончание –овый. Получаем:
метиловый эфир 2,5 - диметил - 3 -оксогексановой кислоты
4)
|
|
|
|
|
|
|
CH |
|
|
|
CH |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
2 |
|
3 2 |
|
1 |
O |
|||||||
7 |
|
6 |
5 |
|
|
4 |
3 |
|
|
||||||||||
CH3 |
|
|
CH |
|
CH2 |
|
CH |
|
|
CH |
|
|
C |
|
C |
H |
|||
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
||||||||||||
|
|
OH |
|
|
|
|
|
|
|
|
|
|
Br |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
В данном случае старшей функциональной группой будет альдегидная, ее название обозначается суффиксом –аль. Выбираем главную цепь, содержащую альдегидную группу, и нумеруем ее, начиная с атома углерода альдегидной группы, т.к. она старшая. Так как в главную цепь входит семь атомов углерода и двойная связь, то корень будет гепт- , суффикс -ен, после которого цифрой ука-
зываем положение двойной связи. Перед названием основы перечислим назва-
ния заместителей и младших функциональных групп и укажем их положение в главной цепи. Получаем:
2 - бром - 6 - гидрокси - 4 - этилгептен - 2 - аль
аль
11

II. Напишите структурные формулы следующих органических соединений:
1)Глутаминовая кислота, применяемая для лечения центральной нерв-
ной системы, по номенклатуре ИЮПАК имеет название 2 – аминопентан-
диовая кислота. Напишите структурную формулу данной кислоты.
1.Основой для названия данной кислоты является название предельного углеводорода «пентан», следовательно, главная цепь содержит 5 ато-
мов углерода и не содержит кратных связей:
1 |
2 |
3 |
4 |
5 |
||||
C |
|
C |
|
C |
|
C |
|
C |
|
|
|
|
|||||
2.Окончание «-диовая» и слово «кислота» означает наличие двух карбок-
сильных групп:
O |
1 |
2 |
3 |
4 |
5 |
O |
||||
HO |
C |
|
C |
|
C |
|
C |
|
C |
OH |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||
3.Приставка «амино-» свидетельствует о наличии группы NH2-, а цифра
«2» перед ней – о том, что эта группа находится у второго атома угле-
рода:
O |
1 |
2 |
3 |
4 |
5 |
O |
|||||
HO |
C |
|
C |
|
C |
|
C |
|
C |
OH |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
NH2 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
||||
4.Допишем недостающие атомы водорода, чтобы атомы углерода были четырехвалентными и получим окончательную формулу глутаминовой ислоты:
O |
1 |
2 |
|
3 |
|
4 |
|
5 |
O |
||
HO |
C |
|
|
CH |
|
CH2 |
|
CH2 |
|
C |
OH |
|
|
|
|
||||||||
|
|
|
|||||||||
|
|
NH2 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||
2) Напишите формулу 2-метил-3-оксобутановой кислоты.
1.Основой для названия данной кислоты является название предельного углеводорода «бутан», следовательно, главная цепь содержит 4 атома углерода и не содержит кратных связей:
12

1 |
2 |
3 |
4 |
|||
C |
|
C |
|
C |
|
C |
|
|
|
||||
2.Окончание «-овая» и слово «кислота» означает наличие карбоксиль-
ной группы:
O 1 2 3 4
 C C C C
C C C C
HO
3.Приставки «2-метил-» и «3-оксо-» означают, что у второго атома уг-
лерода находится метильный радикал, а у третьего - карбонильная группа:
O |
CH |
3 3 4 |
1 2 |
 C C C C
C C C C
HO O
4.Допишем недостающие атомы водорода, чтобы атомы углерода были четырехвалентными и получим окончательную формулу 2-метил-3-
оксобутановой кислоты:
O 1 |
CH |
3 |
|
|
|
||
|
2 |
3 |
4 |
||||
C |
|
CH |
|
C |
|
CH3 |
|
|
|
|
|||||
HO |
O |
|
Упражнения для самостоятельной работы студентов
1.Определите, имеются ли ошибки в названиях нижеприведенных со-
единений:
а) 4 – метил – 4 - оксипентанон -2
CH3
CH3 C CH2 C CH3
CH3 O
б) 2 – хлор – 3 – метил –6 – этилгексановая кислота
13

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
CH3 |
|
|
CH |
|
|
CH |
|
CH2 |
|
CH2 |
|
|
CH |
|
C |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
OH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
CH3 |
|
|
CH3 |
|
CH2 |
||||||
|
|
|
|
|
|
||||||||||
в) 6 – метил- 3 - этил –2 –оксогептандиол - 4,8.
|
|
|
|
|
|
|
CH2 |
|
|
CH3 |
||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||
CH3 |
|
C |
|
CH |
|
|
CH2 |
|
|
CH |
|
CH2 |
|
CH2 |
|
OH |
||||
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
CH3 |
|||||||||
2.Напишите структурные формулы следующих соединений:
а) 5-амино-7-гидрокси-4-метилгептановая кислота;
б) 2-нитро-4-этилпентандиовая кислота;
в) 3-гидрокси-3-карбоксипентандиовая кислота;
г) 3,5-дихлорциклогексанол-1;
д) 2,4-диоксогексановая кислота;
ж) 2-амино-3-меркаптопропановая кислота;
з) 4-метилпентен-3-аль;
и) 2,3,4,5,6-пентагидроксигексаналь;
к) этиловый эфир бутен-2-овой кислоты;
л) хлорангидрид 3,3-дихлорпропановой кислоты.
3.Назовите по номенклатуре ИЮПАК следующие соединения:
а)
|
|
|
|
|
OH |
O |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH |
|
CH |
|
CH2 |
|
C |
OH |
|
|
|
|
|
||||||||
|
|
||||||||||
|
|
NO2 |
|||||||||
|
|
|
|||||||||
б)
O |
|
|
NH2 |
OH |
|
|
O |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
HO |
C |
|
C |
|
|
CH2 |
|
CH |
|
CH2 |
|
CH |
|
CH2 |
|
C |
||||
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
CH |
|
|
CH3 |
|
|
|
|
|
NH2 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
||||||
в)
14

O |
|
|
|
H3C |
|
|
|
CH |
|
|
CH2 |
|
|
CH3 |
|||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
C |
|
CH2 |
|
C |
|
|
C |
|
|
CH2 |
|
|
CH3 |
|||||
|
|
|
|||||||||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
г)
HO CH2 C CH CH CH CH2 OH
O OH OH OH
д)
O
CH2 CH C 
NH2 OH
Рекомендуемая литература:
1.Биоорганическая химия. Учебник. /Тюкавкина Н.А., Бауков Ю.И., С.Э. Зурабян. – М: ГЭОТАР-Медиа, 2012. – 416 стр., ил.
Глава 1, стр. 13-28
2.Биоорганическая химия: руководство к практическим занятиям: учеб. Пособие для студентов мед. Вузов / по ред. Н.А. Тюкавкина – М.: ГЭОТАР-
Медиа, 2010. – 168 с.
3.Химия: учебник.-2-ое изд., испр. и доп./С.А. Пузаков – М: ГЭОТАР - Ме-
диа, 2006.-640 стр.
Глава 5, стр. 57-58
15
2.ПРОСТРАНСТВЕННАЯ ИЗОМЕРИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ПОЛИ-, ГЕТЕРОФУНКЦИОНАЛЬНЫХ И ВЫСОКОМОЛЕКУЛЯРНЫХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Цель занятия: сформировать у студентов представление о пространствен-
ном строении органических соединений и его взаимосвязи со свойствами (в
том числе и биологическими).
Студент должен знать:
-сущность явления изомерии;
-виды структурной и пространственной изомерии;
-сущность явления оптической изомерии;
-особенности строения и различия в свойствах структурных изомеров,
таутомеров, энантиомеров и диастереомеров.
Студент должен уметь:
-определять вид структурной и пространственной изомерии;
-определять асимметрический атом в соединении;
-определять число и природу пространственных изомеров;
-определять конфигурацию стереоизомеров по D,L-системе
Изомерия – явление, характерное почти исключительно для органиче-
ских соединений. Сущность этого явления заключается в существовании изоме-
ров.
Изомеры – это вещества, имеющие одинаковый количественный и
качественный состав, но разное строение и, как следствие, разные свойства.
Существует два типа изомерии – структурная и пространственная.
16
2.1. Структурная изомерия
Структурная изомерия – вид изомерии, при котором изомеры разли-
чаются химическим строением (то есть порядком или последовательностью соединения атомов в молекуле).
Структурная изомерия делится на следующие виды:
1. Изомерия углеродного скелета – изомеры различаются порядком со-
единения атомов углерода в углеродной цепи.
CH3 |
|
CH2 |
|
CH2 |
|
CH3 |
CH3 |
|
|
CH |
|
CH3 |
|
|
|
|
|
||||||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
CH3 |
|||
|
|
Бутан |
Изобутан |
|||||||||
2. Изомерия положения кратной связи – двойная или тройная связь в изо-
мерах находится у различных атомов углерода.
CH2 |
|
CH |
|
CH2 |
|
CH3 |
CH3 |
|
CH |
|
CH |
|
CH3 |
|
|
||||||||||||
|
|
|
|
|
|||||||||
|
|
||||||||||||
|
|
Бутен-1 |
|
|
Бутен-2 |
||||||||
3. Изомерия положения функциональной группы – функциональная группа находится у различных атомов углерода.
CH |
|
CH |
|
CH |
|
OH |
CH3 |
|
|
CH |
|
CH3 |
|
|
|
|
|
||||||||
|
|
|
||||||||||
3 |
2 |
2 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
Пропанол-1 |
Пропанол-2 |
|||||||||
4. Изомерия числа и природы заместителей – изомеры принадлежат одно-
му классу органических соединений, но различаются числом и характером за-
местителей, связанных с функциональной группой.
CH3 |
|
CH2 |
|
NH |
|
CH3 |
CH3 |
|
N |
|
CH3 |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
CH3 |
|||
|
Метилэтиламин |
Триметиламин |
||||||||||
17

5. Межклассовая изомерия – изомеры принадлежат к разным классам ор-
ганических соединений.
|
|
|
O |
|
|
|
|
|
|
CH2 |
|
C |
CH3 |
|
CH2 |
|
NO2 |
|
|
|
|
|||||
|
|
|||||||
NH2 |
OH |
|
|
|
|
|
||
|
|
|
|
|
|
|||
Аминоуксусная кислота |
|
Нитроэтан |
||||||
7. Таутомерия.
Таутомерия – вид изомерии, при котором изомеры самопроизвольно переходят друг в друга и находятся в состоянии химического равновесия.
HO CH2 |
O |
OH |
|
H |
H |
||
|
|||
H |
|
H |
|
OH |
|
OH |
H |
C O |
||||
|
|
|
|
|
|
H |
|
C |
|
OH |
|
|
|
||||
|
|
|
|
|
|
H |
|
C |
|
OH |
|
|
|
||||
|
|
|
|
|
|
H |
|
C |
|
OH |
|
|
|
||||
CH2 OH
HO CH2 |
O |
H |
|
H |
H |
||
|
|||
H |
|
OH |
|
OH |
|
OH |
α-D-рибоза |
Открытая форма рибозы |
β-D-рибоза |
2.2. Пространственная изомерия (стереоизомерия)
Пространственная изомерия – вид изомерии, при котором изомеры различаются расположением частей молекулы в пространстве относитель-
но какого-либо структурного фрагмента молекулы при одинаковом составе и химическом строении.
Разновидностями пространственной изомерии являются оптическая изоме-
рия и геометрическая изомерия
2.2.1.Оптическая изомерия
Очень многие органические вещества обладают оптической активно-
стью. Оптическая активность вещества проявляется при прохождении через него плоскополяризованного света. Плоскополяризованный свет представляет собой электромагнитные колебания, в которых электрический и магнитный векторы
18
совершают колебания только в одной плоскости, перпендикулярной направле-
нию движения луча. При прохождении через оптически активное вещество плоскость поляризации света поворачивается на определенный угол влево или вправо. Таким образом, оптическая активность – это способность вещества
вращать плоскость поляризации света.
Оптическая активность органических соединений чаще всего связана с
наличием в их составе асимметрического атома углерода. Асимметрическим
называется атом углерода, связанный с четырьмя различными заместите-
лями. Например, асимметрическим является обозначенный звездочкой атом уг-
лерода в молочной кислоте:
H O
CH3 C C 
OH OH
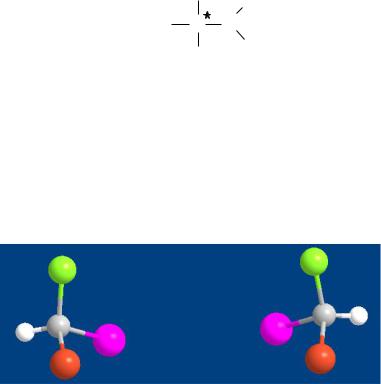
Четыре различных заместителя могут располагаться в пространстве вокруг асимметрического атома углерода двумя способами. Эти два способа относятся друг к другу как предмет и его зеркальное отражение, но при наложении они не совпадают:
Объекты, несовместимые со своим зеркальным отражением, называются
хиральными (от греческого слова χειρ – рука), а асимметрический атом углеро-
да – хиральным центром.
Пространственные изомеры, которые относятся друг к другу как предмет и несовместимое с ним зеркальное отражение, называются энантиомерами или
оптическими антиподами. Способ расположения в пространстве заместителей
19
вокруг асимметрического атома углерода называется конфигурацией энантио-
мера.
Энантиомеры обладают одинаковыми физическими (температура плавле-
ния, температура кипения, растворимость и т.д.) и химическими (одинаково реа-
гируют с неорганическими и большинством органических веществ) свойствами.
Это объясняется тем, что, поскольку энантиомеры являются зеркальными ко-
пиями друг друга, взаимное влияние атомов в их молекулах одинаково. Разли-
чаются энантиомеры только по отношению к плоскополяризованному свету.
Один из энантиомеров вращает плоскость поляризации света вправо, а другой – на такой же угол влево. Правовращающий изомер обозначается знаком (+), лево-
вращающий – знаком (−). Знак вращения энантиомера определяется только экс-
периментально с помощью прибора, который называется поляриметром.
Смесь равных количеств энантиомеров называется рацемической смесью.
Такая смесь оптически неактивна (не вращает плоскость поляризации света).
Таким образом, оптическая изомерия – вид пространственной изоме-
рии, зависящий от различного расположения в пространстве четырех за-
местителей у асимметрического атома углерода, и характеризующийся тем,
что изомеры относятся друг к другу как предмет и зеркальное отражение.
Конфигурацию энантиомеров на плоскости изображают с помощью фор-
мул Фишера. Формулы Фишера изображают следующим образом: главная уг-
леродная цепь располагается вертикально, асимметрические атомы углерода, как правило, не изображаются, а подразумеваются в месте перекрещивания связей.
Считается, что заместители, связи к которым направлены вертикально, находят-
ся за плоскостью рисунка, а заместители, связи к которым направлены горизон-
тально, находятся перед плоскостью рисунка.
20
