
- •Викладач: Бобко а.О.
- •2. Гідрофізичні фактори водних екосистем
- •2.1. Фізико-хімічні властивості води та їх екологічне значення
- •2.2. Щільність води
- •2.3. Кольоровість води
- •2.4. Температурний та термічний режим водних об’єктів
- •9.7. Льодовий режим
- •9.8. Світло та його роль у функціонуванні водних екосистем
- •9.9. Седиментація, осадоутворення та формування донних грунтів
- •9.10. Роль гідрофізичних факторів у життєдіяльності гідробіонтів
- •Глава 10. Сольовий склад вод та адаптація до нього гідробіонтів
- •10.1. Сольовий склад океанічних (морських) вод
- •10.2. Сольовий склад континентальних вод
- •10.3. Евригалінні і стеногалінні гідробіонти
- •10.4. Пристосування гідробіонтів до сольових факторів середовища
- •10.5. Адаптація гідробіонтів до водно-сольових умов середовища Пойкілоосмотичні гідробіонти
- •Гомойоосмотичні гідробіонти
- •Глава 11. Іонні компоненти та їх екологічна роль
- •11.1. Натрій, калій і цезій в водних екосистемах
- •Роль калію в метаболічних реакціях водяних рослин
- •Особливості обміну натрію і калію в організмі водяних безхребетних
- •Натрій і калій у морських і прісноводних рибах
- •Природний цезій в організмі гідробіонтів
- •11.2. Кальцій у водних екосистемах
- •Вміст кальцію в морських і океанічних водах
- •Кальцій континентальних вод
- •Метаболічна роль кальцію та шляхи його надходження в організми гідробіонтів
- •11.3. Магній морських і континентальних вод
- •Форми міграції магнію у природних водах
- •Магній в організмі гідробіонтів
- •Метаболічна роль магнію у гідробіонтів
- •11.4. Сірка природних вод та процеси сульфатредукції
- •Глава 12. Мікроелементи водних екосистем та їх біологічна роль
- •12.1. Залізо
- •Форми розчиненого заліза у водних екосистемах
- •Роль заліза у ферментативних реакціях та процесах дихання гідробіонтів
- •12.2. Мідь
- •12.3. Марганець
- •12.4. Цинк
- •12.5. Кобальт
- •12.6. Кадмій, хром, алюміній
- •Глава 13. Кисень гідросфери та його роль у водних екосистемах
- •13.1. Кругообіг кисню в водних екосистемах. Формування кисневого режиму водних екосистем
- •13.2. Роль кисню в розкладі органічних речовин та формуванні якості води
- •13.3. Роль кисню у життєдіяльності гідробіонтів
- •13.4. Особливості використання гідробіонтами кисню з води
- •Глава 14. Діоксид вуглецю в водних екосистемах
- •14.1. Хімічні та біологічні перетворення діоксиду вуглецю у водних екосистемах
- •14.2. Фотосинтез. Фіксація вуглекислоти автотрофними і гетеротрофними організмами
- •14.3. Адаптація риб до змін вмісту со2 у воді
- •Глава 15. Кругообіг та роль азоту у водних екосистемах
- •15.1. Азотфіксація у водних екосистемах
- •15.2. Використання азоту в біосинтетичних процесах водоростей
- •15.3. Алохтонний і автохтонний азот водних екосистем
- •15.4. Амоніфікація, нітрифікація і денітрифікація та їх роль в кругообігу азота в водних екосистемах
- •Глава 16. Фосфор у водних екосистемах
- •16.1. Неорганічний та органічний фосфор водних екосистем
- •16.2. Вміст фосфору в організмі гідробіонтів і його метаболічна роль
Метаболічна роль магнію у гідробіонтів
Магній належить до іонів з дуже широким спектром дії. Він відіграє виключно важливу роль в активації ферментативних реакцій, які відбуваються у автотрофних і гетеротрофних організмів. У водоростей і вищих водяних рослин він входить у структуру хлорофілу і бере участь в початкових стадіях біосинтезу порфіринового ядра (протопорфірин ІХ). Структурна формула хлорофілу має вигляд:
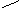 COOCH3
COOCH3
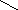 Mg N4
OH30
C32
Mg N4
OH30
C32
COOC20H32 .
При підвищенні концентрації Mg2+ у стромі хлорофілу активується рибульозо-бісфосфат-карбоксилаза та зростає споріднення її до СО2. Про значення магнію для нормального протікання фотосинтезу свідчить блідість та пожовтіння листя у водяних рослин при дефіциті магнію у воді. У водяних тварин магній відіграє ключову роль в біоенергетичному забезпеченні мембранного транспорту іонів та внутрішньоклітинному обміні амінокислот.
11.4. Сірка природних вод та процеси сульфатредукції
Сірка зустрічається в природі як в самородному вигляді, так і в різних сполуках та газоподібному стані, у вигляді сірководню та оксиду сірки. Легкорозчинні сульфати сірки знаходяться у великій кількості в морській воді.
Сірка – один з незамінних компонентів при синтезі білків в організмі тварин та утворенні сірковмістних органічних речовин у рослин. Сіркобактерії можуть окиснювати сірководень (H2S) до сірки, внаслідок чого утворювана енергія служить для них джерелом енергозабезпечення метаболічних процесів (як сонячна енергія при фотосинтезі).
Поверхневі води, у складі яких сульфатні іони становлять більше 25 %, належать до сульфатних вод. Їх хімічний склад визначається надходженням сульфатів з водозбірної площі та вимиванням з донних грунтів. Сульфати можуть надходити у водойми при хімічному вивітрюванні та вимиванні з таких мінеральних покладів, як гіпс (CaSO4·2H2O), ангідрит (CaSO4) та барит (BaSO4). При вилужуванні солончаків, води також збагачуються на сульфатні іони.
Причиною зростання вмісту сірки у воді може бути окиснення сульфідів, які надходять з стічними водами промислових, сільськогосподарських та комунально-побутових підприємств. Значним джерелом утворення сірководню у водних об'єктах є розклад органічних речовин у донних грунтах в анаеробних умовах.
Хоча сульфати добре розчинні у воді, але їх концентрація у водоймах обмежується утворенням малорозчинних сполук з кальцієм (CaSO4), які осідають на дно. В Україні сульфатні води зустрічаються переважно в річках степової зони, яка охоплює Український кристалічний щит, Причорноморську впадину, Донецьку складчасту область та схили Воронізького кристалічного масиву. У водах більшості річок цього регіону провідне місце належить сульфатам, а води належать до сульфатно-хлоридного та натрій-кальцієвого або натрій-магнієвого класу. Переважають сульфатно-хлоридні води мішаного катіонного складу у річках Приазов'я та у лівих притоках Дніпра степової зони (рр. Орель, Самара, Конка та інші).
У водних екосистемах сульфатні іони знаходяться у біологічному кругообігу. Його основними ланцюгами виступають практично всі гідробіонти, які засвоюють сульфати на побудову свого тіла. Після їх відмирання під впливом сіркобактерій Н2S окиснюється спочатку до S, а потім до SO42–, який знову включається у кругообіг. В водних екосистемах має місце також процес сульфатредукції.
Сульфатредукція – це процес відновлення сульфатних іонів до сірководню під впливом сульфатредукуючих бактерій у відсутності кисню і в присутності органічних речовин. Схематично хід реакції зображено нижче:
2 SO42– + 4 С + 3 Н2О = Н2S– + НS– + СО2 + 3 НСО3– .
В анаеробних умовах сульфатредукуючі бактерії використовують енергію сульфатів для дихання, а сірководень виділяється у воду. Подібні реакції протікають практично в усіх водоймах, де є значні поклади донних грунтів та понижений водообмін. Характерними ознаками таких водойм є наявність у воді сірководню, сульфідів, тіосульфатів та сульфатредукуючих бактерій. Такі процеси проходять з найбільшою активністю у мероміктичних водоймах, до яких належить Чорне море.
Мероміктичні – це водойми, які мають двошарову стратифікацію товщі води, при чому вода нижнього шару істотно більш мінералізована і щільна, ніж у верхньому. У таких водоймах циркуляція охоплює тільки поверхневий шар води меншої щільності. Чорне море входить до числа найбільших у світі мероміктичних водойм. В ньому на глибині 150–250 м проходить хемоклин, який розділяє розпріснений і збагачений киснем міксолімніон (верхній шар) і у 10 разів більший монімолімніон, або нижній шар води, який не перемішується.
У водоймах з добрим кисневим режимом сульфатредукція відбувається тільки в товщі мулових відкладів. При цьому чорний колір донних відкладів свідчить про характер сульфатредукуючих процесів, що проходять на дні водойм. Подібні процеси характерні для водних об'єктів, у які скидаються висококонцентровані стічні води, збагачені органічними речовинами, що містять у своєму складі сульфати. Сульфатредукція часто виникає в евтрофних водоймах, коли в них розвивається літня або зимова стагнація.
Підвищений вміст сірководню у водному середовищі негативно впливає на життєдіяльність гідробіонтів і тому вони проявляють високу чутливість до його наявності у воді. Так, поліхети Nereіs zonata, Phyllodoce tuberculata, гіллястовусі рачки Daphnіa longіspіna та багато інших не витримують навіть слідових концентрацій сірководню у воді. Більш стійкі до сірководню донні поліхети Nereіs dіversіcolor, черви Capіtella capіtata та деякі інші бентонти, які живуть у товщі донних відкладів, де відбувається гниття органічних речовин. Винятково стійкий до сірководню рачок Artemіa salіna. Токсичною концентрацією для її молоді є 76,8 мг/дм3, а для дорослих – 109 мг/дм3. Риби, особливо молодь, проявляють підвищену чутливість до сірководню.
