
- •Перший закон термодинаміки
- •Основні поняття хімічної термодинаміки
- •1.2. Сутність та формулювання першого закону термодинаміки
- •Теплоємкість. Теплота нагрівання
- •Загальні відомості. Класифікація
- •Вплив чинників на величину теплоємкості
- •2.3. Розрахунки теплоємкості
- •2.4. Теплота нагрівання
- •3. Термохімія
- •3.1. Загальні положення. Тепловий ефект реакції
- •3.2. Закон Гесса. Визначення стандартних теплових ефектів хімічних реакцій
- •3.3. Залежність теплових ефектів реакцій від температури.
- •4. Другий закон термодинаміки
- •4.1. Загальні положення. Формулювання закону
- •4.2. Два методи визначення можливості і напрямку
- •4.3. Методи розрахунків ентропії речовин і зміни ентропії
- •4.4. Статистичний характер другого закону термодинаміки. Ентропія і імовірність
- •5. Характеристичні функції і термодинамічні потенціали
- •5.1. Термодинамічні потенціали
- •5.2. Характеристичні функції. Умови рівноваги
- •5.4. Методи обчислення стандартної хімічної спорідненості
- •6. Хімічна рівновага
- •6.1. Константа хімічної рівноваги
- •6.2. Визначення виходу продуктів реакції
- •Гомогенні реакції.
- •Гетерогенні реакції.
- •6.3. Зміщення стану рівноваги. Принцип Ле-Шательє
- •6.4. Залежність константи рівноваги від температури. Рівняння ізобари реакції
- •6.5. Третій закон термодинаміки
- •6.6. Розрахунки констант хімічної рівноваги
- •7. Елементи термодинаміки необоротних процесів
- •7.1. Загальні відомості. Класифікація необоротних процесів
- •7.2. Основні закономірності термодинаміки необоротних процесів
3.3. Залежність теплових ефектів реакцій від температури.
Закон Кірхгофа
Здебільшого металургійні процеси проводяться не при кімнатній (298 К), а при значно вищих температурах, оскільки реакції окислення-відновлення і розкладу при низьких температурах протікають дуже повільно.
Тому стає задача визначати теплові ефекти реакцій при будь-яких температурах. Це можна зробити за законом Кірхгофа. Вивід закону проведемо, використавши реакцію відновлення заліза з оксидів воднем
Fe2O3+ 3H2= 2Fe+ 3H2O.
Як вище вказувалось, тепловий ефект реакції – це зміна ентальпії системи у ході реакції. Тому
![]() .
.
Візьмемо диференціал рівняння по температурі при сталому тиску і, пам'ятуючи рівняння (2.5), одержимо:
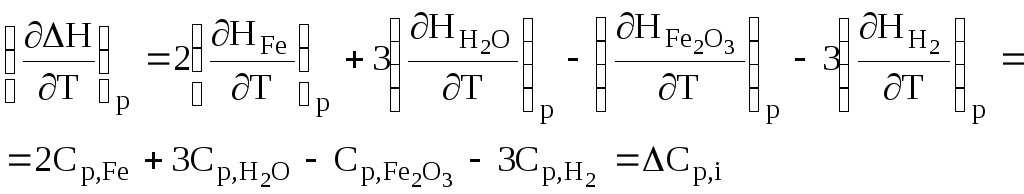
або
![]() , (3.5)
, (3.5)
де Ср,і- зміна теплоємкості у ході реакції, яку можна визначити за рівнянням
Ср,і=nіСр,кін.,і-nіСр,поч.,і.
Рівняння (3.5) є законом Кірхгофа в
диференціальній формі: температурний
коефіцієнт ізобарного теплового ефекту
реакції
![]() дорівнює зміні ізобарної теплоємкості
реакції.
дорівнює зміні ізобарної теплоємкості
реакції.
Аналіз рівняння (3.5) свідчить про складну залежність теплового ефекту реакції від температури.
Дійсно, при Ср,і0 і величина![]() 0,
тобто з ростом температури тепловий
ефект реакції збільшується. ЯкщоСр,і0, то і
0,
тобто з ростом температури тепловий
ефект реакції збільшується. ЯкщоСр,і0, то і![]() 0.
отже з ростом температури тепловий
ефект реакції зменшується. Нарешті, приСр,і= 0 і
величина
0.
отже з ростом температури тепловий
ефект реакції зменшується. Нарешті, приСр,і= 0 і
величина![]() .
У цьому випадку температура на тепловий
ефект реакції не впливає.
.
У цьому випадку температура на тепловий
ефект реакції не впливає.
При зміні температури теплоємкості реагуючих речовин змінюються не однаково, тому можливі випадки, коли для реакції при одних температурах Ср,і0, а при других -Ср,і0 і навпаки. У цьому разі залежність теплового ефекту від температури описується кривими, наведеними на рис. 3.1.
Закон Кірхгофа в диференціальній формі дозволяє лише якісно оцінити вплив температури на тепловий ефект реакції. Щоб мати змогу кількісно обчислювати теплові ефекти при будь-яких температурах, треба проінтегрувати рівняння (3.5) в межах температур від Т1до Т2:
![]()

Рис. 3.1. Залежність теплового ефекту реакції від температури в умовах
зміни знаку величини niCp,i
![]() ;dH
= Cр,іdT;
;dH
= Cр,іdT;
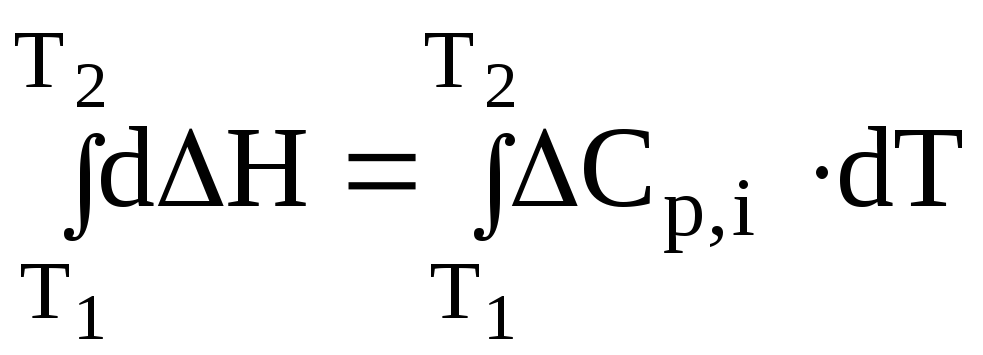 ;
;
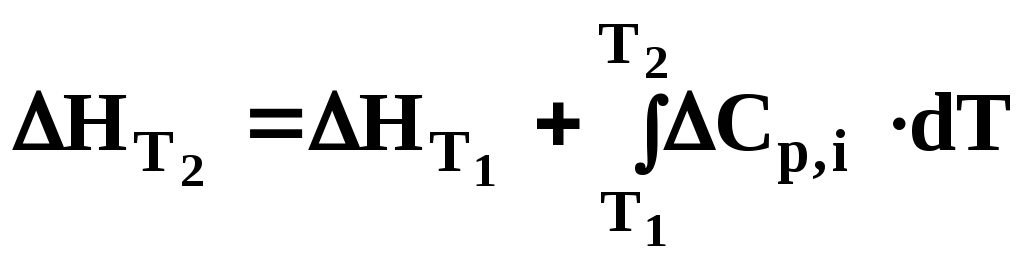 . (3.6)
. (3.6)
Рівняння (3.6) відоме як закон Кірхгофа в інтегральній формі: тепловий ефект реакції при будь-якій температурі (Т2) дорівнює тепловому ефекту цієї реакції при певній температурі (Т1), плюс інтеграл Кірхгофа.
На практиці найчастіше беруть Т1= 298 К, бо стандартні теплові ефекти багатьох реакцій відомі, а при потребі їх можна визначити за законом Гесса. Тому закон Кірхгофа можна представити рівнянням
![]() . (3.7)
. (3.7)
Розв'язати інтеграл Кірхгофа можна двома методами. Перший метод полягає в використанні емпіричного ступеневого ряду теплоємкості
![]()
![]()
![]() , (3.8)
, (3.8)
де а, в, с і с'– зміна коефіцієнтів емпіричного ступеневого ряду у ході реакції, яку можна визначити за рівнянням:
![]() ;
;
![]() і т.д.
і т.д.
При обчисленні інтегралу Кірхгофа за другим методом користуються функціями тепловмісту реагуючих речовин
![]() , (3.9)
, (3.9)
де
![]() і
і![]() - зміна функцій тепловмісту у ході
реакції, яку можна визначити за рівняннями:
- зміна функцій тепловмісту у ході
реакції, яку можна визначити за рівняннями:
![]() ;
;
![]() . (3.10)
. (3.10)
Якщо в інтервалі температур від 298 до Т К є фазові перетворення, обчислення теплового ефекту треба вести за рівнянням (3.9), в якому всі можливі фазові перетворення враховані. При користуванні рівнянням (3.8) необхідно врахувати теплоти фазових перетворень, а також зміну теплоємкості речовини, що при цьому відбувається. У цьому випадку рівняння (3.8) набуває вигляду
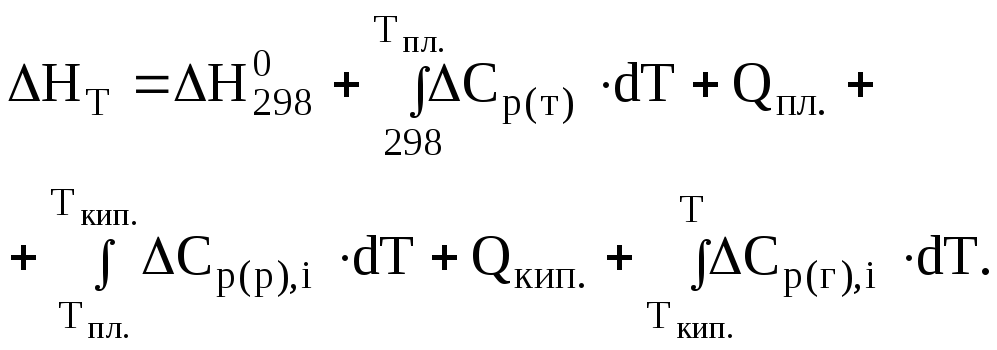 (3.11)
(3.11)
Задача 3.1.Визначити теплові ефекти реакції (Х)
Х. Fe3O4 + 4CO = 3Fe + 4CO2,
що має місце при виплавці чавуну у доменному процесі, при 298 і 1000 К. Зробити висновки про вплив температури на тепловий ефект реакції.
Розв'язання. Стандартний тепловий ефект реакції визначимо шляхом алгебраїчного підсумовування допоміжних реакцій, які підбираємо, користуючись табл. Д.3 і правилами, наведеними на стор. 26:
І .Fe3O4
+ CО = 3FeO + CO2
+1
.Fe3O4
+ CО = 3FeO + CO2
+1
![]() =
39,60 кДж;
=
39,60 кДж;
ІІ. FeO + CO = Fe +
CO2
+3
![]() =
-18,13 кДж.
=
-18,13 кДж.
Перевірка. Підсумовуючи допоміжні рівняння за (3.3), одержуємо
Fe3O4 + CO + 3FeO + 3CO = 3FeO + CO2 + 3Fe + 3CO2.
Після скорочення і об'єднання однакових речовин, маємо рівняння
Fe3O4 + CO = 3Fe + CO2,
що відповідає базовому рівнянню (Х). Перевірка позитивна. Тепловий ефект визначаємо за рівнянням (3.4)
![]() кДж.
кДж.
Оскільки
![]() 0,
то при 298 К досліджувана реакція проходить
з виділенням теплоти (екзотермічна
реакція).
0,
то при 298 К досліджувана реакція проходить
з виділенням теплоти (екзотермічна
реакція).
Тепловий ефект при 1000 К визначимо за рівнянням (3.8)
![]() .
.
![]()
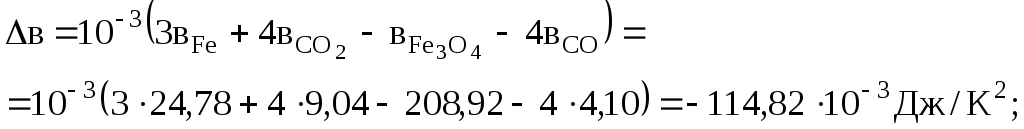
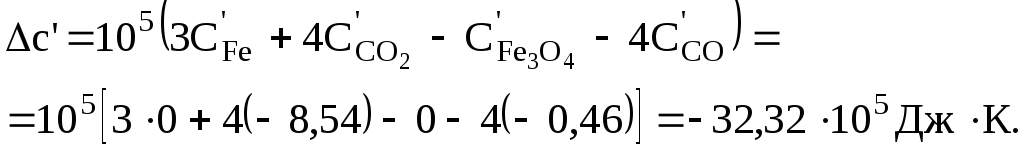
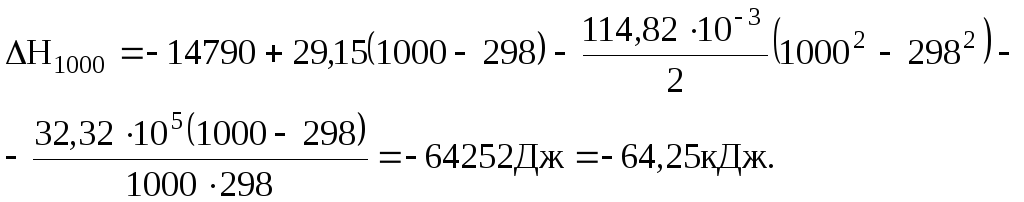
Н1000 0, отже реакція і при 1000 К проходить з виділенням теплоти (екзотермічна). При зростанні температури від 298 до 1000 К тепловий ефект реакції зменшується від –14,79 до –62,30 кДж.
Задача 3.2. Визначити тепловий ефект реакції
Fe3O4+ 4CО = 3Fe+ 4CO2
при 1100 К. Відомо, що при 1033 К залізо з -форми переходить в -форму і теплота переходу (Qпер.) становить 2,76 кДж/моль.
Роз'язання. Тепловий ефект реакції визначаємо за рівнянням (3.11), яке в цьому випадку має вигляд
![]() .
.
Візьмемо а, в і с' до перетворення заліза з попередньої задачі, а після перетворення – розрахуємо по аналогії:
а = 337,68+444,14-86,27-428,41 = 77,69 Дж/К;
в = 10-3(30+49,04-208,92-44,10) = -189,16 Дж/К2;
с' = 105[30+4(-8,54)-0-4(-0,46)] = -32,32105ДжК.

Задача 3.3. Марганець одержують відновленням його оксидів алюмінієм. Реакція природнього MnO2 з алюмінієм проходить дуже бурхливо, тому MnO2 поперед прожарюють до Mn2O3, який реагує з алюмінієм більш спокійно
3Mn3O4+ 8Al= 9Mn+ 4Al2O3.
Визначити теплові ефекти реакції при 298 і 1000 К. Зробити висновок про вплив температури на тепловий ефект реакції.
Розв'язання.
Стандартний тепловий ефект реакції
визначимо за рівнянням (3.2), взявши
![]() з табл. Д.2.
з табл. Д.2.
![]()
Тепловий ефект при 1000 К знайдемо за рівнянням (3.9), скориставшись даними табл. Д.4.
![]() ;
;
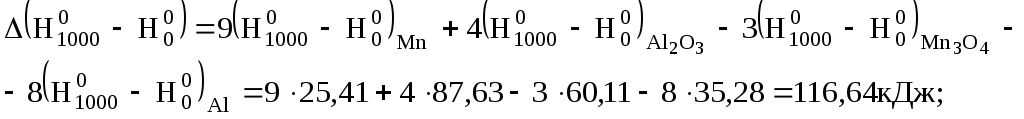
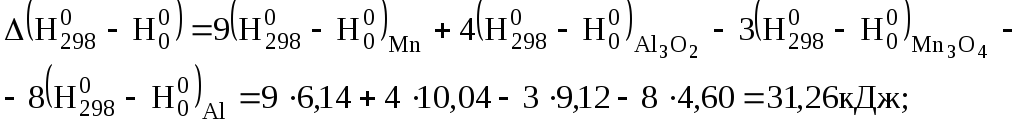
![]() кДж.
кДж.
Таким чином, реакція відновлення марганцю протікає з виділенням теплоти і при 298, і при 1000 К, тобто є екзотермічною. З підвищенням температури тепловий ефект реакції дещо збільшується.
