
- •Перший закон термодинаміки
- •Основні поняття хімічної термодинаміки
- •1.2. Сутність та формулювання першого закону термодинаміки
- •Теплоємкість. Теплота нагрівання
- •Загальні відомості. Класифікація
- •Вплив чинників на величину теплоємкості
- •2.3. Розрахунки теплоємкості
- •2.4. Теплота нагрівання
- •3. Термохімія
- •3.1. Загальні положення. Тепловий ефект реакції
- •3.2. Закон Гесса. Визначення стандартних теплових ефектів хімічних реакцій
- •3.3. Залежність теплових ефектів реакцій від температури.
- •4. Другий закон термодинаміки
- •4.1. Загальні положення. Формулювання закону
- •4.2. Два методи визначення можливості і напрямку
- •4.3. Методи розрахунків ентропії речовин і зміни ентропії
- •4.4. Статистичний характер другого закону термодинаміки. Ентропія і імовірність
- •5. Характеристичні функції і термодинамічні потенціали
- •5.1. Термодинамічні потенціали
- •5.2. Характеристичні функції. Умови рівноваги
- •5.4. Методи обчислення стандартної хімічної спорідненості
- •6. Хімічна рівновага
- •6.1. Константа хімічної рівноваги
- •6.2. Визначення виходу продуктів реакції
- •Гомогенні реакції.
- •Гетерогенні реакції.
- •6.3. Зміщення стану рівноваги. Принцип Ле-Шательє
- •6.4. Залежність константи рівноваги від температури. Рівняння ізобари реакції
- •6.5. Третій закон термодинаміки
- •6.6. Розрахунки констант хімічної рівноваги
- •7. Елементи термодинаміки необоротних процесів
- •7.1. Загальні відомості. Класифікація необоротних процесів
- •7.2. Основні закономірності термодинаміки необоротних процесів
2.4. Теплота нагрівання
Теплотою нагрівання речовини (![]() )
називають величину, що показує, яку
кількість теплоти потрібно надати
одиниці маси речовини (звичайно одному
моль), щоб нагріти її від Т1до Т2.
)
називають величину, що показує, яку
кількість теплоти потрібно надати
одиниці маси речовини (звичайно одному
моль), щоб нагріти її від Т1до Т2.
Розрахунки теплоти нагрівання базуються на рівняннях, що наведені у попередніх розділах.
Теплоту нагрівання одного моль речовини можна визначити за емпіричним ступеневим рядом (2.7; 2.9)
![]()
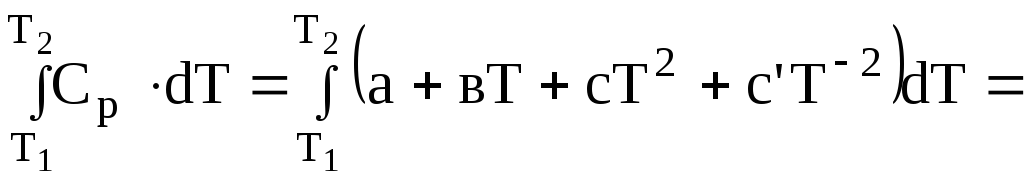
![]() , (2.13)
, (2.13)
за допомогою функцій тепловмісту речовин (1.6)
![]()
![]()
![]() (2.14)
(2.14)
або через середню теплоємкість речовини (2.7; 2.8)
![]() . (2.15)
. (2.15)
Якщо треба визначити теплоту нагрівання
будь-якої маси (m) речовини,
то рівняння (2.13-1.15) треба множити на
величину числа моль (n)
речовини, яку можна знайти з співвідношення![]() .
Наприклад,
.
Наприклад,
![]() і т.д. (2.16)
і т.д. (2.16)
Якщо відома питома теплоємкість речовини, то можна відразу визначити теплоту нагрівання всієї маси за рівнянням
![]() , (2.17)
, (2.17)
а при визначенні теплоти, необхідної для нагрівання і плавлення сполуки, за рівнянням
![]() , (2.18)
, (2.18)
де Qр,пл.– теплота плавлення, Дж/кг.
У випадках, коли в інтервалі температур Т1Т2має місце фазове перетворення (плавлення, кипіння), треба користуватися в розрахунках рівняннями (2.14-2.15), в яких всі можливі в цьому інтервалі температур фазові перетворення враховані. При обчисленні теплоти нагрівання за рівнянням (2.13) необхідно врахувати теплоту фазового перетворення і зміну коефіцієнтів емпіричного ступеневого ряду зі зміною агрегатного стану речовин. Рівняння (2.13) у цьому разі має вигляд
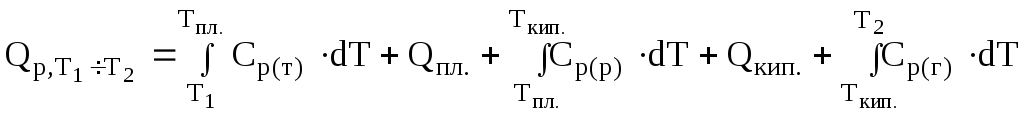 . (2.19)
. (2.19)
При визначенні ізохорної теплоти нагрівання користуються ізохорною теплоємкістю, наприклад
![]() . (2.20)
. (2.20)
На практиці часто виникає потреба визначення теплоти нагрівання складної системи – суміші (сталі, феросплаву і т.д.). Розрахунки базуються на адитивних властивостях теплоти нагрівання і проводяться за рівнянням
![]() , (2.21)
, (2.21)
де
n1,2,…,і– кількість
моль і-ої речовини в суміші;![]() - теплота нагрівання і-ої речовини,
Дж/моль.
- теплота нагрівання і-ої речовини,
Дж/моль.
Задача 2.1. Визначити істинну мольну ізохорну теплоємкість марганцю при 400 К і середню питому теплоємкість в інтервалі температур від 300 до 500 К.
Розв'язання. Істинну мольну ізобарну теплоємкість марганцю можна знайти, скориставшись довідниковими даними (табл. Д.2), за рівнянням (2.9)
![]()
При 400 К марганець знаходиться в твердому агрегатному стані (табл. Д.2), тому
![]() Дж/(мольК).
Дж/(мольК).
Середню мольну теплоємкість марганцю в указаному інтервалі температур можна визначити за рівнянням (2.10)
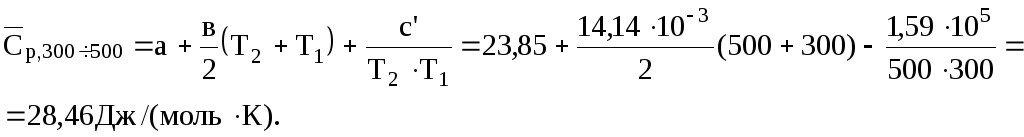
Середня питома теплоємкість марганцю дорівнюватиме (2.1)
![]() Дж/(кгК).
Дж/(кгК).
Задача 2.2. Визначити питому теплоємкість жаростійкої сталі, що містить (у мас. %):Cr– 20,0;Ni– 7,0;Mn– 5,0;Si– 1,5;W– 1,0;C– 0,4. Мольні теплоємкості елементів відповідно дорівнюють: 23,35; 25,78; 26,28; 19,19; 24,98; 8,54.Cр,Fe= 25,00 Дж/(мольК).
Розв'язання. Питому теплоємкість сталі можна визначити за рівнянням (2.12), розрахувавши спочатку питомі теплоємкості елементів за рівнянням (2.1):
![]() Дж/(кгК).
Дж/(кгК).
Аналогічно визначають питому теплоємкість інших елементів і потім питому теплоємкість сталі, зваживши, що вміст заліза за умовами задачі складає 65,1%
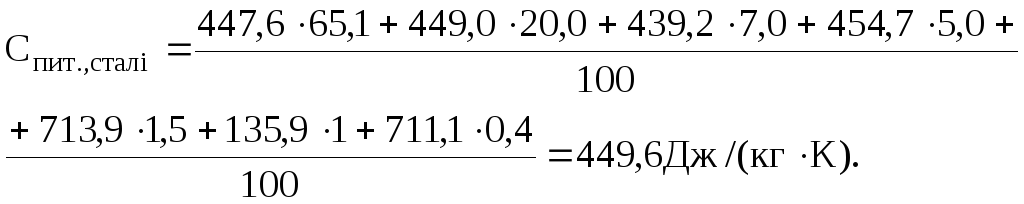
Задача 2.3.Визначити теплоту, яка потрібна для нагрівання 50 кг міді від 298 до 1500 К. Відомо, що Тпл.=1356 К; Ткип.=2843 К;Qпл.=12,98 кДж/моль.
Розв'язання. Теплоту нагрівання можна визначити за рівняннями (3.1 і 3.7), взявши коефіцієнти ступеневого ряду з табл. Д.2:
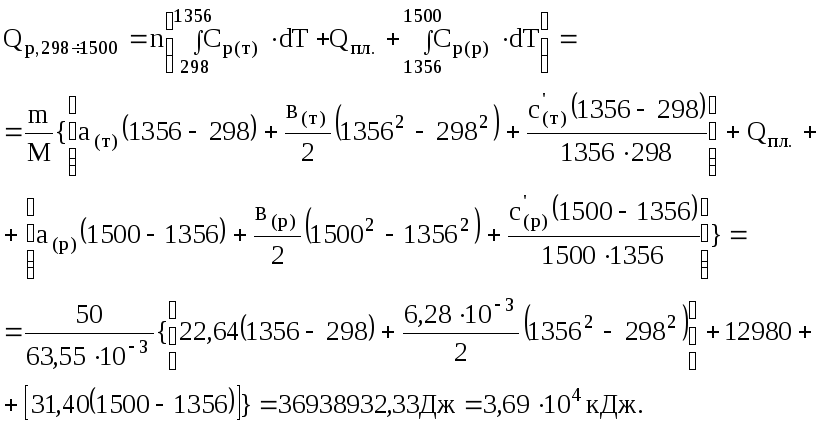
Задача 2.4.Визначити кількість коксу, яка потрібна для плавлення 10 т чавуну, в якому міститься 4,3% вуглецю. Початкова температура чавуну 298 К, температура плавлення 1428 К, теплота плавлення 96 кДж/кг, середня питома теплоємкість чавуну в інтервалі температур 2981428 К дорівнює 540Дж/(кгК). Теплота згоряння коксу становить 3104кДж/кг, коефіцієнт корисної дії печі – 60%.
Розв'язання. Загальну кількість теплоти, що потрібна для нагрівання і плавлення чавуну розраховуємо за рівнянням (3.6)
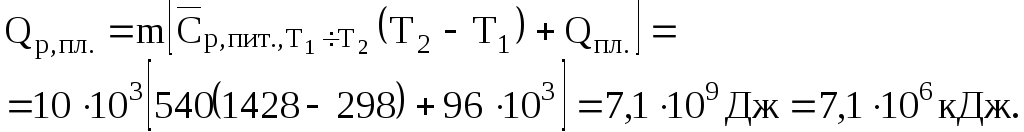
Кількість коксу, яка теоретично потрібна для плавлення чавуну, складатиме
![]() кг.
кг.
З урахуванням к.к.д. печі, кількість коксу, необхідного для плавлення 10 т чавуну, становитиме
![]() кг.
кг.
