
minikurs
.pdf
|
|
КЛАССЫ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ |
|
|
А9, |
А10, |
|
А11, |
В5, |
С2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Оксиды |
|
А9, |
В5 |
|
|
|
Гидроксиды |
|
А10, |
|
В5 |
|
||||||
ОСНОВНЫЕ оксиды – оксиды, которым соответствуют |
основания. |
ОСНОВНЫЕ |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
1. Основный оксид + кислота → соль + вода |
|
|
|
|
1. |
Основание + кислота → соль + вода |
|
|
|
|
|
|
|
|
|
||||
CaO + 2 HNO3 → Ca (NO3)2 + H2O |
|
|
|
|
|
NaOH + HCl → NaCl + H2O |
(реакция нейтрализации) |
||||||||||||
|
|
|
|
|
|
|
Ca(OH)2 + HCl → CaOHCl + H2O |
|
|
|
|
|
|
|
|
|
|||
2. Основный оксид + кислотный оксид → соль |
|
|
|
|
|
Mn(OH)2 + 2 HCl → MnCl2 + 2 H2O |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
2. |
Основание (щелочь) + кислотный оксид → соль + вода |
||||||||||||||
|
t |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
Ca(OH)2 + CO2 → CaCO3 + H2O; |
|
NaOH + CO2(изб.) → NaHCO3 |
|||||||||||
MgO + SiO2 → MgSiO3 |
|
|
|
|
3. |
|
|||||||||||||
|
|
|
|
|
|
Щелочь + амфотерный оксид или гидроксид → соль + вода |
|||||||||||||
3. Основный оксид + вода → щелочь |
|
|
|
|
Сплавление: 2 NaOH + ZnO → Na2ZnO2 + H2O; |
2 NaOH + Zn(OH)2 →Na2ZnO2 + 2H2O |
|||||||||||||
|
|
|
|
В растворе: 2 KOH + H2O + ZnO → K2[Zn(OH)4]; 2KOH + Zn(OH)2 → K2[Zn(OH)4] |
|||||||||||||||
K2O + H2O → 2 KOH |
|
|
|
|
|||||||||||||||
|
|
|
|
4. |
Щелочь + соль (растворимая) → |
новая соль + осадок или газ |
|||||||||||||
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
5. |
2 NaOH + CuSO4 → Cu(OH)2 ↓+ Na2SO4 |
|
NaOH + NH4Cl → NH3↑ + H2O + NaCl |
||||||||||
|
|
|
|
|
|
Щелочи – с неметаллами и амфотерными металлами |
|||||||||||||
|
|
|
|
|
|
Cl2 + 2 KOH(холодн) → KCl + KClO + H2O; Cl2 + 6 KOH(гор) → 5 KCl + KClO3 + 3H2O |
|||||||||||||
|
|
|
|
|
|
3S + 6NaOH→ 2Na2S + Na2SO3+3H2O; |
2Al+2NaOH+2H2O→2NaAlO2 + 3H2 |
||||||||||||
|
|
|
|
|
|
6. |
Разложение нерастворимых оснований при нагревании |
||||||||||||
|
|
|
|
|
|
|
t |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cu(OH)2 → CuO + H2O |
|
|
|
|
|
|
|
|
|
|
|
|
КИСЛОТНЫЕ оксиды – оксиды, которым соответствуют кислоты. |
КИСЛОТНЫЕ (кислородсодержащие кислоты) |
||||||||||||||||||
1. Кислотный оксид + основание → соль + вода |
|
|
|
|
1. |
С металлами, стоящими в электрохимическом ряду левее водорода |
|||||||||||||
|
SO2 + 2 NaOH → Na2SO3 + H2O |
|
|
|
|
|
Zn + H2SO4 → ZnSO4 + H2 |
Fe + 2 HCl → FeCl2 + H2 |
|||||||||||
! особый оксид NO2: |
2 NO2 + 2 NaOH → NaNO3 + NaNO2 + H2O |
2. |
С основными и амфотерными оксидами, если обр-ся растворимая соль |
||||||||||||||||
|
|
|
|
|
|
ZnO + 2 HNO3 → Zn(NO3)2 + H2O |
CaO + H2SO4 → CaSO4 + H2O |
||||||||||||
2. Кислотный оксид + основный оксид → соль |
|
|
|
|
3. |
С основаниями (у NH3 - основные св-ва) и амфотерными гидроксидами |
|||||||||||||
|
|
|
|
H3PO4 + 3NaOH → Na3PO4 + 3H2O |
H3PO4 + NaOH → NaH2PO4 + H2O |
||||||||||||||
|
CaO + CO2 → CaCO3 |
|
|
|
|
||||||||||||||
|
|
|
|
|
H2SO4 + 2 NH3 → (NH4)2SO4 |
H2SO4 + NH3 → NH4HSO4 |
|||||||||||||
3. Кислотный оксид (растворимый в воде) + вода → кислота |
4. |
С солями, если образуется осадок или газ |
|||||||||||||||||
H2SO4 + BaCl2 → BaSO4↓ + 2 HCl |
Na2CO3 + 2 HNO3 → 2 NaNO3 + CO2 + H2O |
||||||||||||||||||
|
N2O5 + H2O → 2 HNO3 |
|
|
|
|
|
|
|
|
HNO3 |
|||||||||
! особый оксид NO2: |
2 NO2 + H2O → HNO3 + HNO2 |
|
|
|
|
Вытеснительный ряд кислот H2SO4 |
|
HCl |
H2SO3, H3PO4, HNO2, H2CO3, H2SiO3 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АМФОТЕРНЫЕ оксиды проявляют и кислотные, и основные свойства. |
АМФОТЕРНЫЕ |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
1. Амфотерный оксид + кислота → соль + вода |
|
|
|
|
1. |
Амфотерный гидроксид + кислота → соль + вода |
|||||||||||||
|
ZnO + 2 HCl → ZnCl2 + H2O |
|
|
|
|
|
Zn(OH)2 + 2 HCl → ZnCl2 + 2 H2O |
||||||||||||
2. Амфотерный оксид + щелочь → вода + соль или комплексное соед – е |
2. |
Амфотерный гидроксид + щелочь → комплексное соед. или соль + вода |
|||||||||||||||||
|
|
|
|
|
|
В растворе: |
Zn(OH)2 + 2 NaOH → Na2[Zn(OH)4] |
||||||||||||
В растворе: |
Al2O3 + 2 NaOH + 3 H2O → 2 Na[Al(OH)4] |
Сплавление: |
Zn(OH)2 + 2 NaOH → Na2ZnO2 + 2H2O |
||||||||||||||||
Сплавление: |
Al2O3 + 2 NaOH → 2 NaAlO2 + H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
СОЛИ |
|
А11, |
|
В5 |
|
|
|
СРЕДНИЕ соли – продукты полного замещения атомов водорода в |
КИСЛЫЕ соли – продукты |
неполного замещения атомов водорода в |
||||||||
кислоте на металл |
|
|
кислоте на металл |
|
|
|
|
|
|
|
1. Соль + кислота→ другая соль + другая кислота (если образуется↓ или ↑) |
1. С основными оксидами: CaO + Ca(HCO3)2 → 2 CaCO3 + H2O |
|||||||||
H2SO4 + BaCl2 → BaSO4↓ + 2 HCl |
|
Na2CO3 + 2 HNO3 → 2 NaNO3 + CO2↑ + H2O |
|
|
|
|
|
|
|
|
2. Соль + щелочь→ другая соль + другое основание (если обр-ся ↓ или ↑) |
2. Со щелочами: NaH2PO4 + 2 NaOH → Na3PO4 + 2 H2O |
|||||||||
Ca(HCO3)2 + Ca(OH)2 → 2 CaCO3 + 2 H2O |
||||||||||
2 NaOH + CuSO4 → Cu(OH)2 ↓+ Na2SO4 |
NaOH + NH4Cl → NH3↑ + H2O + NaCl |
|
|
|
|
|
|
|
||
3. Соль1 + соль2 → соль3 + соль4 ( одна из них в ↓) |
3. С сильными кислотами: |
NaHCO3 + H2SO4 → NaHSO4 + CO2 + H2O |
||||||||
|
|
|
|
|
|
|
||||
(растворимые в воде) |
|
|
4. Разложение при нагревании: Ca(HCO3)2 → CaCO3 + H2O + CO2 |
|||||||
Ca(NO3)2 + Na2CO3 → CaCO3↓ + 2 NaNO3 K2SO4 + BaCl2 → 2 KCl + BaSO4↓ |
||||||||||
4. Соль + металл → другая соль + другой металл |
Получение: |
|
|
|
|
|
|
|||
(металл, стоящий левее в электрохим. ряду активностей, вытесняет из |
1. H2SO4 + NaOH → NaHSO4 + H2O |
|
||||||||
солей металл, стоящий правее его) |
CaCO3 + H2O + CO2 → Ca(HCO3)2 |
|||||||||
Zn + FeSO4 → ZnSO4 + Fe |
|
Fe + CuCl2 → FeCl2 + Cu |
2. Ca(OH)2 + 2 CO2(изб) → Ca(HCO3)2 или |
|||||||
|
3. Ca3(PO4)2 + 4 H3PO4 (изб) → 3 Ca(H2PO4)2 |
|
||||||||
|
|
|
|
|
||||||
|
|
|
|
Диссоциируют ступенчато: I. NaHSO3 ↔ Na+ + (HSO3)- II. (HSO3)- ↔ H+ + (SO3)2- |
||||||
|
|
|
|
|||||||
5. Разложение солей |
|
|
ОСНОВНЫЕ соли – продукты неполного замещения гидроксогрупп в |
|||||||
|
|
|
|
основании на кислотный остаток |
|
|||||
5.1 Разложение нитратов |
|
|
|
|
|
|
|
|
|
|
|
Li - Na…………… |
MeNO2 + O2↑ |
1. С кислотами: Mg(OH)Cl + HCl → MgCl2 + H2O |
|||||||
|
|
|
|
2. С кислотными оксидами: 2 Al(OH)SO4 + SO3 → Al2(SO4)3 + H2O |
||||||
MeNO3 |
Mg - Cu …… |
MeO + NO2↑ + O2↑ |
3. Со щелочами (если обр-ся ↓): Fe(ОН)Cl2 +2 NaOH → 2 NaCl + Fe(ОН)3↓ |
|||||||
|
Hg, Ag…………. |
Me + NO2↑ + O2↑ |
Получение: |
|
|
|
|
|
Диссоциируют ступенчато: |
|
|
|
|
|
1. Ca(OH)2 + HCl → Ca(OH)Cl + H2O |
I. (CaOH)Cl ↔ (CaOH)+ + Cl- |
|||||
|
|
|
|
2. MgO + MgCl2 + H2O → 2 Mg(OH)Cl |
II. (CaOH)+ ↔ Ca2+ + OH- |
|||||
|
|
|
|
|
||||||
|
|
|
|
КОМПЛЕКСНЫЕ соединения, в которых хотя бы одна ковалентная связь |
||||||
|
|
|
|
образована по донорно-акцепторному механизму |
||||||
5.2 Разложение солей аммония |
|
Некоторые реакции: |
|
|
|
|
|
|
||
NH4Cl → NH3 + HCl |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||
NH4NO2 → 2 H2O + N2 |
|
|
Na[Al(OH)4] + HCl → NaCl + Al(OH)3 + H2O |
|||||||
NH4NO3 → 2 H2O + N2O |
|
|
Na[Al(OH)4] + 2 HCl → Al(OH)2Cl + 2 H2O |
|
||||||
(NH4)2Cr2O7 → Cr2O3 + N2 + 4 H2O |
Na[Al(OH)4] + 3 HCl → Al(OH)Cl2 + 3 H2O |
|
||||||||
Na[Al(OH)4] + 4 HCl → NaCl + AlCl3 + 4 H2O |
|
|||||||||
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|

А12
|
|
|
|
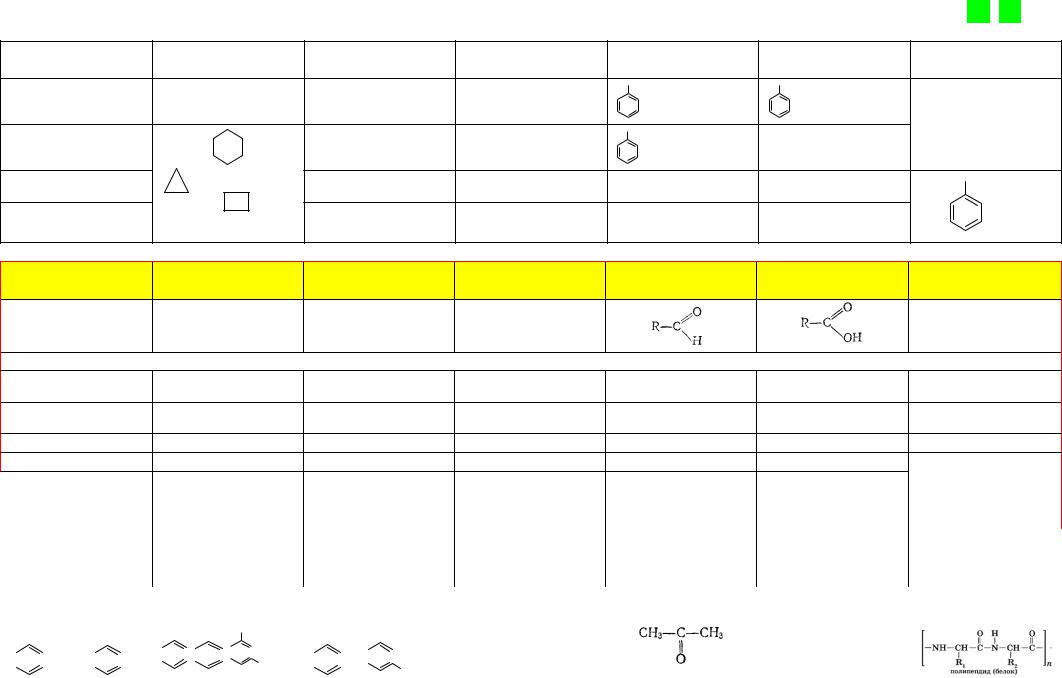
Классификация органических веществ |
|
|
А7, В1 |
||||
CnH2n+1 |
ЦИКЛОАЛКАНЫ |
ДИЕНЫ |
Многоатомные |
Углеводы. |
Другие кислоты |
АМИНЫ |
|||||
РАДИКАЛЫ |
|
|
|
|
спирты |
Другие спирты, альдегиды. |
|
|
|||
|
|
|
|
CH2OH |
|
|
|
||||
Метил |
|
CnH2n |
|
CnH2n-2 |
|
|
|
COOH |
R1-NH2 первичные |
||
|
|
|
|
|
|
|
|||||
|
-CH3 |
|
|
|
|
|
|
COH бензиловый спирт |
бензойная кислота |
R1-NH-R2 вторичные |
|
Этил |
|
|
|
CH2=CH-CH=CH2 |
CH2(OH)-CH2(OH) |
R1-N-R2 третичные |
|||||
|
|
|
|
|
HOOC-COOH |
R3 |
|||||
|
-C2H5 |
|
|
(бутадиен-1,3; дивинил) |
этиленгликоль |
|
|
щавелевая кислота |
|||
|
|
|
|
|
бензальдегид |
|
|||||
Пропил |
-C3H7 |
|
|
|
|
|
|
|
NH2 |
||
|
|
CH2=C(CH3)-CH=CH2 |
CH2(OH)-CH (OH )-CH2(OH) |
C6H12O6 глюкоза |
C17H33COOH |
||||||
Изопропил |
|
|
|
(изопрен) |
глицерин |
CH2OH-(CHOH)4-COH |
олеиновая к-та |
|
|||
|
|
|
|
|
|
C6H12O6 фруктоза |
C17H31COOH |
|
|||
- CH(CH3)2 |
|
|
|
|
|
|
CH2OH-(CHOH)3-CO-CH2OH |
линолевая к-та |
анилин |
||
|
|
|
|
|
|
кетоноспирт |
|
||||
АЛКАНЫ |
АЛКЕНЫ |
АЛКИНЫ |
СПИРТЫ |
АЛЬДЕГИДЫ |
КИСЛОТЫ |
АМИНОКИСЛОТЫ |
|||||
|
|
|
|
|
|
(алканолы) |
|
|
карбоновые |
|
|
CnH2n+2 |
CnH2n |
|
CnH2n-2 |
CnH2n+1OH |
|
|
|
(NH2)CnH2nCOOH |
|||
Метан |
CH4 |
|
_ |
|
_ |
Метанол |
CH3OH |
Метаналь |
HCOH |
Метановая HCOOH |
NH2-CH2-COOH |
Этан |
C2H6 |
Этен (этилен) C2H4 |
Этин(ацетилен) C2H2 |
|
|
(формальдегид, формалин) |
(муравьиная) - формиат |
глицин |
|||
Этанол |
C2H5OH |
Этаналь CH3-COH |
Этановая CH3COOH |
CH3-CH(NH2)-COOH |
|||||||
Пропан |
C3H8 |
Пропен |
C3H6 |
Пропин C3H4 |
|
|
(ацетальдегид) |
(уксусная) - ацетат |
аланин |
||
Пропанол |
C3H7OH |
Пропаналь |
C2H5 -COH |
Пропановая C2H5COOH |
|
||||||
Бутан |
C4H10 |
Бутен |
C4H8 |
Бутин |
C4H6 |
Бутанол |
C4H9OH |
Бутаналь |
C3H7 -COH |
Бутановая C3H7COOH |
C6H5-CH2-CH-COOH |
Пентан |
C5H12 |
Пентен |
|
C5H10 |
Пентин |
|
|
|
C5H8 |
Пентанол |
C5H11OH |
Пентаналь C4H9 -COH |
Пентановая C4H9COOH |
|
|
||||||||||||||||
|
|
|
|
NH2 |
|||||||||||||||||||||||||||
Гексан |
C6H14 |
Гексен |
|
C6H12 |
Гексин |
|
|
|
C6H10 |
Гексанол C6H13OH |
Гексаналь C5H11COH |
Гексановая и т.д. |
|||||||||||||||||||
|
|
|
|
фенилаланин |
|||||||||||||||||||||||||||
Гептан |
C7H16 |
Гептен |
|
C7H14 |
Гептин |
|
|
|
C7H12 |
Гептанол |
C7H15OH |
Гептаналь C6H13COH |
C15H31COOH |
||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||
Октан |
C8H18 |
Октен |
|
C8H16 |
Октин |
|
|
|
C8H14 |
и т.д. |
|
и т.д. |
пальмитиновая к-та |
|
|
||||||||||||||||
Нонан |
C9H20 |
Нонен |
|
C9H18 |
Нонин |
|
|
|
C9H16 |
|
|
|
C17H35COOH |
|
|
||||||||||||||||
Декан |
C10H22 |
Декен |
|
C10H20 |
Декин |
|
|
|
C10H18 |
|
|
|
стеариновая к-та |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CnH2n-8 CnH2n-6 |
|
АРЕНЫ CnH2n-6 |
|
|
|
ФЕНОЛЫ |
Простые ЭФИРЫ |
КЕТОНЫ |
Сложные ЭФИРЫ |
БЕЛКИ |
|||||||||||||||||||||
|
|
CH=CH2 |
H3C |
|
|
CH-CH3 |
|
|
|
|
|
CH3 |
|
CH3 |
|
OH |
|
|
OH |
R1-O-R2 |
|
R1-COO-R2 |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3-COO-CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
CH3-O-CH3 диметиловый |
ацетон |
метилацетат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Стирол |
Кумол |
Бензол Толуол Ксилол |
Фенол |
Крезол |
CH3-O-C2H5 метилэтиловый |
H-COO-C2H5 |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
винилб-л изопропилбензол |
(-C6H5 радикал фенил) |
(карболовая |
|
|
|
|
C2H5-O-C2H5 диэтиловый |
|
этилформиат |
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота) |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
А13 |
|
Гомологический ряд |
|
|
Тип |
Тип связи |
Общая формула |
Молярная |
|
|
|
НОМЕНКЛАТУРА |
|
|
||||||
|
гибридизации |
|
|
|
масса |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||||||||||
Алканы |
sp3 |
при одинарной |
сигма |
|
CnH2n+2 |
14n+2 |
1. В основе названия соединения лежит родоначальная |
|||||||||||
|
|
|
связи |
|
|
|
|
структура (главная цепь: алкан, алкен, диен, алкин и |
||||||||||
|
|
|
|
|
|
|
|
|
|
т.д.). Название родоначальной структуры составляет |
||||||||
Алкены |
sp |
2 |
при двойной |
= |
сигма и π |
CnH2n |
14n |
|||||||||||
|
КОРЕНЬ слова. |
|
|
|
|
|
||||||||||||
|
|
|
связи |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Алкины |
sp |
|
при тройной |
≡ сигма и две π |
CnH2n-2 |
14n-2 |
2. Функциональные группы и заместители (радикалы) |
|||||||||||
|
|
|
связи |
|
|
|
|
обозначаются ПРЕФИКСАМИ и СУФФИКСАМИ. |
||||||||||
|
|
|
|
|
|
|
|
|
|
! ПОРЯДОК СТАРШИНСТВА ОСНОВНЫХ ГРУПП: |
||||||||
Диены |
sp |
2 |
при двойной |
сигма и |
π |
CnH2n-2 |
14n-2 |
|||||||||||
|
− COOH > − COH > C=O > − OH > −NH2 |
|||||||||||||||||
|
|
|
связи |
|
|
|
|
Выделяют старшую группу, которую называть нужно в |
||||||||||
Циклоалканы |
sp3 |
|
|
|
сигма |
|
CnH2n |
14n |
суффиксе. Все остальные заместители называют в |
|||||||||
|
|
|
|
|
|
|
|
|
|
префиксе в алфавитном порядке. |
|
|
|
|||||
Арены |
sp2 |
в бензольном |
единая 6-электр. |
CnH2n-6 |
14n-6 |
3. В название включают обозначение двойной и |
||||||||||||
|
|
|
кольце |
π-система |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
тройной связи, которое идет сразу после корня. |
||||||||
Моногалогеналканы |
sp3 |
|
|
|
сигма |
|
CnH2n+1X |
14n+1+ M(X) |
||||||||||
|
|
|
|
4. Атомы родоначальной структуры нумеруют с того |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
Одноатомные спирты |
sp |
3 |
|
|
|
сигма |
|
CnH2n+1OH |
14n+18 |
конца углеродной цепи (выбирать нужно самую |
||||||||
|
|
|
|
|
длинную цепь), к которому ближе старшая группа или |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
заместитель. |
|
|
|
|
|
|
||
Альдегиды |
sp3 |
иsp2 (C=O) |
сигма и |
π |
CnH2n+1COH |
14n+30 |
|
|
|
|
|
|
||||||
! При наличии кратной связи главная цепь должна |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
содержать данную связь. Наличие связи главнее замов. |
||||||||
Карбоновые кислоты |
sp3 |
и sp2 (C=O) |
сигма и |
π |
CnH2n+1COOH |
14n+46 |
5. Количество одинаковых заместителей указывается |
|||||||||||
(предельные одноосновные) |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
частицами: ди – два, три – три, тетра – четыре, пента – |
||||||||
|
|
|
|
|
|
|
|
|
|
пять. |
|
|
|
|
|
|
|
|
Простые эфиры |
sp |
3 |
|
|
|
сигма |
|
CnH2n+2O |
14n+18 |
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПРИМЕРЫ НАЗВАНИЙ: |
||||
|
|
|
|
|
|
|
|
|
|
CH3-CH2-CH-CH2-CH2-CH3 |
|
|
|
|||||
Сложные эфиры |
sp3 |
иsp2 (C=O) |
сигма и |
π |
CnH2n+2COO |
14n+46 |
|
|
׀ |
|
|
3-этилгексан |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
C2H5 |
|
|
|
|
||
Первичные амины |
sp |
3 |
|
|
|
сигма |
|
CnH2n+1NH2 |
14n+17 |
5 |
4 |
|
3 |
2 |
1 |
2-амино-4-метил- |
||
|
|
|
|
|
CH3-CH(CH3)-CH2-CH(NH2) COOH |
пентановая кислота |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Аминокислоты |
sp3 |
иsp2 (C=O) |
сигма и |
π |
(NH2)CnH2nCOOH |
14n+61 |
5 |
CH3 |
3 |
2 |
1 |
4 , 4 – диметилпентен -2 |
||||||
|
|
|
|
|
|
|
|
|
|
׀ 4 |
||||||||
|
|
|
|
|
|
|
|
|
|
CH3−C− CH= CH−CH3 |
|
|
|
|||||
Углеводы |
sp |
3 |
и sp |
2 |
(C=O) |
сигма и |
π |
Cn(H2O)m |
12n+18m |
|
|
|
||||||
|
|
|
׀ |
|
|
|
(ен -2 обозначает, что двойная связь |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
находится после 2-го атома углерода) |
|||
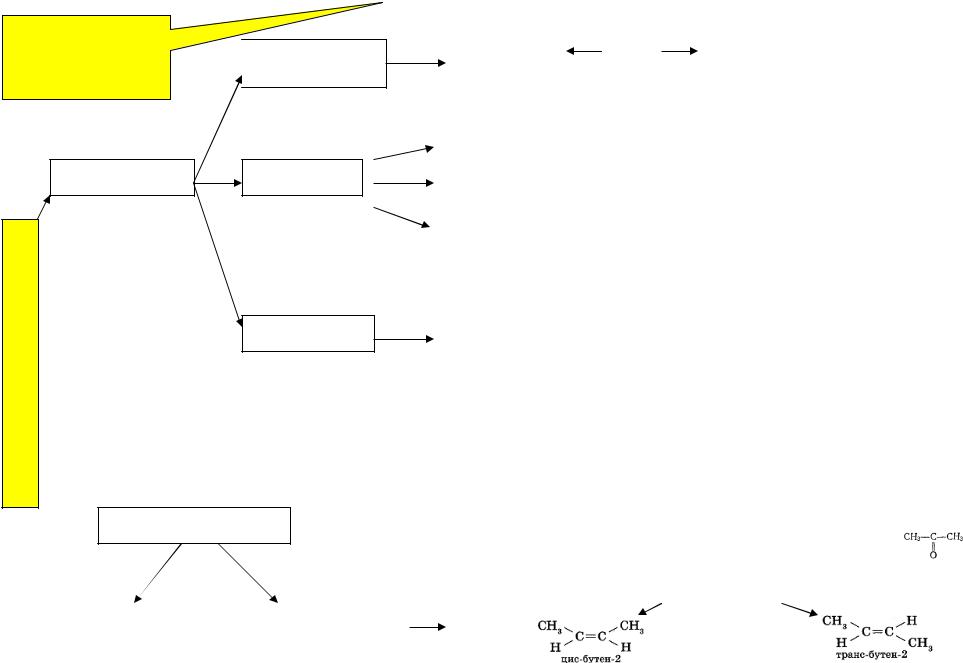
У изомеров состав |
|
|
одинаковый, |
Углеродного |
|
но разное |
||
скелета |
||
строение и свойства |
||
|
||
|
СТРУКТУРНАЯ Положения
И
З
О
Межклассовая
М
Е
Р
И
Я
 ПРОСТРАНСТВЕННАЯ
ПРОСТРАНСТВЕННАЯ
ВИДЫ ИЗОМЕРИИ |
|
|
|
|
|
|
|
|
А13 |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH3-CH2-CH2-CH3 |
|
|
C4H10 |
CH3-CH(CH3)–CH3 |
|
|
|
|
|
|||
|
|
|
бутан |
|
|
|
2-метилпропан (изобутан) |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
CH3-CH2-CH2-CH2-CH3 |
|
|
CH3-CH(CH3)-CH2-CH3 |
CH3 – C – CH3 изомер: |
|
|||||||
|
|
|
пентан |
|
|
изомер: 2-метилбутан |
|
|
CH3 |
2,2-диметилпропан |
|
|||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
1. |
Кратных связей |
: CH3− CH= CH−CH3 |
CH2= CH− CH2−CH3 |
|
|
|
|
|||||
|
|
2. Заместителей: |
|
|
бутен-2 |
|
|
бутен-1 |
|
|
|
|
|
|
|
|
CH3-CH(Cl)-CH2-CH2-CH3 |
CH3-CH2-CH(Cl) -CH2-CH3 |
|
|
|
|
|||||||
|
|
|
|
|
|
2-хлорпентан |
|
3-хлорпентан |
|
|
|
|
|
|
|
|
3. Функциональной группы: |
CH3-CH2-CH2-CH2OH |
CH3-CH2-CH(OH) -CH3 |
|
|||||||||
|
|
|
|
|
|
|
бутанол-1 |
|
бутанол-2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Алкены и |
|
|
|
|
|
Бутен: |
CH3− CH= CH−CH3 |
||||
|
|
циклоалканы |
|
|
CnH2n |
|
Циклобутан: CH2− CH2 |
|||||||
|
|
|
|
|
|
|
|
|
|
׀ |
׀ |
|||
|
|
|
|
|
|
|
|
|
|
CH2 −CH2 |
||||
|
|
|
Алкины и |
|
|
|
|
|
Бутин: |
CH3− C ≡C−CH3 |
||||
|
|
|
алкадиены |
|
|
CnH2n-2 |
|
|||||||
|
|
|
|
|
|
|
|
|
Бутадиен: CH2=CH-CH=CH2 |
|||||
|
|
|
Алканолы и |
|
|
CnH2n+1OH |
Этанол: |
|
CH3-CH2 OH |
|||||
|
|
простые эфиры |
|
|
CnH2n+2O |
Диметиловый эфир: |
CH3 – O – CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
Карбоновые |
|
|
CnH2n+1COOH |
Пропановая кислота: |
CH3-CH2 COOH |
||||||
|
|
|
кислоты и |
|
|
CnH2nO2 |
Метилацетат: |
CH3 COO CH3 |
||||||
|
|
сложные эфиры |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Альдегиды и |
|
|
CnH2n+1COH |
|
Пропаналь: CH3-CH2 COH |
|||||||
|
|
|
кетоны |
|
|
CnH2nO |
|
Пропанон (ацетон): |
||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3− CH= CH−CH3 |
|
Оптическая |
Геометрическая |
||||
|
|
|
|||
(зеркальная) |
|
(цис-транс) |
|
|
|
|
|
|
|
БУТЕН -2 |
|
|
|
||||
|
|
|
|
|

ХИМИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ ВЕЩЕСТВ |
А14, |
|
А15, |
|
А16, |
|
А18, |
В6, |
В7, |
В8, |
С3 |
||
t |
t |
t |
|
|
|
|
|
|
t |
|
|
|
|
Общее свойство всех органических веществ – горение: CxHy + O2 → CO2 + H2O; CxHyOz + O2 → CO2 + H2O; CxHyN + O2 → CO2 + H2O + N2; CxHyCl + O2 → CO2 + H2O + HCl
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
У Г Л Е В О Д О Р О Д Ы |
А14 |
, |
В6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
АЛКАНЫ |
|
|
ЦИКЛОАЛКАНЫ |
АЛКЕНЫ |
|
|
|
АЛКАДИЕНЫ |
|
|
|
АЛКИНЫ |
|
|
|
АРЕНЫ |
|||||||||||||||||||||||||||
|
1. Реакции замещения |
1. Реакции замещения |
|
1. Реакции присоединения |
|
1. Реакции присоединения |
|
1. Реакции присоединения |
1. Реакции замещения |
|||||||||||||||||||||||||||||||||||
|
|
hν |
|
|
|
|
|
|
|
|
|
|
|
|
|
•Гидрирование |
|
•Гидрирование |
|
|
•Гидрирование |
|
ЗАПОМНИ: Арены с |
|
||||||||||||||||||||
|
CH4 + Cl2→ CH3Cl + HCl |
|
|
|
|
|
hν |
|
|
|
|
|
|
Pt |
|
|
|
CH2=CH-CH=CH2+2H2→C4H10 |
|
CH≡CH + H2 → CH2=CH2 |
|
бромной водой не реагируют. |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
CH3Cl + Cl2→ CH2Cl2 + HCl |
|
|
|
|
+ Cl2 → |
Cl + HCl |
C4H8 + H2 →C4H10 |
|
•Галогенирование (по 1,4) |
|
|
CH2=CH2 + H2 → C2H6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
CH2Cl2 + Cl2 → CHCl3 + HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
•Галогенирование |
|
CH2=CH-CH=CH2 + Br2 → |
|
|
•Галогенирование |
|
|
|
кат. |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
CHCl3 + Cl2 → CCl4 + HCl |
2. Реакции присоединения |
CH2=CH2 + Br2 → C2H4Br2 |
|
Br-CH2-CH=CH-CH2-Br |
|
|
CH≡CH + Br2 → Br-CH=CH-Br |
C6H6 + Br2 → C6H5Br + HBr |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
CH3 |
|
|
|
|
CH3 |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
•Гидрогалогенирование |
|
•Гидрогалогенирование (по 1,4) |
|
Br-CH=CH-Br +Br2 → C2H2Br4 |
|
|
|
|
Cl |
|
|
|
|
|
Cl |
|||||||||||||
|
Реакция Коновалова: |
|
|
+ Cl2 |
→ CH2Cl-CH2-CH2Cl |
CH3-CH=CH2 + HCl → |
|
CH2=CH-CH=CH2 + HCl → |
|
•Гидрогалогенирование |
|
|
|
кат. |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
C2H6 + HO-NO2 → C2H5NO2 + H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH -CHCl-CH |
|
|
CH3-CH=CH-CH2Cl |
|
|
CH3-C≡CH+HCl→CH3-CCl=CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
Cl +3 HCl |
|||||||||||||||||||||
|
|
|
|
|
+ HCl → CH3-CH2-CH2Cl |
3 |
|
|
|
|
|
|
|
+3Cl2 → |
|
|
|
|||||||||||||||||||||||||||
|
2. Дегидрирование |
|
|
•Гидратация |
|
|
|
|
|
|
|
|
|
|
|
CH3-CCl=CH2+HCl→CH3-CCl2-CH3 |
2. Реакции присоединения |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3-CH=CH2 + HOH → |
|
|
|
|
|
|
|
|
|
•Гидратация (р. Кучерова) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
t |
|
|
+ H2 |
→ CH3-CH2-CH3 |
CH3 –CH(OH)-CH3 |
|
•Полимеризация |
|
|
CH≡CH + H2O → CH3COH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
CH3-CH3 → CH2=CH2 + H2↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
•Полимеризация |
|
n CH2=CH-CH=CH2 → |
|
|
CH3-C≡CH + H2O → CH3-C-CH3 |
|
|
|
кат. |
|
|
|
|
|
|
|
|
|
|||||||||||
|
3. Крекинг (разложение) |
3. Реакции дегидрирования |
n CH2=CH2 → (..-CH2-CH2-..)n |
|
(…-CH2-CH=CH-CH2-…)n |
|
|
|| |
|
|
|
|
+ 3H2 → |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
||||||||||
|
C7H16 → C3H6 + C4H10 |
|
|
|
|
t,kt |
|
|
|
2. Реакции окисления KMnO4 |
|
2. Реакции окисления KMnO4 |
|
•Полимеризация |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
t |
|
|
|
|
|
→ |
|
|
|
|
+ 3 H2 |
|
|
|
|
|
|
|
|
|
|
|
|
-тримеризация: |
|
|
|
hν |
Cl |
|
|
|
|
Cl |
|||||||||
|
1000°C |
C + 2 H2↑ |
|
|
|
|
|
|
|
|
• в нейтральной среде |
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
Cl |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
CH4 → |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 CH≡CH → C6H6 |
|
|
|
+3Cl2→ |
|
|
|
Cl |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
1000°C |
|
|
|
|
|
|
|
|
|
|
|
|
|
3 CH2=CH2 + 2 KMnO4 + 4 H2O |
|
|
|
|
|
|
|
|
|
НО! |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-димеризация: |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
2CH4 → CH≡CH + 3 H2↑ |
|
|
|
|
|
|
|
|
|
|
|
|
|
→3 HOCH2CH2OH+2MnO2 +2KOH |
|
|
|
|
|
|
|
|
|
|
|
|
hν |
|
|
|
|
|
|
|
|
|
|
||||||
|
4. Изомеризация |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
• в кислой среде |
|
|
2 CH≡CH → HC≡C-CH=CH2 |
C6H5CH3 + Cl2 →C6H5CH2Cl+HCl |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
• в кислой среде |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(до кислот) |
|
|
2. Реакции замещения |
3. Алкилирование |
|||||||||||||||||||||||||
|
|
t,kt |
|
|
|
|
|
|
|
|
|
|
|
|
|
5 CH3-CH=CH-CH3 + 8KMnO4 |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
CH3-CH2-CH2-CH2-CH3 → |
|
|
|
|
|
|
|
|
|
|
|
|
|
+ 12 H2SO4 → 10 CH3COOH + |
|
|
|
|
|
|
|
|
|
HC≡CH + Ag2O → Ag-C≡C-Ag |
C6H6+ CH3Cl → C6H5CH3+ HCl |
||||||||||||||||||
|
CH3-CH-CH2-CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H2O |
C6H6 + CH2=CH2 → C6H5-C2H5 |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8MnSO4 + 4 K2SO4 + 12 H2O |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 CH3-C≡CH+2 Na → H2 + |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2CH3-C≡CNa |
4. Реакции окисления KMnO4 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3. Реакции окисления KMnO4 |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЗАПОМНИ: бензол не |
|
||||||||||||||
|
ЗАПОМНИ: Алканы с р-ром |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
• в кислой среде |
|
окисляется KMnO4. |
|
|||||||||||||||
|
KMnO4 |
и бромной водой не |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(до кислот) |
|
А его гомологи окисляются |
|
|||||||||||||||
|
реагируют (не обесцвечив.) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
до бензойной кислоты (в |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислой среде) |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
К И С Л О Р О Д С О Д Е Р Ж А Щ И Е |
А15, |
|
А16, |
|
В7 |
|
|
|
|
А З О Т С О Д Е Р Ж А Щ И Е |
|
|
|
|
|
|
В8 |
|
|
||||||||||||||||||||
|
СПИРТЫ и ФЕНОЛЫ |
АЛЬДЕГИДЫ, кетоны |
КИСЛОТЫ карбонов. |
|
|
СЛОЖНЫЕ ЭФИРЫ |
|
|
АМИНЫ |
|
АМИНОКИСЛОТЫ |
|||||||||||||||||||||||||||||||||
|
1. с Na |
|
1. Восстановление Н2 |
|
1. Свойства всех кислот: |
|
1. Гидролиз |
|
|
Амины - органические основания |
Амфотерные (кислотно-основные) |
|||||||||||||||||||||||||||||||||
|
2C2H5OH +2 Na →2 C2H5ONa + H2 |
|
|
|
|
|
+H2 →CH3CH2CH2OH |
- с активными металлами (до Н); |
|
CH3COOC2H5 + HOH → |
|
|
1. С водой |
1. С основаниями |
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
HOCH2-CH2OH + 2Na → H2 + |
|
|
|
|
|
- с оксидами любых металлов; |
|
CH3COOH + C2H5OH |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
NaOCH2-CH2ONa |
|
|
|
|
|
|
|
|
|
|
|
|
|
- с основаниями; |
|
|
|
|
|
|
|
|
|
CH3NH2 + HOH→[CH3NH3]OH |
CH2COOH+KOH→CH2COOK+H2O |
||||||||||||||||||
|
2C6H5OH + 2Na → 2C6H5ONa +H2 |
|
|
|
|
|
+ H2 → |
|
- с солями слабых кислот, напр-р: |
|
2. Щелочной гидролиз |
|
|
|
|
|
| |
|
|
|
|
| |
|
|
|
|
|
|
|
|
||||||||||||||
|
2. c NaOH |
|
|
|
|
|
|
2 CH3COOH + Na2CO3 → |
|
CH3COOC2H5 + NaOH → |
|
|
2. С кислотами |
NH2 |
NH2 |
|||||||||||||||||||||||||||||
|
C2H5OH + NaOH ⁄ |
|
|
|
|
|
|
|
|
|
|
|
|
|
(CH3COO)2Na + H2O + CO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3COONa + C2H5OH |
|
|
CH3NH2 + HCl→[CH3NH3]Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
HOCH2-CH2OH + 2NaOH → 2 H2O |
2. Другие реакции присоединения |
- с аммиаком: |
|
|
|
|
|
2. С кислотами– по аминогруппе |
|||||||||||||||||||||||||||||||||||
|
CH3COOH + NH3 → CH3COONH4 |
|
|
|
|
|
|
|
|
|
C6H5-NH2+HCl→(C6H5NH3)Cl |
|||||||||||||||||||||||||||||||||
|
+ NaOCH2-CH2ONa |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(NH3 + HBr → NH4Br) |
|||||||||||||||||

C6H5OH + NaOH → C6H5ONa +H2O |
CH3CH=O + HCl → CH3CH(Cl)-OH |
|||||||||||||||||||||||||
3. c HCl |
|
|
|
|
|
|
|
|
CH3CH=O + HOH → CH3CH(OH)2 |
|||||||||||||||||
C2H5OH+ HCl → C2H5Cl + H2O |
||||||||||||||||||||||||||
HOCH2-CH2OH + 2HCl → 2 H2O + |
CH3CH=O + C2H5OH→ CH3CHOH |
|||||||||||||||||||||||||
ClCH2-CH2Cl |
|
|
|
|
|
|
|
|
||||||||||||||||||
C6H5OH + HCl |
⁄ |
|
|
|
|
|
|
|
|
|
|
|
|
| |
||||||||||||
4. с HNO3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OC2H5 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(полуацеталь) |
||||||
C2H5OH+HONO2→C2H5NO2+H2O |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
HOCH2-CH2OH + 2 HONO2 → |
3. Окисление |
|
|
|
|
|||||||||||||||||||||
2H2O + O2NCH2-CH2NO2 |
|
|
|
|
|
|
||||||||||||||||||||
|
OH |
|
|
|
OH |
|
|
• р. серебряного зеркала |
||||||||||||||||||
|
|
|
O2N |
|
|
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
t |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
+3HONO2 → |
|
|
|
|
|
|
|
+3H2O |
CH3-COH +2[Ag(NH3)2] OH → |
||||||||||||||
|
|
|
|
|
|
|
NO2 |
|
|
CH3-COONH4+2 Ag↓ +3NH3+H2O |
||||||||||||||||
5. Дегидратация спиртов |
(соль аммония) |
|
|
|
|
|||||||||||||||||||||
|
|
|
кат. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C2H5OH →C2H4 + H2O |
• с Cu(OH)2 |
|
|
|
t |
|||||||||||||||||||||
|
|
|
кат. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
2C2H5OH → C2H5-O-C2H5+ H2O |
CH3-COH + 2Cu(OH)2 → |
|||||||||||||||||||||||||
6. Реакция этерификации |
CH3-COOH + Cu2O ↓+ 2H2O |
|||||||||||||||||||||||||
|
|
|
|
|
|
t,kt |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
CH3COOH + C2H5OH → |
|
H2O + |
4. Фенолформальдегидная |
|||||||||||||||||||||||
CH3COOC2H5 |
|
|
|
|
|
|
|
|
конденсация |
|
|
|
|
|||||||||||||
7. Особые свойства |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
t |
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
OH |
||||||
C2H5OH + CuO → CH3-COH +Cu |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
+ H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
+ HCOH + |
|
|
|
→ |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
HOCH2-CH2OH + Cu(OH)2 → |
|
|
|
OH |
|
|
OH |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
OH |
|
OH |
|
(синий) |
|
|
|
|
|
- CH |
- |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Br |
|
|
|
|
Br |
|
|
2 |
|
|
|
|
|
+ H2O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ 3 Br2 → |
|
|
|
|
|
|
+ 3 HBr |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
(бромная вода) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2. Реакция этерификации
t,kt CH3COOH + C2H5OH → H2O + CH3COOC2H5
3. Образование ангидридов:
t,P2O5
2CH3COOH → (CH3CO)2O+H2O 3RCOOH +PCl3→3RCOCl+H3PO3
4. Замещение в радикале
кат. H-CH2COOH + Cl2 → HCl +
Cl-CH2COOH
Особые свойства муравьиной кислоты HCOOH
H2SO4k
HCOOH → CO + H2O
t,NH3
HCOOH + Ag2O → 2Ag +CO2 +H2O
t HCOOH + 2 Cu(OH)2 → Cu2O +
CO2 + H2O
3. с Н2
CH3COOCH3 +2 H2 → C2H5OH + CH3OH
3.Особое свойство анилина |
CH2COOH+HBr → CH2COOH |
|
|||||||||
|
|
|
|
|
|
|
|
|
| |
| |
|
|
|
NH |
|
NH2 |
NH2 |
NH3 |
Br |
||||
|
2 |
Br |
|
|
|
Br |
3. Образование пептидов |
|
|||
|
|
|
|
|
|
|
|
||||
|
|
|
|
+ 3Br2→ |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br +3HBr |
CH2COOH + CH2COOH → H2O+ |
||||||
|
|
|
|
|
|
|
|
|
| |
| |
|
|
|
|
|
|
|
|
|
|
NH2 |
NH2 |
|
|
|
|
|
|
|
|
|
|
O H |
|
|
|
|
|
|
|
|
|
|
|
|| |
| |
|
|
|
|
|
|
|
|
|
|
CH2-C – N-CH2-COOH |
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
4. Все остальные свойства |
|
|
|
|
|
|
|
|
|
|
|
карбоновых кислот также |
|
|
|
|
|
|
|
|
|
|
|
проявляются и у аминокислот. |
||
|
|
|
|
|
|
|
|
|
Например: |
|
|
|
|
|
|
|
|
|
|
|
CH2COOH+ROH→CH2COOR+H2O |
||
|
|
|
|
|
|
|
|
|
| |
| |
|
|
|
|
|
|
|
|
|
|
NH2 |
NH2 |
|
|
|
|
|
|
|
|
|
|
CH2COOH+Na→ CH2COONa+ ½H2 |
||
|
|
|
|
|
|
|
|
|
| |
| |
|
|
|
|
|
|
|
|
|
|
NH2 |
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Б И О Л О Г И Ч Е С К И В А Ж Н Ы Е В Е Щ Е С Т В А
|
|
ЖИРЫ |
|
В7 |
|
УГЛЕВОДЫ |
В8 |
|
БЕЛКИ |
В8 |
|
|
1. Гидролиз |
|
|
|
|
|
|
1. Спиртовые свойства (как многоатомные спирты |
) |
1. Гидролиз |
|
|
|
|
|
|
|
|
|
CH2OH(CHOH)4COH + 5HO-NO2 → 5 H2O + CH2ONO2(CHONO2)4COH |
|
|
|
|||
CH2-O-CO-C17H35 |
|
HOH |
H2C-OH |
|
|
|
2. Альдегидные свойства (только у восстанавливающих сахаров) |
|
+ |
|||
| |
|
|
| |
|
|
|
например, глюкозы |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||
CH2-O-CO-C17H35 |
+ |
HOH → |
HC-OH |
+ 3 C17H35COOH |
CH2OH-(CHOH)4COH+H2 → CH2OH-(CHOH)4CH2OH |
2. Цветные реакции |
|
|
||||
| |
|
|
| |
|
|
|
CH2OH-(CHOH)4COH+2Cu(OH)2 →CH2OH-(CHOH)4COOH+Cu2O+2H2O |
|
|
|||
CH2-O-CO-C17H35 |
|
HOH |
H2C-OH |
|
|
|
CH2OH(CHOH)4COH + Ag2O → CH2OH(CHOH)4COOH + 2Ag |
А) биуретовая: белок + Cu(OH)2 → фиолетовое окрашивание |
||||
2. Щелочной гидролиз |
|
|
|
|
|
|
|
|||||
|
|
|
|
3. Гидролиз ди-и полисахаридов |
|
|
(на наличие пептидных связей) |
|
|
|||
CH2-O-CO-C17H35 |
|
NaOH |
H2C-OH |
|
|
|
C12H22O11 (сахароза)+ H2O → C6H12O6 (глюкоза) + C6H12O6 (фруктоза) |
Б) ксантопротеиновая: белок + HNO3 → желтое окрашивание |
||||
|
|
|
|
Крахмал (C6H10O5)n + nH2O → n C6H12O6 (глюкоза) |
|
|
||||||
| |
|
|
| |
|
|
|
|
|
|
( на наличие бензольных колец) |
|
|
CH2-O-CO-C17H35 |
+ |
NaOH → |
HC-OH |
+ 3 C17H35COONa |
4. Особые свойства |
|
|
|
|
|||
|
|
|
|
|
||||||||
| |
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- спиртовое брожение глюкозы: C6H12O6 →2 C2H5OH + 2 CO2 |
|
|
|
||||
CH2-O-CO-C17H35 |
|
NaOH |
H2C-OH |
|
|
|
|
|
|
|||
|
|
|
|
- посинение иода в реакции с крахмалом |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- нитрование и ацетилирование целлюлозы |
|
|
|
|
|
|
|
|
|
|
|
|
(C6H10O5)n +3n HONO2 → [C6H7O2(ONO2)3]n + 3n H2O |
|
|
|
||

|
|
|
|
|
|
|
МЕХАНИЗМ ХИМИЧЕСКИХ РЕАКЦИЙ В ОРГАНИЧЕСКОЙ ХИМИИ |
В6, |
В7 |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
РАДИКАЛЬНЫЙ |
|
|
|
|
|
|
|
|
И О Н Н Ы Й |
|
|
|
||||
|
|
|
|
замещение |
присоединение |
|
|
|
|
|
|
замещение |
|
присоединение |
отщепление |
||||||
|
|
|
|
|
|
|
|
|
электрофильное |
нуклеофильное |
|
электрофильное |
нуклеофильное |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
hν |
|
|
|
|
|
|
|
|
|
C2H5OH + HCl → |
|
CH2=CH-CH3 + HCl |
CH3-CН=O + |
|
|
|
CH4 + Cl2 → CH3Cl + HCl |
n CH2 = CH2 → |
|
|
|
|
|
|
|
|
CH3 – CH (OH) – CH2 – CH3 |
|||||||||||
C2H6 + HO-NO2 |
|
( - CH2 – CH2 - ) n |
|
|
|
|
|
кат. |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
+ Cl2 → |
C2H5Cl + H2O |
|
→ CH3-CHCl-CH3 |
CH3O H |
→ CH3 – CH = CH – CH3 + |
||||||||||||
C2H5NO2 + H2O |
|
n CH2=CH-CH=CH2 → |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
C6H5 Cl + HCl |
|
|
|
|
|
|
|
|||||||
C6H5 –CH3 + Cl2 |
hν |
(-CH2-CH=CH-CH2-) n |
|
|
|
|
|
H2O |
|||||||||||||
→ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
CH2Cl |
|
|
|
CH3 + 3 Cl2 |
|
кат. |
|
|
|
→ CH3 – CH (OH) |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
→ |
|
|
|
׀ |
|
|
|
||||
|
|
|
|
|
|
|
|
|
׀ |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
+ HCl |
|
|
|
|
|
|
|
|
OCH3 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
||||
|
|
|
|
|
t |
|
|
|
|
Cl |
|
|
Cl |
|
|
|
(полуацеталь) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CxHy + O2 → CO2 |
+ H2O |
|
|
|
|
|
|
|
+ 3HCl |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH3COOH + Cl2 → |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH2ClCOOH + HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Замещение водорода на |
|
|
|
|
|
|
|
|
|
|
Водород присоединяется к |
|
Водород отщепляется от того |
||||||||
другой атом происходит у |
|
|
|
|
|
|
|
|
|
|
тому атому углерода, где |
|
атома углерода, где его было |
||||||||
того атома С, где водорода |
|
|
|
|
|
|
|
|
|
|
водорода большеи было. |
|
меньше. |
||||||||
меньше: |
hν |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 – CH2 – CH3 + Cl2 → |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3 – CH(Cl) –CH3 + HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

ВЗАИМНОЕ ВЛИЯНИЕ АТОМОВ В МОЛЕКУЛАХ |
В6, |
В7, |
В8 |
ЭФФЕКТ
СОПРЯЖЕНИЯ ИНДУКЦИОННЫЙ (в π-связях)
ЭФФЕКТ (смещение электр. плотности
по сигма связям)
Графическое изображение:
Галоген |
Непредельные |
Арены |
Спирты |
Фенол |
Альдегиды |
Карбоновые |
Амины |
производные |
углеводороды |
|
|
|
|
кислоты |
|
|
|
|
Подвижность атома |
|
|
|
Чем больше |
|
Электронная |
Двойную связь нужно |
|
водорода в спиртах даже |
|
Углеводородные |
|
отрицательный заряд |
|
рассматривать как место |
|
хуже, чем в воде. |
|
радикалы влияют на |
|
на атоме азота за счет |
||
плотность смещается в |
|
|
|
|||||
скопления |
|
Причина в том, что |
Кислотные |
уменьшение |
За счет мезомерных |
радикалов, тем более |
||
сторону более |
|
|||||||
отрицательного заряда. |
Перераспределение |
углеводородные |
свойства фенола |
полярности связи |
эффектов в кислотах |
выражены основные |
||
электроотрицательн. |
||||||||
Например, в молекуле |
электронной |
радикалы увеличивают |
сильнее, чем у |
С=О. |
подвижность |
свойства у амина. Т.е. |
||
атома – хлора. Эта |
плотности в |
на атоме кислорола |
карбоксильного |
|||||
связь более полярна, |
пропилена: электронная |
бензольном кольце |
электронную плотность. |
спиртов. |
Следовательно, в |
водорода достаточно |
вторичные амины |
|
плотность в радикале |
||||||||
чем связь С-Н. |
происходит под |
Значит, чем больше сам |
Причинавлияние |
реакции окисления |
большая. |
основнее первичных. |
||
смещена от атомов |
влиянием тех или |
|||||||
Наиболее сильное |
радикал или чем больше |
бензольного |
и присоединения с |
Но чем больше |
(У третичных – уже |
|||
водорода к атому |
иных заместителей. |
|||||||
влияние идет на атомы |
радикалов (как у |
кольца. |
самой большей |
радикал, тем в |
пространственные |
|||
углерода, и на нем |
|
|||||||
водорода, которые к |
|
|||||||
скапливается |
Орто-пара- |
третичных спиртов), тем |
|
скоростью из |
большей степени |
затруднения). |
||
атому хлора ближе. |
|
|||||||
избыточный |
ориентанты: |
хуже кислотные свойства |
|
альдегидов вступает |
гасится частичный |
|
||
Поэтому они |
спиртов. |
|
положит. заряд на |
|
||||
замещаются на другие |
отрицательный заряд. |
1)радикалы |
|
|
метаналь. |
атоме углерода. При |
|
|
атомы в первую |
Под влиянием этого |
(-CH3, -C2H5 …) |
Подвижность водорода |
|
|
этом химическая |
|
|
происходит сдвиг |
|
|
|
|||||
очередь. С ростом |
2) -OH, -NH2 |
повышается в |
|
|
активность кислот |
|
||
электронов к |
|
|
|
|||||
углеродной цепи |
3) -Cl, -Br |
многоатомных спиртах. |
|
|
уменьшается. Значит, |
|
||
центральному атому |
|
|
|
|||||
влияние атома |
|
|
|
|
муравьиная кислота |
|
||
углерода. Он, в свою |
|
|
|
|
|
|||
галогена постепенно |
Мета- |
Еще лучше – при |
|
|
сильнее следующих |
У анилина же |
||
очередь, вызывает |
|
|
||||||
затухает. |
|
|
||||||
сильное смещение π- |
ориентанты: |
введении в радикал |
|
|
гомологов. |
основные свойства |
||
|
|
|
||||||
|
электронов двойной |
-NO2, –COH, |
электроотрицательного |
|
|
|
выражены хуже |
|
|
связи к группе СН2. |
-COOH |
атома, например, хлора: |
|
|
|
(влияние бензольного |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
кольца) |
