
- •1. Введение
- •1. Допастеровская эра (до 1865 г.).
- •2. Послепастеровская эра (1866 – 1940 гг.).
- •3. Эра антибиотиков (1941-1960 гг.).
- •4. Эра управляемого биосинтеза (1961 – 1975 гг.).
- •5. Эра новой биотехнологии (после 1975 г.).
- •Вопросы для самоконтроля
- •2. Живая клетка – основа биологических систем
- •Эндоплазматический ретикулум (эр)
- •Аппарат Гольджи
- •Цитоплазматический матрикс
- •Клеточные органеллы
- •Хлоропласты
- •Клеточная стенка
- •3. Общая характеристика организмов – объектов биотехнологии
- •Эукариоты. Водоросли
- •Принципы подбора биотехнологических объектов
- •Вопросы для самоконтроля
- •4. Основы генетики микроорганизмов
- •Репликация
- •Синтез белка
- •Регуляция генной активности
- •Изменчивость
- •Генетическая рекомбинация
- •Плазмиды
- •Вопросы для самоконтроля
- •5. Метаболизм и принципы его регуляции
- •Анаболизм и катаболизм
- •Углеводы как источник энергии
- •Анаэробное дыхание
- •Брожение
- •Молочнокислое брожение
- •Спиртовое брожение
- •Маслянокислое брожение
- •Аминокислоты как источник энергии
- •Липиды как источники энергии
- •Двууглеродные соединения как источники энергии
- •Рост микроорганизмов на углеводных средах, спиртах, органических кислотах, углеводородах, с1-соединениях
- •Вопросы для самоконтроля
- •6. Ассимиляция у автотрофных и гетеротрофных организмов
- •Биосинтез углеводов
- •Поглощение света и возбуждение пигментов.
- •Биосинтез нуклеиновых кислот
- •Синтез пуриновых нуклеотидов:
- •Регуляция метаболизма
- •Первичные метаболиты
- •Производство аминокислот.
- •Производство органических кислот.
- •Производство спиртов.
- •Производство витаминов.
- •Вторичные метаболиты
- •Антибиотики.
- •Вопросы для самоконтроля
- •7. Питание микроорганизмов
- •Механизм поступления веществ в клетку
- •1) Пассивная диффузия.
- •4) Перенос (транслокация) групп.
- •1.Фотолитотрофия.
- •2. Фотоорганотрофия.
- •3. Хемолитотрофия.
- •4. Хемоорганотрофия.
- •Потребности микроорганизмов в дополнительных питательных веществах
- •Минеральные элементы.
- •Ростовые вещества.
- •Вопросы для самоконтроля
- •8. Рост, размножение и культивирование микроорганизмов
- •Рост бактериальной клетки
- •Размножение бактерий
- •Размножение бактериальной популяции
- •Непрерывные культуры
- •Синхронные культуры
- •Вопросы для самоконтроля
- •9. Подготовка биологических объектов для биотехнологического процесса
- •Гибридизация микроорганизмов
- •1. Получение генов.
- •2. Введение гена в вектор.
- •3. Перенос генов в клетки организма-реципиента.
- •4. Идентификация клеток-реципиентов, которые приобрели желаемый ген (гены).
- •Генетическая инженерия и конструирование новых организмов
- •Улучшение продуцентов, используемых в производстве, методами генетической инженерии
- •Клеточная инженерия
- •Получение гибридных клеток
- •Возможности клеточной инженерии
- •Культуры тканей и клеток высших растений
- •Культуры клеток животных и человека
- •Трансплантация эмбрионов
- •Гибридомная технология
- •Вопросы для самоконтроля
- •10. Культивирование биологических объектов
- •Принципы действия и конструкции биореакторов
- •Системы перемешивания и аэрации
- •1. Аппараты с механическим перемешиванием.
- •2. Аппараты с пневматическим перемешиванием.
- •3. Аппараты с циркуляционным перемешиванием.
- •Лабораторные, пилотные и промышленные биореакторы: проблемы масштабирования
- •Биотехнологические процессы и аппараты периодического и непрерывного действия
- •Периодические процессы.
- •Специализированные типы биотехнологических процессов и аппаратов Анаэробные процессы.
- •Твердофазные и газофазные процессы.
- •Поверхностные процессы.
- •Вопросы для самоконтроля
- •11. Словарь терминов
- •12.Список использованной литературы
Маслянокислое брожение
Маслянокислое брожение – сбраживание углеводов, спиртов, кислот и полисахаридов под влиянием микроорганизмов до масляной кислоты. Брожение происходит в строго анаэробных условиях.
Маслянокислое брожение вызывают бактерии рода Clostridium.
При брожении в больших количествах образуется масляная кислота, сопутствующими продуктами являются этиловый и бутиловый спирты, уксусная кислота, углекислота и водород.
Процесс идет по гликолитическому пути. Пируват распадается на уксусный альдегид и муравьиную кислоту (м.б. уксусная кислота). Из данных продуктов путем конденсации и внутренней перегруппировки образуется масляная кислота.
Суммарная реакция:
![]()
Аминокислоты как источник энергии
Первостепенная роль углеводов как источников энергии в клетке была отмечена. Однако субстратами катаболических процессов могут служить также белки и жиры. При этом энергетическая роль белков вторична. Они бывают востребованы в качестве субстратов, если израсходованы все запасы жиров и углеводов. Жиры – «резервное топливо», поэтому клетка охотно использует их, если исчерпан запас углеводов.
Белки распадаются на аминокислоты, которые сами по себе не являются макроэргическими соединениями, но расщепление некоторых из них сопровождается синтезом АТФ или образованием пировиноградной кислоты.
Под действием эндоферментов – дезаминаз и декарбоксилаз – в клетках микроорганизмов происходит расщепление аминокислот, при этом может отщепляться или аминная (-NH2), или карбоксильная (-СООН) группы. Характер превращения аминокислот зависит, главным образом, от реакции среды в период роста бактерий. В кислой среде происходит декарбоксилирование, в щелочной – дезаминирование, при этом среда нейтрализуется. Обе системы ферментов действуют как механизмы нейтрализации среды, в результате рН сохраняется в физиологических пределах.
При декарбоксилировании образуются амины соответствующих кислот по уравнению:
![]()
В настоящее время обнаружены декарбоксилазы для всех 20 аминокислот. Они характеризуются специфичностью катализируемых реакций.
Дезаминирование аминокислот сопровождается выделением NH3и осуществляется многочисленными и разнообразными реакциями. Разнообразие реакций определяется набором ферментов, присущих тому или иному микроорганизму.
У аэробов распространено окислительное дезаминирование, приводящее к образованию α-кетокислоты:
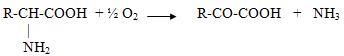
Некоторые микроорганизмы производят дезаминирование аминокислот с образованием пировиноградной кислоты, которая включается в энергетический обмен.

Однако было установлено, что значительная часть энергии микроорганизмам может поставляться из смеси аминокислот, за счет сопряженных окислительно-восстановительных реакций между аминокислотами (реакция Стикленда). При этом одни аминокислоты играют роль доноров, а другие – акцепторов водорода.

Образовавшаяся кетокислота декарбоксилируется, а если это происходит в присутствии фосфата, то образуется макроэргическое фосфорное производное:
![]()
Для аминокислот характерен процесс переаминирования (трансаминирования), когда аминогруппа α-аминокислоты перемещается в α-положение кетокислоты, в процессе которого ферменты трансаминазы переносят аминогруппу с аминокислоты на кетокислоту:

В реакции переаминирования аланина и кетоглутаровой кислоты образуются глутаминовая и пировиноградная кислоты.
Переаминирование широко распространено у бактерий и является важным процессом биологического распада и синтеза аминокислот.
