
- •Калюжний а.П.
- •Тема 1 пом’якшення води…………………………………………………….5
- •І теоритична частина
- •Тема 1. Пом'якшення води
- •1.1. Основи процесів і класифікація методів пом’якшення води
- •1.2. Термічний метод пом’якшення води
- •1.3. Реагентні методи пом’якшення води
- •1.4. Термохімічний метод пом’якшення води
- •Тема 2. Застосування іонного обміну для очистки води
- •2.1. Суть іонного обміну. Характеристика іонітів
- •2.2. Пом’якшення води катіонуванням
- •2.3. Знезалізнення води катіонуванням
- •2.4. Опріснення і знесолення води іонним обміном
- •Тема 3. Дезодорація води
- •3.1. Джерела появи в природних водах присмаків і запахів
- •3.2. Методи усунення запахів, присмаків і токсичних забруднень води
- •Тема 4. Фторування води
- •4.1. Класифікація якості питної води за вмістом іонів фториду
- •4.2. Технологія фторування води. Реагенти
- •4.3. Фтораторні установки
- •Тема 5. Дефторування води
- •5.1. Класифікація методів дефторування води
- •5.2. Сорбційні методи дефторування води
- •5.3. Іонообмінні методи дефторування води
- •Тема 6. Знезалізнення води
- •6.1. Основи процесу знезалізнення води
- •6.2. Безреагентні методи знезалізнення води
- •6.3. Реагентні методи знезалізнення води
- •Технологічні схеми для знезалізнення поверхневих вод:
- •Тема 7. Знезалізнення води
- •7.1. Характеристика методів знесолення і опріснення води
- •7.2. Знесолення води із зміною її агрегатного стану
- •7.3. Знесолення води без зміни її агрегатного стану
- •7.4. Зворотний осмос (гіперфільтрація)
- •Тема 8. Дегазація води
- •8.1. Основи процесів дегазації води
- •8.2. Фізичні методи дегазації води
- •8.3. Хімічні методи дегазації води
- •Тема 9. Електрохімічна обробка води
- •9.1. Основи електрохімічного очищення води
- •9.2. Електродні процеси, що протікають при очищенні води
- •9.3. Класифікація методів електрохімічного очищення води
- •Тема 10. Радіаційне очищення води
- •Тема 11. Очищення води від радіактивних елементів
- •11.1. Радіаційне забруднення води
- •11.2. Методи очищення води від радіоактивних елементів
- •Іі опис розрахунково-графічної роботи
- •Література
- •Ііі указівки до виконання ргр
- •Вибір методу та схеми водопідготовки
- •2. Визначення доз реагентів для вапняно-содового пом’якшення води
- •3. Визначення іонного складу води після реагентного пом’якшення
- •Кількість іонів хлору дCl, уведених із хлорним залізом:
- •4. Катіонітове пом’якшення води
- •4.1. Розрахунок витрат води за різними напрямками
- •4525 М3/добу 700 м3/добу
- •700 М3/добу 660 м3/добу 40 м3/добу 700 м3/добу
- •4.2. Визначення якості води після н- та Na-катіонітових фільтрів
- •4.2.1. Визначення якості фільтрату н-катіонітового фільтра
- •4.2.2. Визначення сольового складу суміші води, яка пройшла
- •4.2.3. Визначення якості фільтрату Na-катіонітового фільтра
- •4.3. Розрахунок Na-катіонітових фільтрів
- •4.3.1. Вибір фільтрів
- •4.3.2. Витрата солі для регенерації Na-катіонітових фільтрів
- •4.3.3. Витрата води на власні потреби Na-катіонітових фільтрів
- •4.3.3.1. Розпушування фільтрів
- •4.3.3.2. Відмивання катіоніту
- •4.3.3.3. Визначення витрати води для приготування
- •4.4. Вибір солерозчинника
- •4.5. Визначення дегазатора
- •4.6. Розрахунок н-катіонітових фільтрів
- •4.6.1. Вибір фільтрів
- •4.6.2. Витрата сірчаної кислоти для регенерації
- •4.6.3. Визначення витрати води на власні потреби
- •4.6.3.1. Розпушування фільтра
- •4.6.3.2. Відмивання катіоніту
- •4.6.3.3. Визначення витрати води для приготування
- •5. Установлення розрахункових витрат станції пом’якшення води
- •1 Робоча
- •1 Резервна
- •Спосок використаних джерел
4.6.3.3. Визначення витрати води для приготування
1-відсоткового розчину кислоти
Витрата води для приготування 1-відсоткового розчину кислоти для регенерації одного фільтра:
WВ = WК – WТК = WК – 100∙ РК / (1000 ∙ mK ∙ К) =
= 4,067 – 100∙40,67/(1000∙75∙1,675) = 4,04 м3.
Годинна витрата води:
qРЕГ = WВ / tРЕГ = 4,04/0,5 = 8,08 м3/год.
Добова витрата води:
Q Н2SO4 = qРЕГ ∙ n ∙ N = 8,08∙0,20∙2 = 3,23 м3/добу.
Для приготування 1-відсоткового розчину кислоти використовується не пом’якшена вода.
Для зберігання кислоти приймається 2 витискувача (робочий і резервний) концентрованої сірчаної кислоти об’ємом 1 м3.
Із витискувача кислота надходить у мірники. Прийнято бак-мірник діаметром 300 мм, об’ємом 50 л.
Подача кислоти із мірника на регенерацію Н-катіонітового фільтра відбувається за допомогою ежектора.
5. Установлення розрахункових витрат станції пом’якшення води
Загальна продуктивність станції визначається за формулою:
Q = Q1 + Q2 + Q3 + Q4,
де Q1 – корисна витрата на господарсько-питне водопостачання;
Q2 – корисна витрата пом’якшеної води;
Q3 – витрата води на власні потреби станції вапняно-содового пом’якшення;
Q4 – витрата води на власні потреби станції H- та Na-катіонітового пом’якшення води.
За будівельними нормами витрати води на власні потреби станцій водопідготовки повинні прийматися не більше ніж 20-30% від корисної витрати і уточнюватися розрахунками [1]. Тому розрахунки починаються з останньої групи споруд – катіонітових фільтрів.
Витрата води Na-катіонітовими фільтрами:
QNa = QВ3 + 0,5∙ QВІД Na + QРОЗ Na = 700 + 0,5∙7,22 + 4,33 = 707,94 м3/добу.
Витрата води дегазатором:
QДЕГ = QНк = 40 м3/добу.
Витрата води H-катіонітовими фільтрами:
QН = QДЕГ + 0,5∙ QВІД Н + QРОЗ H = 40 + 0,5∙1,22 + 1,37 = 41,98 м3/добу.
Витрата води обвідним трубопроводом:
QОБВ = QNa – QН = 707,94 – 41,98 = 665,96 м3/добу.
Витрата води на приготування реагентів:
QРГ = QН2SO4 + QNaCl = 3,23 + 2,10 = 5,33 м3/добу.
Витрата води на іонообмінне пом’якшення:
QІО = QН + QОБВ + QРГ = 41,98 + 665,96 + 5,33 = 713,27 м3/добу.
Витрата пом’якшеної води для питного водопостачання:
QВ1П = 3825 м3/добу.
Витрата води на реагентне пом’якшення:
QРП = 1,2 ∙ (QВ1П + QІО) = 1,2 ∙ (3825 + 713,27) = 5445,92 м3/добу.
Витрата на освітлення води питного водопостачання:
QОСВ = 1,04 ∙ (QВ1 – QВ1П) = 1,04 ∙ (15300 – 5445,92) = 10248,24 м3/добу.
Подача води на станцією пом’якшення:
Q = QОСВ + QРП = 10248,24 + 5445,92 = 15694,16 м3/добу.
Витрати води та її якість після кожного етапу обробки нанесено на схему.
Q
= 15694,16
м3/добу
Ж
= 9 мг-екв/л
Са2+
=
30 мг/л
Мg2+
=
2,4 мг/л
Na+
= 60
мг/л
CO2
= 70
мг/л
SO42-
= 150
мг/л
Cl-
= 70
мг/л
М
= 200
мг/л
Qосв
= 10248,24 м3/добу
Q=15300
м3/добу
ДК
= 31,52 мг/л
ДС
= 327,74 мг/л
ДВ
= 248,23 мг/л
QРП
= 5445,92 м3/добу
Са2+
=
0,25 мг-екв/л
Na+
= 7,91
мг-екв/л
QІО
=
713,27 м3/добу
Ж
= 1 мг-екв/л
Мg2+
=
0,75 мг-екв/л
SO42-
= 4,0
мг-екв/л
Cl-
= 3,71
мг-екв/л
8,8
М<1,5
мг/л
Ж<7
мг-екв/л
рН=6,5-8,5
М<8
мг/л
рН
=
8,8
Л=1,2
мг-екв/л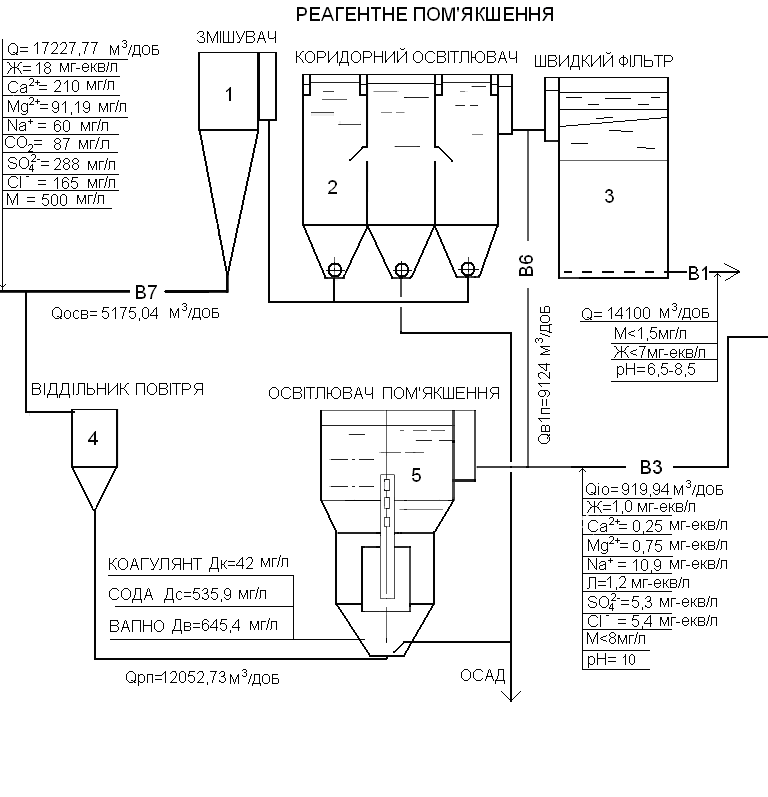

Схема реагентного пом’якшення води
1 – змішувач підготовки питної води; 2 – освітлювач із завислим осадом для підготовки питної води; 3 – швидкий фільтр підготовки питної води; 4 – віддільник повітря, 5 – освітлювач із завислим осадом для реагентного пом’якшення води
