
- •Кафедра прикладной экологии и охраны окружающей среды
- •Характеристика объектов окружающей среды
- •Химический состав, классификация и некоторые особенности природных вод
- •Подразделения вод согласно минерализации
- •Состав поверхностых вод суши
- •Характерные интервалы концентрации биогенных элементов в поверхностных водах суши (в скобках пдк, мг/л)
- •Зависимость содержания nh3 от рН воды при разных температурах
- •Содержание микроэлементов в поверхностных водах суши и биометаллах
- •Молекулярные массы комплексных соединений микроэлементов
- •Характерные интервалы концентраций органических соединений природного происхождения в поверхностных водах суши в мг с/л.
- •Состав подземных вод
- •Состав воздуха и атмосферных осадков
- •Химический состав чистого воздуха
- •Химический состав почв.
- •Группы водосборной площади Днепра
- •Химический состав донных отложений
- •Содержание основных компонентов и микроэлементов в донных отложениях
- •Общая схема анализа и основные этапы
- •Характеристика методов анализа
- •Общая характеристика методов анализа объектов окружающей среды
- •Особенности анализа воздуха
- •Отбор проб
- •Подготовка проб к анализу.
- •Особенности анализа почв и донных отложений.
- •Отбор проб и их подготовка к анализу
- •Основные этапы анализа
- •Особенности анализа природной воды. Виды проб и техника их отбора
- •Отбор проб с водных объектов
- •Консервация, транспортировка и хранение проб воды
- •Определение химических ингредиентов в растворённом состоянии, коллоидно-дисперсной форме и взвесях
- •Концентрирование микрокомпонентов
- •Зависимость количества экстракций n для 99 % извлечения веществ от коэффициента разделения (d) и кратности концентрирования (vвод./vорг.)
- •Удаление веществ, мешающих анализу
- •Автоматизация анализа природных вод
- •Статистическая обработка результатов анализа
- •Зависимость t от n при различных р
Концентрирование микрокомпонентов
Концентрирование микропримесей неорганических и органических соединений целесообразно проводить после предварительной фильтрации воды или центрифугирования, чтобы избавиться от нерастворённых соединений.
Для концентрирования микрокомпонентов используют 2 группы методов.
К первой из них принадлежит выпаривание и вымораживание, которые приводят к уменьшению общего объема пробы воды и, как следствие, к увеличению концентрации всех ингредиентов.
Общий недостаток этих методов заключается в том, что при значительной концентрации главных ионов они выпадают в осадок в виде солей, например, СаСО3, СаSO4 и т.д. При этом на поверхности осадка способны сорбироваться органические и неорганические микропримеси, вследствие чего химический состав и содержание растворённых компонентов изменяется.
При выпаривании пробы воды из неё могут выделяться не только осадки солевых компонентов, но и отгоняться летучие органические соединения. Установлено, например, что в период цветения днепровской воды, когда она насыщена органическими соединениями, результаты определения химического употребления О2 в кипяченной в течение 15 – 20 мин. воды могут быть на 30 – 40 % меньше от результатов анализа некипячённой пробы воды, т.е. выпаривание природной воды с целью концентрирования микропримесей может изменять её химический состав, особенно концентрацию лёгких органических веществ.
Метод вымораживания с целью концентрирования в меньшей степени влияет на химический состав пробы воды. Вымораживать воду можно в холодильнике. Следует иметь в виду, что при вымораживании определённое количество растворённых в природной воде веществ переходит в фазу льда, причём чем больше степень концентрирования, тем более значительные потери концентрата. Поэтому вымораживать пробу воды с уменьшением её объема более чем в 8 – 10 раз не рекомендуется.
Ко второй группе принадлежат методы концентрирования, которые базируются на экстракции, сорбции, соосаждении или электрохимическом выделении микрокомпонентов без изменения общего объема пробы воды. Эти методы позволяют не только концентрировать микрокомпоненты, но также отделять их от матрицы и веществ, которые мешают анализу, поэтому они являются более эффективными в сравнении с выпариванием и вымораживанием.
Экстракционное концентрирование состоит в том, что определённый объем природной воды (vвод.) энергично взбалтывают в делительной лейке с меньшим объёмом органического растворителя, который практически не смешивается с водой, до установления равновесия. Конечно, для этого необходимо не более 3 – 5 минут. Микрокомпоненты в виде органических соединений или комплексов ионов металлов, которые в безводном растворителе растворяются лучше, чем в воде, переходят в органическую фазу. Распределение компонента А между двумя фазами описывается коэффициентом разделения:
![]() (11)
(11)
где [А]орг. и [А]вод. – равновесные концентрации А в орг. и водной фазе соответственно.
Если микрокомпонент содержится в водном растворе или в органической фазе в различных молекулярных или ионных формах (например, уксусная кислота в водном растворе содержится в форме НАс и Ас, а в неводном – в виде димеров (НАс)2 и мономеров НАс), то [А]орг. и [А]вод. равны сумме всех форм в каждой из фаз.
Поэтому экстракции с практической точки зрения удобнее характеризовать через степень экстракции R (фактор извлечения), %
![]() (12)
(12)
где СА – общая концентрация компонента А в водной фазе до экстракции.
Величины R и D связаны между собой уравнениями
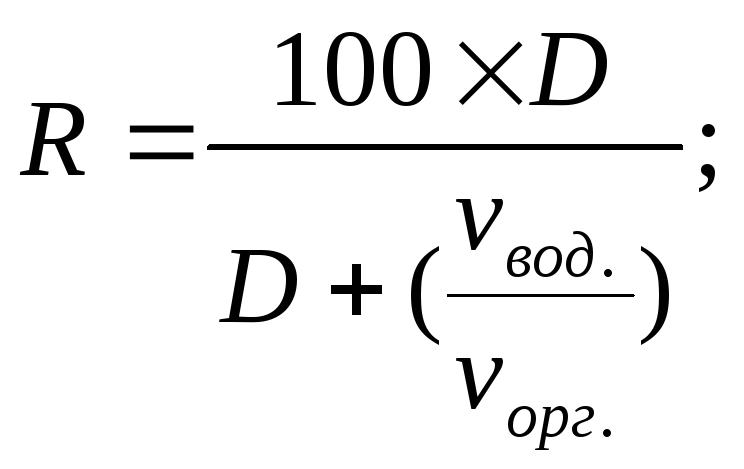
![]() (13)
(13)
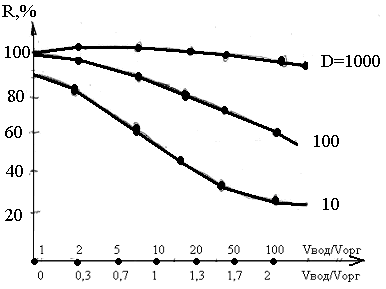
Рис. 6. Зависимость степени экстракции R, %, от кратности концентрирования Vвод/Vорг и коэффициента распределения D.
Соотношение объемов водной и органической фаз при практически полной экстракции равняется кратности концентрирования.
Из уравнения (13) вытекает, что степень экстракции зависит не только от значения коэффициента распределения, но и от соотношения объемов водной и органической фаз, как показано на рис. 6. Из него видно, что при одноразовой экстракции ≥ 99 % - го извлечения вещества в органическую фазу при кратности концентрирования vвод./vорг. ≤ 10 можно достичь лишь в системах, в которых коэффициент распределения D ≥ 1000. При меньших значениях D или при увеличении отношения vвод./vорг. значительное количество распределенного вещества остаётся в водной фазе.
Во многих случаях для концентрирования не удаётся найти экстракционных систем с высокими значениями D. В таком случае для практически полного извлечения вещества следует использовать многоразовую экстракцию (например, так делают при экстракционном концентрировании фосфорорганических пестицидов). Расчёт количества экстракций n, необходимых для практически полного извлечения, можно провести по формуле:
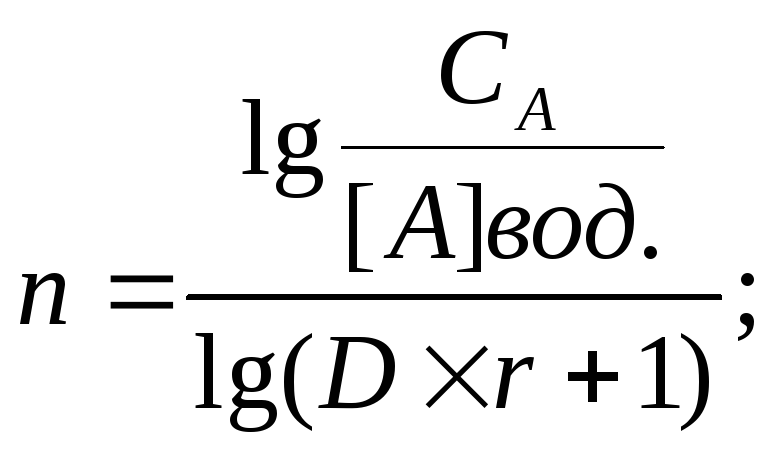 (14)
(14)
где СА – общая концентрация вещества А в пробе до экстракции;
[А]вод. – равновесная концентрация в водной фазе после экстракции;
r = vвод./vорг.
Для 99 % - ой экстракции эта формула имеет вид
![]() (15)
(15)
Таблица 13
