
glava7
.pdf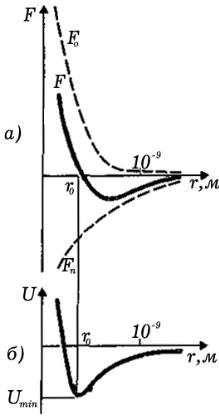
Глава 7
Реальные газы, жидкости и твердые тела
§ 39
Силы и потенциальная энергия межмолекулярного взаимодействия
При повышении давления газа происходит уменьшение среднего расстоя-
ния между молекулами, поэтому в этих условиях необходимо учитывать объем молекул и взаимодействие между ними. Так, в 1 м3 газа при нормальных условиях содержится 2,68×1025 молекул, занимающих объем примерно 10–4 м3, которым по сравнению с объемом газа можно пренебречь. При давлении 500 МПа объем мо-
лекул составляет уже половину всего объема газа. Таким образом, при высоких
давлениях и низких температурах модель идеального газа уже неприемлима.
При рассмотрении реальных газов необходимо учитывать силы межмолекулярного взаимодейст-
вия, которые проявляются на расстояниях £ 10−9 м и быстро убывают с увеличением расстояния. Такие силы называются короткодействующими.
Между молекулами вещества одновременно действуют силы притяжения Fn и отталкивания Fo ,
зависимость которых от расстояния качественно
приведена на рисунке. r = r0 соответствует результи-
рующей силе F = 0 .
Элементарная работа δA силы F при увеличе-
нии расстояния между молекулами на dr соверша-
ется за счет уменьшения взаимной потенциальной
энергии молекул U , т.е.
δA = Fdr = −dU . |
(39.1) |
Критерием различных агрегатных состояний вещества является соотноше- |
|
ние величин Umin и kT . Umin – |
наименьшая потенциальная энергия взаимодейст- |

вия молекул – определяет работу, которую нужно совершить против сил притя-
жения для того, чтобы разъединить молекулы, находящиеся в равновесии ( r = r0 ).
Если Umin << kT , то вещество находится в газообразном состоянии. Если
Umin >> kT, то вещество находится в твердом состоянии. Если Umin ≈ kT , то ве-
щество находится в жидком состоянии.
§ 40
Уравнение Ван-дер-Ваальса
Учитывая собственный объем молекул и сил межмолекулярного взаимодей-
ствия, голландский физик И. Ван-дер-Ваальс (1837–1923) вывел уравнение со-
стояния реального газа.
1. Учет собственного объема молекул. Наличие сил отталкивания сводится к тому, что фактический свободный объем, в котором могут двигаться молекулы реального газа
будет не Vm , а Vm −b, где b – объем, занимаемый самими молекулами. Опреде-
лим этот объем на примере двух молекул, показанном на рисунке. Центры моле-
кул не могут приблизиться друг к другу на расстояние меньшее диаметра молекул d . Это означает, что центр первой молекулы не может находиться в сферическом объеме b вблизи второй молекулы. Определим этот объем
b = |
4 |
πd3 |
= |
4 |
π8r3 = 8 |
4 |
πr3 |
= 8Vмол , |
|
|
|
|
|||||||
3 |
|
3 |
|
3 |
|
|
|||
где r – радиус молекулы, |
Vмол – |
объем одной молекулы. Таким образом, объем b |
|||||||
равен учетверенному собственному объему молекул.
2. Учет притяжения молекул. Действие сил притяжения газа приводит к появлению дополнительного давления на газ, называемого внутренним давлени-
ем
p′ = |
a |
, |
(40.1) |
2 |
|||
|
V |
|
|
|
m |
|
|
где a – постоянная Ван-дер-Ваальса, характеризующая силы межмолекулярного
взаимодействия.
Введя эти поправки, уравнение для одного моля газа будет иметь вид
(p + |
a |
)(V −b) = RT . |
(40.2) |
|
V2 |
||||
|
m |
|
||
|
m |
|
|
Для произвольного количества вещества ν это уравнение с учетом V = νVm , при-
мет вид
(p + ν2 a)( V −b) = RT,
V2 ν
или
(p + ν2 a)(V − νb) = νRT.
V2
§ 41
Изотермы Ван-дер-Ваальса
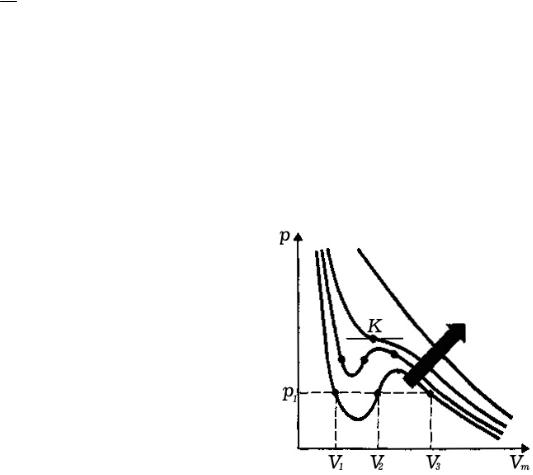
Для исследования поведения реального газа рассмотрим изотермы Ван-дер-Ваальса –
кривые зависимости p от Vm при заданных T ,
определяемые уравнением Ван-дер-Ваальса
(71.2) для моля газа. Эти кривые (на рисунке рас-
сматриваются для четырех различных температур) имеют довольно своеобразный характер. При высоких температурах ( T > Tk )
изотерма реального газа отличается от изотермы идеального газа только некото-
рым искажением ее формы, оставаясь монотонно спадающей кривой. При некото-
рой температуре Tk на изотерме имеется лишь одна точка перегиба К. Эта изо-
терма называется критической, соответствующая ей температура Tk – критиче-
ской температурой. Критическая изотерма имеет лишь одну точку перегиба К,
называемую критической точкой; в этой точке касательная к ней параллельна оси абсцисс. Соответствующие этой точке объем Vk и давление pk называются также критическими. Состояние с критическими параметрами ( pk , Vk , Tk ) назы-
вается критическим состоянием. При низких температурах (T < Tk ) изотермы имеют волнообразный участок, сначала монотонно опускаясь вниз, затем моно-
тонно поднимаясь вверх и снова монотонно опускаясь.
Для пояснения характера изотерм преобразуем уравнение Ван-дер-Ваальса
(71.2) к виду
pV3 |
−(RT + pb)V2 |
+ aV −ab = 0 . |
(41.1) |
m |
m |
m |
|
Уравнение (41.1) при заданных p и T является уравнением третьей степени |
|||
относительно Vm ; следовательно, оно может иметь либо три вещественных кор-
ня, либо один вещественный и два мнимых, причем, физический смысл имеют лишь вещественные положительные корни. Поэтому первому случаю соответст-
вуют изотермы при низких температурах (три значения объема газа V1 , V2 и V3
отвечают одному значению давления p1 ), второму случаю – изотермы при высо-
ких температурах.
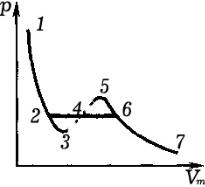
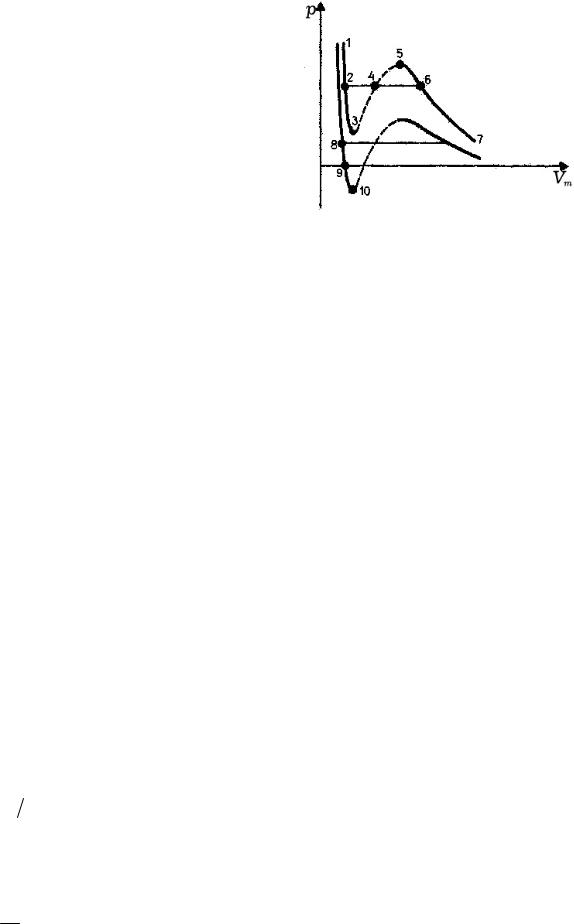
Рассматривая различные участки изотермы при
T < Tk , из рисунка видно, что на участках 1–3 и 5– 7
при уменьшении объема Vm давление p возрастает,
что естественно. На участке 3–5 сжатие вещества приводит к уменьшению давления; практика же
показывает, что такие состояния в природе не осуществляются. Наличие участка
3–5 означает, что при постепенном изменении объема вещество не может оста-
ваться все время в виде однородной среды; в некоторый момент должно насту-
пить скачкообразное изменение состояния и распад вещества на две фазы. Таким образом, истинная изотерма будет иметь вид ломаной линии 7– 6– 2– 1. Часть 7–6
отвечает газообразному состоянию, а часть 2–1 – жидкому. В состояниях, соот-
ветствующих горизонтальному участку изотермы 6– 2, наблюдается равновесие жидкой и газообразной фаз вещества. Вещество в газообразном состоянии при температуре ниже критической называется паром, а пар, находящийся в равнове-
сии со своей жидкостью, называется насыщенным.
Для нахождения критических параметров подставим их значения в уравне-
ние (41.1) и запишем
p |
V3 −(RT + p |
b)V2 + aV −ab = 0 . |
(41.2) |
k |
k k |
|
|
Поскольку в критической точке все три корня совпадают и равны Vk , уравнение приводится к виду
pk (V − Vk )3 = 0 ,
или
p |
V3 −3p V V2 |
+3p V2 V − p V3 |
= 0 . |
(41.3) |
|
k |
k k |
k k |
k k |
|
|
Так как уравнения (41.2) и (41.3) тождественны, то в них должны быть равны ко-
эффициенты при неизвестных соответствующих степеней. Поэтому можно запи-
сать
pk Vk3 = ab , 3pk Vk2 = a , 3pk Vk = RTk + pkb .
Решая полученные уравнения, найдем
V = 3b , p |
k |
= a (27b2 ) , T = 8a (27Rb) . |
(41.4) |
k |
k |
|
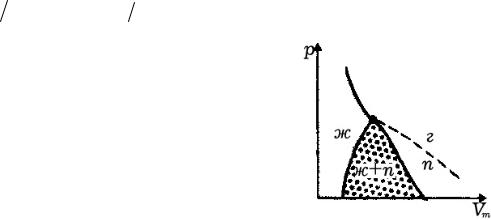
Если через крайние точки горизонтальных участков семейства изотерм провести линию, то, как это показано на рисунке, получится колоколообразная кри-
вая, ограничивающая область двухфазных состояний вещества. Эта кривая и критическая изотерма делят диаграмму p , Vm под изотермой на три области: под ко-
локолообразной кривой располагается область двухфазных состояний (жидкость и насыщенный пар), слева от нее находится область жидкого состояния, а справа
– область пара. Пар отличается от остальных газообразных состояний тем, что при изотермическом сжатии претерпевает процесс сжижения. Газ же, при темпе-
ратуре выше критической не может быть превращен в жидкость ни при каком давлении.
Сравнивая изотерму Ван-дер-Ваальса с изотермой реального газа (верхняя кривая на рисунке), видим, что последняя имеет прямолинейный участок 2– 6, со-
ответствующий двухфазным состояниям вещества. Правда, при некоторых
условиях могут быть реализованы состояния,
изображаемые участками ван-дер-ваальсовой изотермы 5– 6 и 2– 3. Эти неустойчивые со-
стояния называются метастабильными. Уча-
сток 2– 3 изображает перегретую жидкость,
5– 6 – пересыщенный пар. Обе фазы ограни-
ченно устойчивы.
При достаточно низких температурах изотерма пересекает ось Vm , перехо-
дя в область отрицательных давлений (нижняя кривая на рисунке). Вещество под отрицательным давлением находится в состоянии растяжения. При некоторых ус-
ловиях такие состояния также реализуются. Участок 8–9 на нижней изотерме со-
ответствует перегретой жидкости, участок 9–10 – растянутой жидкости.
Задача 1. Найдите температуру и плотность аргона в критическом состоя-
нии, считая газ ван-дер-ваальсовским. Постоянные Ван-дер-Ваальса для этого газа
равны 0,137 Па×м6/моль2 и 3,23×10–5 |
м3/моль. |
|||||
Дано: |
|
|
|
Решение |
||
|
|
|
||||
M = 0,04 кг/моль |
Температура газа в критическом состоянии опре- |
|||||
a = 0,137 Па×м6 /моль2 |
деляется по формуле |
|||||
b = 3,23×10−5 м3/моль |
T = |
8a |
. |
|
||
|
||||||
|
|
|
k |
27Rb |
||
|
|
|
|
|||
Tk = ? ρk = ? |
|
Подставим числовые значения |
||||
|
|
|
||||
|
|
|
|
|
||
|
|
8 ×0,137 Па×м6/моль2 |
||||
Tk = |
|
|
|
|
|
= 151 К. |
|
|
|
|
|
||
27 |
×8,31 Дж/(моль×К) ×3,23×10−5 м3/моль |
|||||
Плотность газа в критическом состоянии определим по формуле |
||||||
ρk = M Vk , |
|
|
|
|
||
где Vk = 3b – |
молярный объем газа в критическом состоянии. Тогда плотность га- |
|||||
за будет определяться выражением
rk = M . 3b

Подставим числовые значения
rk |
= |
|
0,04 кг/моль |
= 413 |
кг/м3 . |
||
|
×3,23×10−5 |
м3 |
/моль |
||||
|
3 |
|
|
||||
Задача 2. Вычислите постоянные Ван-дер-Ваальса для аргона, если его кри-
тическая температура 151 К и критическое давление 4,86 МПа.
Дано: |
|
|
|
|
СИ |
|
|
|
|
Решение |
|||||
pk = 4,86 МПа |
|
4,86×106 Па |
Критическая температура и критическое дав- |
||||||||||||
Tk =151 К |
|
|
|
|
|
|
|
ление газа определяются следующими формулами |
|||||||
|
|
|
|
|
|
|
|
|
|
8a |
|
|
a |
|
|
a = ? b = ? |
|
|
|
|
|
|
|
Tk = |
и pk |
= |
. |
||||
|
|
|
|
|
|
|
|
27b2 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
27Rb |
|
|
||
|
|
|
|
|
|
|
|
|
|
Найдем отношение температуры к давлению |
|||||
|
T |
|
8a |
|
27b2 |
8b |
|
|
|
|
|
|
|||
|
k |
= |
|
|
|
|
= |
|
. |
|
|
|
|
|
|
|
|
27Rb |
|
|
|
|
|
|
|
|
|||||
|
pk |
|
|
a |
R |
|
|
|
|
|
|
||||
Выразим из этого равенства постоянную b
b = RTk . 8pk
Подставим числовые значения
b = 8,31 Дж/(моль× К) ×151 К = 3,23×10−5 м3/моль. 8 × 4,86 ×106 Па
Постоянную a выразим из формулы для критического давления
a = 27pkb2 .
Подставим числовые значения
a = 27 × 4,86 ×106 Па ×(3,23×10−5 м3/моль)2 = 0,137 Па ×м6 /моль2 .
Задача 3. Критическая температура углекислого газа равна 304 К и крити-
ческое давление 73 атм. Считая газ ван-дер-ваальсовским, найдите критический молярный объем углекислого газа.
Дано: |
СИ |
Решение |
p = 73 атм |
7,3·106 Па |
Критический молярный объем газа определяется |
k |
|
|
Tk = 304 К |
|
по формуле |
|
|
Vk = 3b, |
Vk = ? |
|
|
|
|
|
|
|
|
где b – постоянная Ван-дер-Ваальса. Для того, чтобы ее найти запишем выражения для критического давления и критической температу-
ры газа
p = |
a |
и T = |
8a |
. |
27b2 |
|
|||
k |
k |
27Rb |
||
|
|
|||
Найдем отношение критической температуры к критическому давлению
Tk = 8a 27b2 = 8b . pk 27Rb a R
Выразим из этого равенства постоянную b
b = |
RTk |
и |
|
8pk
подставим в формулу для критического молярного объема
Vk = 3RTk . 8pk
Подставим числовые значения
Vk = 3×8,31 Дж/(моль×К) ×304 К = 1,3×10−4 м3/ммол. 8 ×7,3×106 Па
§ 42
Внутренняя энергия реального газа
Внутренняя энергия реального газа складывается из кинетической энергии теплового движения его молекул CVT и потенциальной энергии межмолекуляр-
ного взаимодействия. Потенциальная энергия реального газа обусловлена только силами притяжения между молекулами. Наличие сил притяжения приводит к воз-
никновению внутреннего давления

p′ = a . Vm2
Работа, которая затрачивается для преодоления сил притяжения, действующих между молекулами газа, равна
′ |
= δU , или dU = |
a |
|
a |
|
|
V2 |
dVm , откуда U = - V . |
|||||
δA = p dVm |
||||||
|
|
m |
|
m |
||
Учитывая это выражение, получаем внутреннюю энергию для моля реаль-
ного газа
Um |
= CVT - |
a |
. |
(42.1) |
|
||||
|
|
Vm |
|
|
Если газ расширяется без теплообмена с окружающей средой ( δQ = 0 ) и не совершает работы ( δA = 0 ), то из I начала термодинамики следует
U1 = U2 . |
(42.2) |
Для идеального газа из этого равенства следует, что T1 = T2 . В случае реального газа из равенства (42.2), учитывая, что для моля газа
U = C |
T − |
|
a |
и U |
|
= C |
T − |
a |
, |
(42.3) |
||||||
|
|
|
|
|
||||||||||||
1 |
V |
1 |
|
|
V |
|
|
|
2 |
|
V 2 |
V |
|
|||
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
2 |
|
|
получаем |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
1 |
|
|
1 |
|
|
|
|
|
||
T1 - T2 |
= |
|
|
|
- |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
V1 |
V2 |
. |
|
|
|
|
||||||
|
|
CV |
|
|
|
|
|
|
|
|||||||
Так как V2 > V1 , |
то T1 |
> T2 , т.е. реальный газ при адиабатическом расширении в |
||||||||||||||
вакуум охлаждается. При адиабатическом сжатии реальный газ нагревается. |
|
|||||||||||||||
Задача. Теплоизолированный сосуд объемом 2 л разделен перегородкой на две равные части. В одной половине находится 2 моля углекислого газа, во второй половине газа нет. Перегородку мгновенно убирают, и газ заполняет весь объем.
На сколько изменится температура газа? Для углекислого газа
a = 0,367 Па×м6/моль2 .

Дано: |
Решение |
|
V = 0,002 м3 |
Согласно первого начала термодинамики |
|
ν = 2 моля |
Q = A + U . |
|
|
||
i = 6 |
Если нет теплообмена с окружающей средой ( Q = 0 ) и |
|
a = 0,367 Па×м6 /моль2 |
газ расширяется в пустоту ( A = 0 ), тогда |
|
|
U = U2 − U1 = 0 . |
|
T1 −T2 = ? |
||
|
||
|
|
Отсюда получаем, что U2 = U1 . Запишем выражения для внутренней энергии реального газа до его расширения и после
|
|
|
|
a |
|
|
|
|
|
|
a |
|
|
|
U = ν C T − |
|
и U |
|
= ν C T |
− |
|
, |
|
||||||
|
2 |
|
|
|||||||||||
1 |
|
|
V 1 |
|
|
|
V |
2 |
|
|
|
|
|
|
|
|
|
|
Vm1 |
|
|
|
|
|
Vm2 |
|
|
||
где C = |
i |
R – |
молярная теплоемкость газа при постоянном объеме; V |
= V ν – |
||||||||||
|
||||||||||||||
V |
2 |
|
|
|
|
|
|
|
|
|
|
|
m1 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
молярный объем газа до его расширения; |
|
Vm2 = V2 ν – молярный объем газа по- |
||||||||||||
сле расширения. Из равенства начальной и конечной внутренних энергий имеем
C T - |
|
a |
= C T - |
a |
. |
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
V |
1 |
Vm1 |
|
|
|
|
V |
2 |
|
|
Vm2 |
|
|
|
|
|
|
|
|
|
|||||||
Выразим отсюда разность температур |
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
a |
|
|
|
|
|
|
1 |
|
|
2na |
|
|
|
1 |
|
||||||||
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
1 |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
T1 - T2 = CV Vm1 - Vm2 = |
iR V1 |
- V2 . |
|||||||||||||||||||||||||
Принимая во внимание, что V1 = V 2 |
и V2 = V , получаем |
||||||||||||||||||||||||||
T - T = |
2na |
|
2 |
- |
1 |
= |
2na |
. |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
1 |
2 |
|
|
iR V |
|
|
V |
|
iRV |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
Подставим числовые значения |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
T - T = |
|
2 × 2 моля×0,367 Па×м6 /моль2 |
= 15 К. |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
1 |
2 |
|
|
6 ×8,31 Дж/(моль×К) ×0,002 м3 |
|
|
|||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||
Таким образом, температура углекислого газа в результате расширения умень-
шится на 15 К.
