
- •Министерство образования республики беларусь
- •Оглавление
- •Список сокращений
- •Введение
- •Литературный обзор
- •Характеристика воды как объекта исследования
- •Исторические данные
- •Молекула воды
- •Строение воды
- •Физические свойства воды
- •Химические свойства воды
- •Вода – среда жизни
- •Значение воды в жизни человека и общества
- •Значение воды в химическом производстве и технологии лс.
- •Вода в химической промышленности
- •Отделение ндф [17]
- •Общая характеристика производимой продукции
- •Описание технологического процесса очистки сточных вод
- •Нитрификация
- •Денитрификация
- •Отделение бхо [18]
- •Общая характеристика производимой продукции
- •Описание технологического процесса
- •Вода на фармацевтическом предприятии
- •Предварительная подготовка и получение
- •Дистилляция
- •Ионный обмен
- •Фильтрация
- •Электродеионизация
- •Обратный осмос
- •Экспериментальная часть
- •Стандарт качества воды на химическом предприятии оао «Гродно Азот» и исследования образцов на различных участках производства
- •Водно-химический режим котлов Общие требования
- •Требования к качеству питательной воды [7]
- •Требования к качеству котловой воды
- •Оборотное водоснабжение
- •Водооборотная система
- •Проблемы, связанные с оборотной водой
- •Коррозия
- •Образование солей
- •Загрязнение
- •Защита от коррозии
- •Защита от солеотложений
- •Защита от загрязнения
- •Стандарт качества воды и исследование образцов на ооо «Фармтехнология»
- •Технические характеристики установки
- •Устройство системы для получения воды очищенной
- •Принцип работы
- •Изложение технологического процесса
- •Стандарты качества воды гф рб
- •Вода очищенная [1]
- •Производство
- •Проведение измерений
- •Испытания
- •Вода очищенная в контейнерах [1]
- •Испытания
- •Вода для инъекций [1]
- •Производство
- •Проведение измерений
- •Испытания
- •Вода для инъекций стерильная [1]
- •Испытания
- •Вода высокоочищенная [1]
- •Производство
- •Проведение измерений
- •Испытания
- •Литература
Химические свойства воды
Вода
– термически устойчивое вещество. Она
выдерживает нагревание до температуры
1000 и лишь при температуре свыше 1000
и лишь при температуре свыше 1000 частично разлагается на водород и
кислород:
частично разлагается на водород и
кислород:
2
Н2О
 2Н2
+ О2
(2)
2Н2
+ О2
(2)
Термическое
разложение (иначе термическая диссоциация)
воды протекает с поглощением теплоты,
а поэтому, согласно принципу Ле Шателье,
чем выше температура, тем больше степень
диссоциации. Но все же она очень мала и
даже при 2000 составляет не более 2% [4].
составляет не более 2% [4].
Вода
– весьма реакционное способное вещество.
Она реагирует с оксидами многих металлов
(Na2O,
CaO
и др.) и неметаллов (Cl2O,
[Al2(SO4)3
 18H2O]),
вступает во взаимодействие с активными
металлами (Na,
K
и др.).
18H2O]),
вступает во взаимодействие с активными
металлами (Na,
K
и др.).
Вода – катализатор многих химических реакций, и иногда для прохождения реакции необходимы хотя бы ее следы. Так, следы воды нужны для взаимодействия натрия с кислородом в атмосфере воздуха, для реакции фтористого водорода со стеклом и хлора с металлами.
С
веществами реакционно малоспособными,
находящимися обычно в газообразном
состоянии, вода образует ряд интересных
соединений. Молекулы газообразного
вещества проникают в пустоты структуры
ассоциатов воды и образуют соединения,
называемые соединениями включения или
клатратами. Такие соединения неустойчивы
и легко разлагаются при повышении
температуры. Примеры клатратов являются
СН4
 6 Н2О,
С2Н5Cl
6 Н2О,
С2Н5Cl
 15
Н2О
и др.
15
Н2О
и др.
Тяжелая вода D2О по своим химическим свойствам заметно отличается от обычной воды. Реакции с тяжелой водой, как правило, протекают медленее [4].
Таблица 5 – Химические свойства воды [15]
|
С простыми веществами |
активный металл* + вода = щелочь + водород 2Na
+ 2H2O
= 2NaOH
+ H2
металл средней активности** + вода = оксид металла + водород (только при нагревании) Zn
+ H2O
= ZnO
+ H2
4F2
+ 3H2O
= OF2
+ 6HF + O2 Cl2 + H2O = HClO + HCl
|
|
Со сложными веществами |
оксид активного металла + вода = щелочь СаО + H2O = Са(ОН)2 кислотный оксид + вода = кислота (кроме SiO2) SO3 + H2O = H2SO4
CuSO4
+
5H2O
= CuSO4
бледно-голубой ярко-синий
гидрид металла + вода = щелочь + водород КН + H2O = КОН + Н2
|
|
*активные металлы – стоящие в ряду напряжений металлов до Mg включительно; **средней активности металлы – стоящие в ряду напряжений металлов от Mg до Pb |
Вода – среда жизни
В ходе эволюции вода сыграла решающую роль. Именно водная среда (Мировой океан) явилась тем «питательным бульоном», в котором 3,5 млрд лет назад при специфических внешних условиях зародилась жизнь на Земле.
Мировой океан в настоящее время служит важнейшим источником пищевых ресурсов для человечества, поставляя 25% белков животного происхождения [2].
Вода обеспечивает существование жизни на нашей планете: сложнейшие биохимические реакции в клетках животных и растительных организмов могут протекать только при наличии воды. Живые существа на Земле содержат в среднем около 70-80% воды, т.е. на ¾ состоят из нее. С химической точки зрения живое вещество – это водный раствор, и почти все процессы, обеспечивающие его жизнедеятельность, сводятся к химическим реакциям в водном растворе.
По солевому составу кровь человека и морская вода очень близки. Кровь человека составляет десятую часть жидкости в его теле (в среднем 5 л крови, из них 3,5 л – жидкая составляющая, плазма) и обеспечивает возможность обмена веществ в организме. Одна из ее главных функций, подобно воде в природе, - транспортная (перенос кислорода, питательных веществ, шлаков). Для поддержания жизни человек должен получать около 2,5 л волы в сутки (непосредственно и с пищей). В среднем за свою жизнь человек потребляет и выделяет около 75 т воды, а все человечество – почти четвертую часть годового стока всех рек мира. Без воды человек не проживет и недели. Обезвоживание организма приводит к серьезным нарушениям функционирования различных органов. Человек тяжело переносит потерю 5% воды, а обезвоживание на 15-25% приводит к необратимым изменениям в организме и к смерти [2].
Как известно, кислород атмосферы, играющий исключительно важную роль в функционировании всех аэробных живых организмов, в том числе и человека, - биогенного происхождения. Более 150 млрд т кислорода поставляют ежегодно в атмосферу фитопланктон и наземные растения за счет фотосинтеза – важнейшего биохимического процесса на нашей планете.
Доказано, что источником кислорода при фотосинтезе служит вода [2]:
 18О
18О

 n
+
18O2
n
+
18O2
 (3)
(3)
Формула
 n
отражает
не реальное вещество, а состав углевода.
n
отражает
не реальное вещество, а состав углевода.
Установлено, что более точным итоговым уравнением фотосинтеза является уравнение вида:
 18О
18О

 n
+
n
+ 18О
+
18O2
18О
+
18O2
 ,
(4)
,
(4)
из которого следует, что в процессе фотосинтеза вода не только используется, но и образуется [2].
Одновременно с образованием первичных гидросферы и атмосферы на Земле зародился геологический круговорот воды (рисунок 7).
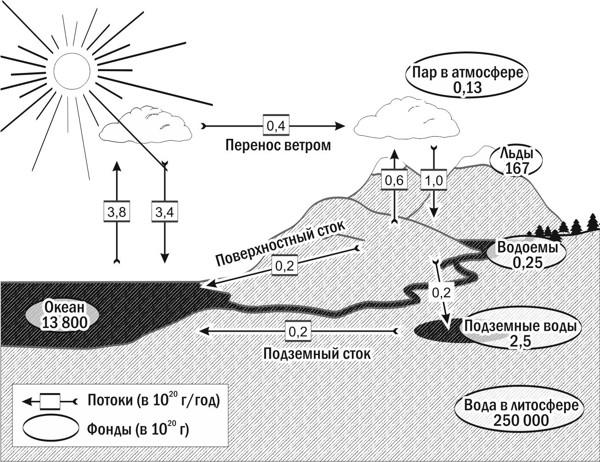
Рисунок 7 – Круговорот воды
Этот планетарный круговорот воды продолжается до сих пор, в нем участвует и живая природа, теперь он имеет геобиохимический характер. По словам В.И.Вернадского, «любое проявление природной воды – глетчерный лед, безмерный океан, почвенный раствор, гейзер, минеральный источник – составляет единое целое, прямо или косвенно, но глубоко связанное между собой» [2].
Круговорот воды в природе – это непрерывный процесс движения и обмена водой между различными составляющими гидросферы. Примерно за 3000 лет вся современная масса гидросферы испаряется, т.е. интенсивность возобновления воды достаточно велика. Обладая в миллион раз меньшей массой воды, чем масса гидросферы, живые организмы, главным образом растения, пропускают ее через себя (примерно за 1 млн лет). Таким образом, природная вода – это важный продукт жизнедеятельности живых организмов. В круговороте воды на суше доминирующая роль принадлежит растениям, 2/3 осадков определяются транспирацией.
«Вся масса воды, - писал В.И.Вернадский, - и в жидкой, и в газообразной, и в твердой форме находится в непрерывном движении, переполнена действенной энергией, сама вечно меняется и меняет все окружающее… Картина видимой природы определяется водой…» [2].
Велика роль воды в истории человеческой цивилизации. Вся практическая (хозяйственная) деятельность человека с самой глубокой древности связана с использованием воды. Вода – ценнейший природный ресурс, и нет ни одной отрасли мирового хозяйства, где бы она не использовалась.
Вода – важнейший техногенный источник получения энергии. Значительный энергетический потенциал заключен в океанических водах – приливах, температурной разности вод, морских течениях. В настоящее время пятую часть вырабатываемой в мире электроэнергии дают гидроэлектростанции. На тепловых и атомных электростанциях (ТЭС и АЭС) именно вода, превращенная в пар, вращает турбины, связанные с электрогенераторами [2].

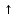


 5H2O
5H2O