
- •Білки харчової сировини
- •Вміст білкових фракцій у зернових культурах
- •Амінокислотний склад білків борошна (у % від кількості білка)
- •Амінокислотний склад і кількість сумарного білку у продуктах із бобів сої
- •Склад незамінних амінокислот насіння олійних культур (мг/1г білка)
- •2. Біохімічні основи визрівання м’яса
- •Біохімічні зміни компонентів м’яса під дією мікроорганізмів
- •Зміни пігментів
- •Зміни пігментів м’яса при обробці і зберіганні
ЛЕКЦІЯ №2
Білки харчової сировини
ПЛАН
Класифікація білків.
Білки злаків.
Білки бобових і олійних культур.
Білки плодів і овочів.
Білки м’яса.
Білки молока.
1. Білки – високомолекулярні органічні сполуки, нітрогенвмісні біополімери, побудовані з великої кількості залишків амінокислот, сполучених пептидним та іншими видами зв'язків. Свою назву білки дістали від яєчного білка, що з давніх-давен використовувався як харчовий продукт.
Класифікацію білків за їхньою розчинністю у різних речовинах запропонував Т.Осборн ще у 1907 році. При послідовній обробці досліджуваного продукту фракції білків послідовно екстрагують водою (такі білки називають альбумінами), 5-10% розчином NаСІ (глобуліни), 60-80% спиртом (проламіни) і 0,1-0,2% розчином NаОН (глютеліни). Склеропротеїни – нерозчинні білки, які містяться в оболонках і виконують в основному структурну функцію у комплексі з полісахаридами. Фракції білків відрізняються між собою амінокислотним складом, за яким судять про біологічну цінність білка харчової сировини.
2. Білки злаків. У порівнянні з еталоном білка для харчування людини білки злаків бідні на лізин, окрім овесу, ізолейцин окрім рису і сорго. Пшениця містить недостатньо треоніну і метіоніну, кукурудза – триптофану, білки жита, ячменю теж бідні на метіонін. Більш збалансовані за амінокислотним складом білки овесу, жита і рису.
Найбільш вивчені білки, які кількісно переважають у зернових це: гліадін і глютенін пшениці; зеїн кукурудзи; орізин рису; секалін жита; кафірин сорго; авенін овесу.
Основна кількість білків у зернівці припадає на ендосперм (65-75%), менше – на алейроновий шар (до 15,5%) і зародок (до 22%). Білки зародку й алейронового шару виконують в основному каталітичну функцію при проростанні зерна, вони представлені в основному альбумінами і глобулінами. Ці білки входять також до складу мембран, рибосом, мітохондрій переважно у складі нуклеопротеїдів, ліпопротеїдів, фосфопротеїдів. До 80% запасних білків ендосперма складають проламіни і глютеліни (табл. ).
Таблиця
Вміст білкових фракцій у зернових культурах
|
Культура |
Азот фракцій (у %від білкового азоту) | ||||
|
Альбу міни |
Глобу ліни |
Проламіни |
Глютеліни |
Склеро протеїни | |
|
Пшениця м ‘яка |
5,2 |
12,6 |
35,6 |
28,2 |
8,7 |
|
Жито |
24,5 |
13,9 |
31,1 |
23,3 |
7,2 |
|
Ячмінь |
6,4 |
7,5 |
41,6 |
26,6 |
17,9 |
|
Кукурудза |
9,6 |
4,7 |
29,9 |
40,3 |
15,5 |
|
Овес |
7,8 |
32,6 |
14,3 |
33,5 |
11,8 |
|
Гречка |
21,7 |
42,6 |
1,1 |
12,3 |
23,3 |
|
Рис |
11,2 |
4,8 |
4,4 |
63,2 |
16,4 |
Білкові фракції зернових – це суміш компонентів, які схожі за фізико-хімічними властивостями, але відрізняються між собою за молекулярною масою, амінокислотним складом, швидкістю руху при електрофорезі, здатністю взаємодіяти між собою та з іншими речовинами. Наприклад, сорти фуражної мякої пшениці, на відміну від твердої, яка використовується в харчовій промисловості і кулінарії, містять 12-14 компонентів альбумінної водорозчинної фракції з молекулярною масою близько 11 і 20 кДа.
Найбільш вивчені, так звані, клейковинні білки пшениці – гліадін і глютенін, які мають велике значення для виробництва продукції з борошна. За допомогою іонообмінної хроматографії, гельхроматографії, електрофорезу та інших методів гліадінова фракція пшениці розділена на велику кількість компонентів, які умовно об’єднані за зменшенням їхньої електрофоретичної рухливості в кислому середовищі у 4 групи: α-, β-, γ- та ω-гліадіни. Кожна з цих фракцій складається з декількох компонентів, загальна кількість яких у пшениці складає від 40 до 50.
При визначених умовах електрофорезу (у ПААГ, у крохмальному гелі) електрофоретичний спектр розглядається як фенотипічна ознака виду і сорту пшениці.
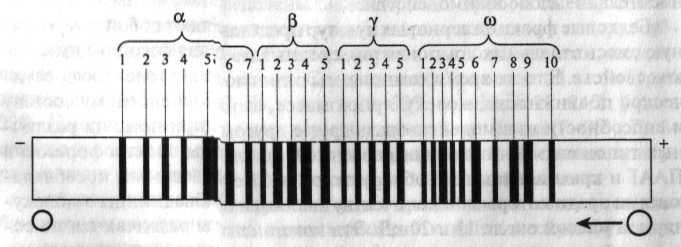 Рис.
Еталонний електрофоретичний спектр
гліадіну пшениці
Рис.
Еталонний електрофоретичний спектр
гліадіну пшениці
Еталонний спектр має 30 позицій, які розподіляються за фракціями так: α 01234567, β 1-5, γ 1-5, ω 1-12. Відповідно до цього еталону досліджується і записується гліадін різних сортів, що має велике значення для використання пшеничного борошна у виробництві різних продуктів харчування.
Б ільшість
гліадінових білків складаються з одного
поліпептидного ланцюга з молекулярною
масою 30-45 кДа і внутрішньомолекулярними
дисульфідними зв'зками. У меншій кількості
виявлені білки з молекулярною масою
22, 25, 48, 57, 64-80 кДа.
ільшість
гліадінових білків складаються з одного
поліпептидного ланцюга з молекулярною
масою 30-45 кДа і внутрішньомолекулярними
дисульфідними зв'зками. У меншій кількості
виявлені білки з молекулярною масою
22, 25, 48, 57, 64-80 кДа.
–S–S– –S–S– –S–S–
Глютенін пшениці – більш гетерогенна фракція і складається з багатьох компонентів з молекулярною масою 50-3000 кДа. Цей білок без розриву дисульфідних зв'зків не рухається в гелі при електрофорезі. Причиною є те, що окрім внутрішньомолекулярного S-S зв‘яку, на кожний поліпептидний ланцюг припадає 2-3 дисульфідних зв’язки з сусідніми ланцюгами.
–S–S– –S–S– –S–S–
– S – S – – S – S –
Складністю при вивченні будови глютеніну була здатність білків до утворення полімерних структур. Більшість учених дійшли думки, що глютенін в основному складається з білкових субодиниць з молекулярною масою від 100 до 300 кДа. Частка високомолекулярних білків і одно ланцюгових молекул складає близько 20%.
Здатність білків клейковини утворювати полімерні структури є дуже важливою для виробництва продукції з борошна. Питання формування клейковинного комплексу до кінця не вияснене. Запропоновано декілька наступних гіпотез, але жодна з них не дає вичерпної відповіді на питання взаємозв’язку будови і пружно-еластичних властивостей пшеничного тіста. Глютеліни зернових культур, які утворюють клейковину мають лінійну структуру на відміну від розгалуженої у культур, які її не утворюють (овес, кукурудза). Еластичність виникає внаслідок здатності розтягнутих, поліпептидних ланцюгів повертатись до попереднього спіралевидного стану, а також внаслідок постійного зміщення (ковзання) лінійних молекул одна відносно одної. Відсутність пружно-еластичних властивостей вівсяного, кукурудзяного тіста обумовлена розгалуженим, трьохмірним способом з’єднання поліпептидних ланцюгів. Найбільш виражений вплив на якість клейковини має наявність 50-60% високомолекулярних субодиниць глютеліну з молекулярною масою близько 100 кДа. Взаємодія фракцій глютеліну, який надає клейковині міцність і пружність і гліадіну, що обумовлює еластичність, і здатність розтягуватись, створює клейковинний білковий полімер з властивими йому особливостями.
Властивості клейковинного комплексу залежать не лише від будови і взаємодії білкових фракцій. У структурі трьохвимірної сітки комплексу гліадіну і глютеліну окрім ковалентних дисульфідних зв'язків значну роль відіграють нековалентні: водневі, електростатичні, гідрофобні взаємодії. Висока реакційна здатність молекул білка сприяє взаємодії їх з ліпідами і вуглеводами, утворенню відповідно ліпопротеїнових і глікопротеїнових комплексів, які теж впливають на структуру і властивості клейковини. Загальновизнана гіпотеза: ліпопротеїн забезпечує листкову структуру тіста і процес «ковзання» між білковими пластинами.
Білки, які виконують функції ферментів, теж впливають на якість клейковини і виробів з тіста. Протеази, розщеплюючи білки, послаблюють клейковину. Ліпоксигеназа сприяє взаємодії продуктів окиснення жирних кислот з –SН групами білків і цим зміцнює клейковину. Помірна активність амілаз необхідна для бродіння і газоутворення.
За поживною цінністю серед злаків цінною є культура тритікале - гібрид пшениці (Triticum) і жита (Secale)), яка містить 11-22% білка і краще співвідношення амінокислот: більше лізину, метіоніну, ніж пшениця (табл. ).
Таблиця
