
- •3.Основные сведения о строении атомов. Квантово-механическая модель атома. Волновые свойства электронов.
- •4.Квантовые числа электронов. Распределение электронов по орбиталям. Принцип Паули. Порядок заполнения атомных орбиталей электронами.
- •5. Электронные и электронно-графические формулы. Привести конкретные примеры указанных формул для элементов 3, 5 ,7 периодов.
- •6. Периодический закон и периодическая система д.И. Менделеева Структура периодической системы (период, группа, подгруппа). Значение периодического закона и периодической системы.
- •7. Периодическое изменение свойств химических элементов. Атомные и ионные радиусы. Энергия ионизации. Сродство к электрону. Электроотрицательность.
- •8. Химическая связь. Основные типы и характеристики химической связи. Условия и механизм ее образования. Метод валентных связей. Валентность. Понятие о методе молекулярных орбиталей.
- •9. Водородная связь. Особые свойства воды и некоторых других соединений, способных образовывать водородную связь.
- •10.Донорно-акдепторная связь. Комплексные соединения. Комплексообразователь и лиганды. Заряд комплексообразователя и координационной сферы. Координационное число константы нестойкости.
- •12.Химическая термодинамика. Энергетика химических процессов. Внутренняя энергия и энтальпия. Термохимические уравнения. Теплота образования и разложения веществ.
- •13.Стандартные тепловые эффекты различных процессов. Основной закон термохимии (закон Гесса). Применение термохимических расчетов,
- •14.Химическое сродство. Энтропия. Ее изменение при химических процессах. Стандартные энтропии веществ. Методы расчета" изменения энтропии в ходе химической реакции.
- •16.Химическая кинетика. Факторы влияющие на скорость реакции, методы ее регулирования. Закон действующих масс. Константа скорости реакции. Кинетические уравнения реакций.
- •17.Энергия активации. Активированный комплекс. Энергетические схемы хода реакции. Температурная зависимость скорости реакций. Правило Вант-Гоффа,
- •18.Катализ и катализаторы. Гомогенный и гетерогенный катализ.
- •19.Химическое равновесие. Константа равновесия. Принцип Ле-Шателье Влияние на равновесие изменения температуры, давления» концентрации. Практическое применение принципа Ле-Шателье.
- •20. Дисперсные системы, их классификация, устойчивость и коагуляция. Колойдные и истинные растворы. Способы выражения состава растворов.
- •21.Растворимость газов, жидкостей и твердых веществ в жидкостях. Закон Генри. Закон распределения. Давление насыщенного пара растворителя над раствором. Первый закон Рауля.
- •22.Температура кристаллизации и температура кипения растворов неэлектролитов. Второй закон Рауля. Осмотическое давление. Закон Вант-Гоффа.
- •23.Электролиты. Электролитическая диссоциация. Степень и константа диссоциации, связь между ними. Активность и сила раствора
- •24 Свойство растворов электролитов. Изотонический коэффициент, его определение. Связь изотонического коэффициента со степенью диссоциации. Применение электрохимических процессов.
- •25.Вода Природные воды, их обработка Замкнутый водооборот. Водород, водородная энергетика.
- •26.Произведение растворимости. Электролитическая диссоциация воды. Ионное произведение воды. Водородный показатель. Методы определения концентрации ионов водорода
- •28.Электродные потенциалы. Механизм их возникновения. Двойной электрический слой. Уравнение Нернста. Ряд напряжений.
- •29.Гальванические элементы. Теория гальванических элементов.
- •30.Электролиз расплавов растворов. Правила электролиза с инертным анодом. Электролиз раствора с растворимым анодом.
- •31.Основные законы электролиза. Применение электролиза. Гальваностегия и гальванопластика. Электрохимическая обработка металлов. Аккумуляторы.
- •33.Методы защиты металлов от коррозии. Металлические защитные покрытия (анодные, катодные). Неметаллические покрытия. Электрохимические методы защиты от коррозии.
- •34.Общие свойства металлов. Металлическая связь. Тепло- и электропроводность. Физико-механические и химические свойства металлов.
- •35. Высокомолекулярные соединения (вмс). Полимеры. Классификация. Методы получения. Полимеризация. Поликонденсация.
- •36. Форма, гибкость и структура макромолекул полимеров. Конформация и конфигурация. Атактические и стереорегулярные полимеры. Сополимеры и блоксополимеры. Надмолекулярная структура полимеров.
- •37. Агрегатные, физические и фазовые состояния полимеров. Физикомеханические и химические свойства полимеров.
- •38. Неорганическая химия р-элементов IV группы. Важнейшие соединения углерода и кремния, использование их в строительстве. Карбонаты, силикаты, стекла, ситаллы, керамика. Их св-ва и применение.
- •40.Цементы. Портландцемент, его химический и минералогический состав. Получение портландцемента.
- •41Химизм процессов, протекающих при получении цемента и его взаимодействии с водой. Основные составляющие цементного камня. Влияние добавок на процессы твердения
- •42. Коррозия бетона и методы борьбы с ней. Основные виды коррозии бетона. Химизм процессов, протекающих при коррозии. Основные методы защиты бетона от коррозии.
38. Неорганическая химия р-элементов IV группы. Важнейшие соединения углерода и кремния, использование их в строительстве. Карбонаты, силикаты, стекла, ситаллы, керамика. Их св-ва и применение.
Покрытия неметаллические неорганические:
Эмалевые покрытия: (из стекла) – защищают хорошо от коррозии. Недостаток: неустойчивость к механическому и термическому удару (резкое изменение температуры).
Цементные покрытия: толщина выше 5 мм, при большей толщине армируют – надёжно защищают металл; обладают способностью самозалечивать дефекты, в некотором смысле имеет ингибиторные способности: легко наносить, ремонтировать, удобно для защиты от почвенной коррозии.
Оксидные покрытия –обработка металлов ненадёжна, много дефектов.
Важнейшие соединения С и Si, используемые как строительные материалы.
Карбонаты-
комплексы С, простейшими из которых
являются 3-оксокорбанат. Оксокарбонаты
получают взаимодействием СО с растворами щёлочей. При нагревании
карбонаты разлогаются, образуя оксиды
СО
с растворами щёлочей. При нагревании
карбонаты разлогаются, образуя оксиды
СО .
Наибольшее применение в строительстве
находят карбонатыCa
( мел, мрамор, известняк, ракушечник).
.
Наибольшее применение в строительстве
находят карбонатыCa
( мел, мрамор, известняк, ракушечник).
Силикаты –обширный
класс неорг соед, в основе структуры
которых лежат тетраэдрические группы.
Эти группы могут быть связаны между
собой или изолированы другими структурными
элементами. Образуются при сплавлении
SiO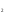 с
оксидами металлов. Большинство
нерастворимы в металлах, за исключением
щелочных металлов. При добаклении к-ты
к р-ру Na
с
оксидами металлов. Большинство
нерастворимы в металлах, за исключением
щелочных металлов. При добаклении к-ты
к р-ру Na SiO
SiO студенистый осадок. если такой осадок
отмыть от минеральной к-ты и высушить,
то получится пористый материал –
силикогель.
В природе почти все породообразующие
материалы являются силикаты. Так же их
применяют как технические продукты
(керамика, огнеупоры, стекло, цемент).
студенистый осадок. если такой осадок
отмыть от минеральной к-ты и высушить,
то получится пористый материал –
силикогель.
В природе почти все породообразующие
материалы являются силикаты. Так же их
применяют как технические продукты
(керамика, огнеупоры, стекло, цемент).
Стекло – аморфное вещ-во, получаемое при затвердивании сплава оксидов. Структура очень сложна, имеет полимерно-кристаллидную структуру. По составу стёкла делят на силикатные, алюмосиликатные, боросиликатные. Ионы щелочных и щелочноземельных металлов могут размещаться в промежутках тетроэдрической сетки. Эти атомы наз Модификаторами. В ведение их уменьшает прочность стекла. По содержанию модификаторов делят: щелочные, безщелочные, кварцевые. По назначению: технические, строительные, бытовые.
Св-ва стёкл:
Плавится в интервале температур: ниже темпера приобретает хрупкость; Выше температура-тягучесть.
Мех свойство стёкл: характерно высокое сопотивление сжатию и низкий предел прочности при растяжении. Твердость довольно высока по 10-альной шкале 5-7 единиц. Важное свойство стёкл – прозрачность ( 90% видимого света).
Ситаллы – стекло-кристаллические
материалы – получают контролируемой
кристаллизацыей. Св-ва: плотность 2,3…3
г/см .
Прочность на изгиб, на растяжение. Можно
вырабатывать методом резанья, сверлить,
пилить и др.
.
Прочность на изгиб, на растяжение. Можно
вырабатывать методом резанья, сверлить,
пилить и др.
Применение: как у стёкл, для изготовления деталей машин.
Керамика, фарфор- неорганический материал, получаемый спеканием порошков минеральных веществ. Спекание – 1200-2500С. Исходные вещ-ва для керамики: глина, полевой шпак, тальк, каулин, оксиды ряда металло. Строительная керамика: обжиг, перимущественно глиняных масс с предварительным формированием и сушкой. После обжига стойкость, прочность.
39.Вяжущие вещ-ва. Определения и классификация вяжущих. Известковые и магнезиальные вяжущие. Гипсовые вяжущие.
Вяжущие вещ-ва – вещества, способные при определённых условиях переходить из пластического в твёрдое состояние, прочно скрепляя контактирующие с ними элементы в единое изделие. Минеральные: порошкообразные продукты, которые при смеивании с водой образуют пластичную массу, затвердевающую в прочное тело; Органические: битумные., клея. Подразделяют на воздушные и гидравлические. Воздушные – вещ-ва, которые после смешивания с водой затвердевают и длительно сохраняются на воздухе, на прочность неустойчивы в воде (известь, гипс, магнезиальные вяжущие). Гидравлические – после смешивания с водой и предварительного затвердевания на воздухе могут продолжать твердеть в воде, сохраняя при этом прочность (цемент, гидравлическая известь).
Минеральные – изготавливаются из распространённых горных пород ( гипсовых, известковых, кремниезёместых)Используются так же отходы промышленности (шлаки, зола, кремнеземные отходы).
Магнезиальные – смесь 30%-ого раствора MgCl с MgO. Гипсовые вяжущие –природный гипс ( водная соль сульфата кальция) при высушивании природного гипса образуется полуводный гипс.
