
posobia2 / Лекции по биоорганической химии (2011 г
.).pdf
ЛЕКЦИЯ № 5
Конкурентные реакции нуклеофильного замещения и элиминирования у насыщенного атома углерода
В реакциях нуклеофильного замещения в качестве субстратов выступают спирты, тиолы, амины, галогенпроизводные, т.е. соединения, в молекулах которых содержатся sp3-гибридизированные атомы углерода, связанные ковалентной полярной связью с более электроотрицательным атомом функциональной группы. В качестве нуклеофильных частиц в этих реакциях выступают анионы и нейтральные молекулы, имеющие атом с одной или несколькими парами электронов.
|
|
R1 |
|
R1 |
Nu |
|
|
R2 C Nu + Z |
|
+ |
R2 C |
Z |
||
|
|
|
|
|
|
|
R3 |
|
R3 |
Существование большого количества потенциальных нуклеофилов (Nu) и уходящих групп (Z) позволяет широко использовать SN2 -реакции в органическом синтезе:
Нуклеофил + |
|
Субстрат → |
Продукт |
+ |
Уходящая группа |
|||||||||
|
|
|
|
I¯ |
+ |
CH3Cl |
|
|
CH3I |
|
+ Cl¯ |
|||
|
|
CH3O¯ |
+ |
CH3Cl |
|
CH3OCH3 |
+ |
Cl¯ |
||||||
|
|
HS¯ |
+ |
CH3Br |
|
CH3SH |
|
+ |
Br¯ |
|||||
|
|
(CH3)2N + |
CH3I |
|
(CH3)3N |
|
+ |
I¯ |
||||||
|
|
HC≡C¯ |
+ |
CH3 –CH2 – I |
HC≡C–CH2–CH3 |
+ |
I¯ |
|||||||
|
|
OH¯ |
+ |
CH3Br |
|
CH3 – OH |
+ |
Br¯ |
||||||
|
|
O |
|
CH3–CH2–I |
|
|
O |
|
+ I¯ |
|||||
H3C C |
+ |
H3C C |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
C2H5 |
|
|
||
|
|
|
|
|
|
|
|
|
||||||
61
Реакционная способность субстрата зависит:
От полярности связи С + Z - (статический фактор). Чем выше электроотрицательность заместителя Z, тем больше полярность связи, тем больший положительный заряд возникает на атоме углерода, тем он больше предрасположен к нуклеофильной атаке.
От способности заместителя Z к отщеплению и образованию устойчивой частицы (динамический фактор). Чем длиннее связь
С + Z -, тем она менее прочная и тем легче она подвергается разрыву. Длина связи С + Z - увеличивается с ростом атомного радиуса заместителя; одновременно с увеличением радиуса заместителя увеличивается также стабильность уходящей группы. Хорошо уходящими группами являются галогенид–ионы: F < Cl < Br < I . С увеличением ионных радиусов возрастает стабильность анионов, так как отрицательный заряд делокализуется в большем объеме. Плохо уходящими группами являются анионы, являющиеся сильными основаниями: Н ; ОН ; СН3О ; NH2 ; СН3 и др.
Реакционная способность нуклеофильных частиц тем выше, чем легче они предоставляют пару электронов для образования связи с электронодефицитным атомом углерода. У галогенид-ионов реакционная способность в ряду F < Cl < Br < I увеличивается, что объясняется уменьшением электроотрицательности и ростом радиуса. С ростом радиуса увеличивается поляризуемость ионов, при этом пара электронов слабее удерживается ядром и легче предоставляется для образования связи с электрофильной частицей. Аналогичным образом объясняется разная реакционная способность гидроксид-ионов и гидросульфид-ионов и их аналогов: HS > HO ; CH3S > CH3O .
62

Нуклеофильное замещение может идти по одному из двух механизмов – SN2 или SN1. По механизму бимолекулярного нуклеофильного замещения SN2 реагируют субстраты, содержащие уходящую группу, связанную с первичным атомом углерода.
В качестве субстратов в реакциях, идущих по механизму SN2, могут выступать алкилгалогениды, спирты, тиолы, амины, содержащие первичные углеводородные радикалы.
Общая схема бимолекулярного нуклеофильного замещения SN2 :
|
R1 |
|
|
R1 |
|
R1 |
|
|
Nu + |
C |
|
|
|
|
|
||
- |
|
|
|
|
|
|||
|
R2 |
Z |
Nu |
C |
Z |
C |
+ |
Z |
|
R3 |
|
|
|
Nu |
R2 |
|
|
|
|
R3 |
R2 |
|
R3 |
|
||
|
|
|
|
|
|
переходное состояние
Реакции бимолекулярного нуклеофильного замещения представляют собой согласованный процесс, так как образование связи с нуклеофилом и разрыв связи с уходящей группой происходит одновременно, атакующая нуклеофильная частица постепенно вытесняет уходящую группу. При этом часть энергии, необходимая для разрыва связи С-Z, возмещается за счет энергии, выделяющейся при образовании связи С-Nu. Эти реакции являются бимолекулярным процессом, так как в образовании переходного состояния (самая медленная стадия) участвуют обе частицы и скорость реакции зависит от концентрации как нуклеофила, так и субстрата.
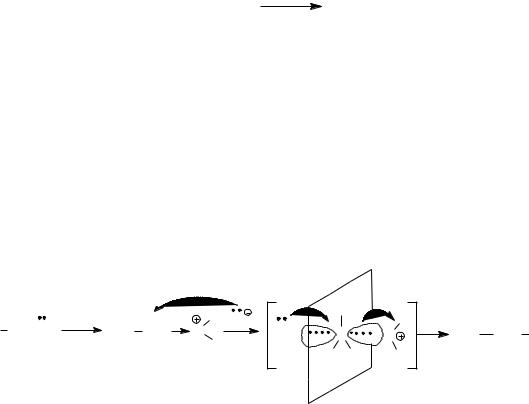
В переходном состоянии изменяется тетраэдрическое расположение связей атома углерода, подвергающегося нуклеофильной атаке: три заместителя R1, R2, R3 располагаются в одной плоскости,
63

перпендикулярной плоскости рисунка, а уходящая группа и нуклеофильная частица расположены на одной линии, перпендикулярной этой плоскости. Наличие объемных заместителей R1, R2, R3, связанных с атакуемым атомом углерода, затрудняет нуклеофильную атаку, так как атаке подвергается тыльная сторона связи С-Z.
Увеличение полярности растворителя также снижает скорость реакции. Это объясняется тем, что полярный растворитель стабилизирует нуклеофильную частицу, имеющую отрицательный заряд, лучше, нежели переходное состояние, в котором отрицательный заряд распределен между нуклеофилом и уходящей группой. Это приводит к тому, что реакционная способность нуклеофила уменьшается и увеличивается разность энергий исходного вещества и переходного состояния, что ведет к увеличению энергии активации реакции.
Рассмотрим в качестве примеров реакции гидролиза галогеналканов и реакции превращения спиртов в галогеналканы.
CH3 |
|
CH2 |
|
Br + KOH |
H2O |
CH3 |
|
CH2OH + KBr |
|
|
|
|
Гидролиз галогеналканов осуществляется действием водных растворов щелочей. В качестве нуклеофильной частицы в этой реакции выступает гидроксид-ион, образующийся при диссоциации щелочи.
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
- |
|
|
|
|||
HO |
+ |
CH3 CH2 |
Br |
HO |
C |
Br |
CH3 CH2 OH + Br |
||
|
|||||||||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
H |
H |
|
|
64
Однако превращение спиртов в галогенпроизводные не удается осуществить действием на спирты солями галогеноводородных кислот:
C2H5OH + KBr  C2H5Br + KOH
C2H5Br + KOH
Это объясняется наличием в субстрате (спирте) плохо уходящей группы ОН . Протекание реакции возможно при переводе плохо уходящей группы (ОН ) в хорошо уходящую группу (Н2О), что достигается действием на спирты соответствующих кислот:
CH |
|
CH OH + HBr |
CH |
|
CH |
|
Br + H O |
|
|
|
|||||
3 |
2 |
3 |
2 |
2 |
|||
Ион водорода протонирует атом кислорода гидроксильной группы (быстрая стадия), что приводит к возникновению на атоме кислорода полного положительного заряда. Вследствие этого связь С ОН становится более полярной, а на атоме углерода увеличивается частичный положительный заряд, что делает его более восприимчивым к нуклеофильной атаке.
+ |
H |
+ |
|
H |
Br |
Br- |
CH3 |
|
H |
CH3 CH2OH |
|
|
|
|
|||||
|
|
CH3 CH2 O |
H |
|
C |
O |
CH3 CH2 Br + H2O |
||
|
|
|
|
|
H |
H |
|
H |
|
|
|
|
|
|
|
|
В качестве субстратов в реакциях, идущих по механизму мономолекулярного нуклеофильного замещения SN1, могут выступать алкилгалогениды, спирты, тиолы, амины, содержащие третичные углеводородные радикалы.
65

Общая схема мономолекулярного нуклеофильного замещения
SN1:
R1 |
|
|
R2 |
|
|
|
R1 |
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
C |
|
C R1 |
+ |
Nu |
|
C |
|
|
C |
|
|
Z |
|
R2 |
|
|
R2 |
||||||
R2 |
-Z |
|
|
Nu |
+ |
||||||
R3 |
|
R3 |
|
|
R3 |
|
|
Nu |
R3 |
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Реакции SN1 не являются согласованным процессом и состоят из двух отдельных стадий. На первой стадии происходит ионизация (медленная стадия) исходного соединения с образованием катиона и аниона. На второй стадии (быстрая стадия) образовавшийся катион реагирует с нуклеофильной частицей, давая конечный продукт. Скорость реакции в целом зависит от скорости образования катиона. Геометрия карбкатиона, отвечающая минимуму энергии, характеризуется плоским расположением связей относительно положительно заряженного sp2- гибридизированного атома углерода. Скорость взаимодействия катиона с нуклеофилом не зависит от того, с какой стороны плоскости происходит атака. В результате реакции образуется эквимолярная смесь стереоизомеров (энантиомеров). Протеканию реакций по этому механизму способствует наличие объемных заместителей у электронодефицитного атома углерода, которые затрудняют нуклеофильную атаку с тыла. Проведение реакций в полярных растворителях также способствует протеканию реакции по механизму SN1, так как под действием полярных молекул растворителя легче происходит гетеролитический разрыв связи С-Z (ионизация), а также лучше стабилизируется уходящая группа Z . Субстраты, у которых уходящая группа связана с вторичным атомом углерода, реагируют либо по механизму SN1, либо по механизму SN2.
66

В качестве примера рассмотрим реакцию превращения третбутанола в трет-бутилбромид. Как и в случае с первичными спиртами, необходимо реакцию проводить в кислой среде для превращения плохо уходящей группы – гидроксид-иона (НО ) в хорошо уходящую группу – молекулу Н2О.
|
|
|
CH3 |
HBr |
|
|
|
CH3 |
||||
H3C |
|
C |
|
OH + |
H C |
|
C |
|
Br + H O |
|||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
3 |
|
2 |
|||
|
|
CH3 |
|
|
|
CH3 |
||||||
Реакция |
|
|
протекает |
в |
три последовательные стадии: |
|||||||
1) протонирование спирта – быстрая стадия; 2) гетеролитический разрыв связи С-О, приводящий к отщеплению воды и образованию карбкатиона
–медленная стадия реакции, определяющая скорость реакции в целом; 3) нуклеофильная атака бромид-ионом образовавшегося на предыдущей стадии карбкатиона, в результате которой образуется конечный продукт
–быстрая стадия.
Механизм реакции:
CH3 |
CH |
3 |
H |
CH3 |
- |
CH3 |
|
|
Br |
|
|||
|
|
|
|
|
|
|
H3C C OH + H+ |
H C C O |
|
H3C C |
|
H3C C Br |
|
|
3 |
|
|
|
|
|
CH3 |
CH |
3 |
H - H2O |
CH3 |
|
CH3 |
|
|
|
|
|
|
|
На механизм нуклеофильного замещения большое влияние оказывают заместители при электронодефицитном атоме углерода. При изучении реакций гидролиза в ряду галогеналканов
СН3Cl |
C6H5CH2Cl |
(C6H5)2CHCl (C6H5)3CCl |
|
|
наблюдалось протекание реакции |
по SN1 |
механизму, начиная |
с |
|
бензилхлорида |
– C6H5CH2Cl, а ионизация |
трифенилхлорметана |
– |
|
67

(C6H5)3CCl - выражена настолько сильно, что растворы этого соединения в жидком SO2 обладают электропроводностью. Причиной столь сильного облегчения ионизации, и связанного с этим быстрого перехода к механизму SN1 является значительная стабилизация карбкатиона, обусловленная делокализацией положительного заряда:
CH2 |
CH2 |
CH |
CH |
|
|
2 |
2 |
При переходе от бензилхлорида к дифенилхлорметану и трифенилхлорметану эффект стабилизации карбкатиона становится все более отчетливо выраженным и атака по механизму SN1 облегчается еще сильнее, так как возможность делокализации положительного заряда возрастает. Аналогичная стабилизация наблюдается также для аллильных карбкатионов:
CH2 CH CH2Cl |
CH |
CH CH |
CH |
CH CH |
+ |
- |
|
2 |
2 |
2 |
2 |
|
Cl |
Схема реакции гидролиза бензилхлорида имеет вид:
CH2Cl |
CH2OH |
|||
+ H2O |
|
|
|
+ HCl |
|
||||
|
|
|
|
|
Реакция протекает в три последовательные стадии:
1)гетеролитический разрыв связи С-Сl, протекающий под действием полярных молекул растворителя – медленная стадия реакции;
2)нуклеофильная атака молекулой воды образующегося карбкатиона с образованием оксониевого катиона – быстрая стадия;
68

3) отщепление протона от оксониевого катиона с образованием спирта – быстрая стадия.
Механизм реакции:
CH2Cl |
|
|
|
|
|
H |
CH2 |
H2O |
CH |
2 |
O |
CH2OH |
|
|
|
|
|
H |
||
- Cl- |
|
|
|
|
|
|
|
|
|
|
|
- H+ |
Аллилгалогениды, подобно бензилгалогенидам, обладают значительно большей реакционной способностью по сравнению с соединениями, для которых невозможна стабилизация карбкатионов за счет делокализации положительного заряда. Однако особенностью аллилгалогенидов и бензилгалогенидов является то, что группа СН2 в этих соединениях значительно легче атакуется также по механизму SN2, чем группа СН2 в хлорэтане (замещение идет в 100 раз быстрее). Такой эффект объясняется тем, что sp2-гибридизированный атом углерода в переходном SN2 состоянии использует свою негибридную р- орбиталь для взаимодействия не только с атакующей нуклеофильной частицей и отщепляющейся уходящей группой, но также с -орбиталью двойной связи, что приводит к стабилизации переходного состояния.
|
|
H |
|
H |
|
C |
|
CH2 CH CH2Br + I- |
C |
H |
CH2 CH CH2I + Br- |
I |
C |
Br |
|
H |
|
H |
|
|
|
|
Рассмотрев оба механизма нуклеофильного замещения, можно сделать некоторые обобщения о влиянии различных факторов на механизм реакции:
69
Реакция протекает по SN1 механизму в случае тех соединений, которые способны образовывать достаточно стабильные катионы. Триалкилметильные и мезомерно стабилизированные катионы обеспечивают преимущественное протекание реакции мономолекулярного замещения. Увеличение числа алкильных заместителей облегчает мономолекулярное и затрудняет бимолекулярное замещение.
Растворители с высокой диэлектрической проницаемостью (Н2О, НСООН, водноорганические смеси) стабилизируют ионы и поэтому способствуют мономолекулярному замещению, растворители с низкой диэлектрической проницаемостью (диметилформамид), не вызывающие стабилизации ионов, способствуют бимолекулярному замещению.
Реакции элиминирования у насыщенного атома углерода
Реакциям нуклеофильного замещения очень часто сопутствуют конкурирующие с ними реакции отщепления (элиминирования). Реакциям SN1 сопутствуют реакции мономолекулярного элиминирования Е1, реакциям SN2 сопутствуют реакции бимолекулярного элиминирования Е2. Это обусловлено основностью нуклеофильных частиц. Одна и та же частица может проявлять одновременно свойства основания (предоставлять пару электронов для образования связи с протоном) и свойства нуклеофила (предоставлять пару электронов для образования связи с электрофилом – атомом углерода, или другим атомом, имеющим частичный положительный заряд).
70
