
posobia2 / Лекции по биоорганической химии (2011 г
.).pdf
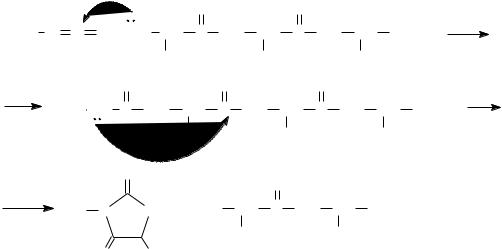
Некоторые аминокислоты (цистин, треонин, изолейцин и гидроксипролин) имеют два хиральных центра и могут существовать в виде четырех стереоизомеров. Однако для цистина число возможных стереоизомеров меньше из-за наличия плоскости симметрии у мезоформы, которая оптически неактивна.
|
|
|
|
COOH |
|
|
|
|
|
|
COOH |
|
|
|
|
COOH |
|
|
|
COOH |
||||||||||||||||||||
H2N |
|
|
|
|
H |
|
|
H |
|
|
|
|
|
|
|
NH2 |
|
H |
|
|
|
NH2 |
H2N |
|
|
|
|
H |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
CH2 |
|
|
|
|
|
|
CH2 |
|||||||||||||
|
|
|
|
S |
|
|
|
|
|
|
S |
|
|
|
|
S |
|
|
|
|
|
S |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
|
|
|
|
S |
|
|
|
|
S |
|
|
|
S |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|||||||||||||||
H |
|
|
|
|
|
NH2 |
|
H2N |
|
|
|
|
|
|
|
H |
|
H |
|
|
|
NH2 |
H2N |
|
|
|
|
H |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
COOH |
|
|
|
|
|
|
COOH |
|
|
|
|
COOH |
|
|
|
COOH |
||||||||||||||||||||
|
L-цистин |
|
|
|
|
|
|
D-цистин |
|
|
|
|
мезоформа цистина |
|
|
|
|
|||||||||||||||||||||||
-Аминокислоты в свободном виде представляют собой твердые кристаллические вещества, хорошо растворимые в воде, плохо растворимые в спирте, не растворимые в эфире и других неполярных органических растворителях. -Аминокислоты характеризуются высокими температурами плавления, что обусловлено их существованием в виде цвиттер-ионов (биполярных ионов):
+ |
_ |
||||
H3N |
|
|
CH |
|
COO |
|
|
||||
|
|
|
|
||
|
|
R |
|||
Наличие как основной (NH2), так и кислотной (СООН) групп в молекуле означает, что в водном растворе реальное строение частиц зависит от значения рН. При низких значениях рН карбоксильная группа находится в недиссоциированном состоянии, аминогруппа – в протонированной форме.
171

H2N CH COO |
+ OH- |
|
+ H+ |
|
|
H3N CH COO |
H N CH COOH |
||
|
_ H2O |
|
3 |
|
R |
R |
R |
||
|
При высоких значениях рН аминокислоты в водных растворах находятся в виде аминокарбоксилат-анионов. При промежуточных значениях рН основная частица, находящаяся в растворе в существенных количествах, – это цвиттер-ион, молекулярная форма RCH(NH2)CООН не присутствует в сколько-нибудь значительной степени. На существовании в сильно кислой среде аминокислот в катионной форме и в щелочной среде – в анионной форме основано разделение аминокислот методом электрофореза: катионы под действием электрического тока перемещаются к катоду (отрицательно заряженному электроду), анионы – к аноду (положительно заряженному электроду). рН раствора аминокислоты, при котором средний заряд молекулы равен нулю, называется изоэлектрической точкой (рI). Состояние аминокислоты, в котором ее заряд равен нулю, называется изоэлектрическим состоянием (т.е. в растворе концентрация биполярных ионов аминокислоты максимальна, а концентрации катионных и анионных форм аминокислоты минимальны и равны между собой). Для моноаминомонокарбоновых кислот значения рН, при котором они находятся в изоэлектрическом состоянии, лежат в пределах 5.5-6.3, что близко к нейтральной среде, поэтому такие аминокислоты называют нейтральными. Для моноаминодикарбоновых кислот значения рН, при котором они находятся в изоэлектрическом состоянии, лежат в сильно кислой среде (рI 3.1), поэтому такие аминокислоты называют кислыми. У диаминомонокарбоновых кислот значения рН в изоэлектрическом
172

состоянии лежат в сильно щелочной среде (рI 9.8), такие аминокислоты называют основными.
В реакциях аминокислоты проявляют себя как гетерофункциональные соединения, т.е. реагируют в зависимости от реакционного партнера либо одной функциональной группой, либо обе функциональные группы вступают в реакцию с реагентом.
Качественной реакцией на -аминокислоты является их взаимодействие со свежеполученным гидроксидом меди (II), в результате которого образуется внутрикомплексное соединение синефиолетового цвета:
|
O |
|
|
R |
|
NH2 |
O |
O |
2 H N CH C + |
Cu(OH) |
|
|
|
|
|
C |
|
_ |
|
|
|
Cu |
|
|||
2 |
OH |
2 |
2H2O |
|
|
|
||
R |
|
|
C |
|
|
|
||
|
|
|
|
|
|
|||
|
|
|
O |
O |
NH2 |
R |
||
|
|
|
|
|
||||
Реакции по аминогруппе:
Под действием ацилирующих агентов аминокислоты легко подвергаются ацилированию с образованием амидов:
|
|
|
|
|
|
|
O |
|
|
O |
O |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
N |
|
CH |
|
C |
+ (CH CO) O |
|
|
|
|
|
|
|
|
|
|
|
|
+ |
CH COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
CH3 C NH |
CH C |
||||||||||||||||||
2 |
|
|
|
|
|
|
3 2 |
|
3 |
||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
R |
|
|
|
|
|
|
|
|
R |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Превращение аминогруппы в амидную используется для защиты аминогруппы при синтезе пептидов и белков.
Как амины, аминокислоты подвергаются алкилированию под действием галогеналканов:
|
|
|
|
|
|
O |
AgOH |
|
|
|
|
|
|
|
|
O |
|
H2N |
|
CH |
|
C |
+ CH I |
H C |
|
NH |
|
CH |
|
C |
|
||||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
3 |
_ |
AgI,H2O |
3 |
|
|
|
|
|
|
|
|
|
|
R |
OH |
|
|
|
|
|
R |
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
||||||||
173

Аминокислоты реагируют с альдегидами, образуя аминоспирты, которые легко могут быть превращены в имины (основания Шиффа). Реакция аминокислот с формальдегидом приводит к образованию аминоспиртов, которые можно оттитровывать, используя метод кислотно-основного титрования. Непосредственное титрование аминокислот щелочью не может быть использовано для их количественного определения вследствие амфотерности аминокислот:
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
H |
|
C + |
H N |
|
CH |
|
C |
|
HO |
|
CH |
|
NH |
|
CH |
|
C |
|
_ |
|
CH2 |
|
N |
|
|
CH |
|
C |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
H |
2 |
|
|
|
|
|
OH |
2 |
|
|
|
|
|
|
|
H O |
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
2 |
|
|
|
|
R |
||||||
|
|
|
|
|
R |
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Аминокислоты могут вступать в реакции дезаминирования. В лабораторных условиях (in vitro) дезаминирование происходит под действием азотистой кислоты:
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
H2N |
|
|
CH |
|
C + HNO2 |
R |
|
|
CH |
|
C |
+ N2 |
+ H O |
|
|
||||||||||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
2 |
|
|
R |
|
|
|
OH |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||
В животных и растительных организмах дезаминирование происходит с участием ферментов и может быть окислительным или неокислительным.
Неокислительное дезаминирование приводит к образованию , - непредельных кислот и отщеплению аммиака:
|
|
|
|
|
O |
аспартаза |
O |
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H N |
|
CH |
|
C |
|
C |
|
CH |
|
CH |
|
C |
+ NH |
|
|
|
|
|
|||||||||||
|
|
|
|
|
||||||||||
|
|
|
|
|||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
OH |
|
HO |
OH |
||||||
|
|
|
|
|||||||||||
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
||
|
|
COOH |
|
|
|
|
|
|
|
|
|
|||
Окислительное дезаминирование идет с участием кофермента НАД+ и оксидаз – ферментов, катализирующих окислительновосстановительные реакции.
174

O |
|
|
|
|
O |
+ |
+ O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|
|
|
|
|
|
O |
|||
C |
|
CH2 |
|
|
CH |
|
C |
|
НАД |
|
|
|
|
|
|
|
|
|
|
|
+ H2O |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
_ НАД Н |
C |
|
CH |
|
C |
|
C |
|
C |
|
CH |
|
C |
|
C |
|
||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
2 |
|
|
|
|
|
|
_ |
NH3 |
|
2 |
|
|
|
|
|
|
|||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
OH |
||||||||
NH2 |
|
HO |
|
|
|
|
|
NH |
|
HO |
|
|
|
O |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
- иминокислота |
|
|
|
|
кетокислота |
|||||||||||||||
|
-Аминокислоты |
реагируют |
|
с нингидрином |
с |
образованием |
|||||||||||||||||||||||||||
продукта сине-фиолетового цвета, что используется как общая качественная реакция на -аминкислоты:
|
O |
O |
OH |
NH2 CH COOH + 2 |
OH |
|
N |
|
_ CO , RCHO, |
||
|
OH |
|
|
|
2 |
|
|
R |
|
_ 3 H O |
|
|
|
2 |
|
|
O |
O |
O |
Взаимодействие -аминокислот с 2,4-динитрофторбензолом приводит к образованию динитрофенильных производных, окрашенных в желтый цвет. Эти соединения легко идентифицируются хроматографическими методами по значениям Rf.
NH |
|
CH |
|
COOH + F |
|
|
|
|
|
|
|
NO |
OH- |
O N |
|
|
|
|
|
|
|
NH |
|
CH |
|
COOH |
||
|
|
|
|
|
|
|
|
|
_ HF |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
2 |
|
|
|
|
|
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
NO2 |
|||||||||
Взаимодействие с 2,4-динитрофторбензолом ранее использовалось для идентификации N-концевой аминокислоты белков и пептидов. Для этого на пептид действовали 2,4-динитрофторбензолом, а затем продукт подвергали гидролизу, получая в итоге смесь - аминокислот и концевую аминокислоту в виде динитрофенильного производного. При помощи хроматографического анализа легко идентифицировали N-концевую кислоту по ее динитрофенильному производному и определяли аминокислотный состав пептида. Однако аминокислотная последовательность в этом случае оставалась
175

неизвестной. Только для дипептидов, используя данный способ, можно было установить их аминокислотную последовательность.
|
NO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||||||
|
|
|
F + NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
NO |
|
|
|
|
CH |
|
|
C |
|
|
|
NH |
|
CH |
|
|
|
C |
|
|
|
||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
O2N |
|
|
|
|
|
|
|
NH |
|
|
CH |
|
|
C |
|
NH |
|
|
|
CH |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
NO2 |
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
NH |
|
CH |
|
|
|
COOH |
|
|||||||
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R3 |
|
|
|
|
|
|
|
||
O |
|
|
|
|
|
|
|
|
|
|
+ H O,H+ |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
NH |
|
|
CH |
|
COOH |
2 |
||||||
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R3 |
|
||||
O N |
|
|
|
|
|
|
|
NH |
|
CH |
|
COOH + NH |
2 |
|
CH |
|
COOH + NH |
|
|
CH |
|
COOH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
R2 |
|
|
R3 |
|||||||
|
|
|
|
|
|
NO2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Один из универсальных способов установления аминокислотной последовательности основан на взаимодействии -аминокислот с фенилизотиоцианатом:
|
|
|
|
|
S |
|
|
|
S |
|
|
C H |
N C |
S + NH CH COOH |
C H NH C NH CH COOH |
C H N |
NH |
6 |
5 |
2 |
6 5 |
_ H O 6 5 |
|
|
|
R |
R |
2 |
|
|
|
|
|
||
|
|
|
|
O |
R |
На первом этапе реакции идет нуклеофильное присоединение – аминогруппа аминокислоты присоединяется к атому углерода за счет разрыва двойной связи углерод-азот, на втором этапе происходит внутримолекулярное нуклеофильное замещение, приводящее к образованию фенилтиогидантоина – циклического амида. Для определения аминокислотной последовательности пептида его подвергают воздействию фенилизотиоцианата в щелочной среде. Как и в предыдущем примере, сначала происходит нуклеофильное
176
присоединение к фенилизотиоцианату свободной аминогруппы N- концевой аминокислоты.
|
|
|
O |
|
|
|
O |
|
|
|
|
C6H5 N C |
S + NH2 CH C |
NH |
CH |
C |
NH |
CH |
COOH |
||||
|
|
R1 |
|
|
|
R2 |
|
|
|
R3 |
|
|
S |
|
|
O |
|
|
|
O |
|
|
|
C6H5 NH C |
NH |
CH |
C |
NH CH |
C |
NH |
CH COOH |
||||
|
|
|
R1 |
|
|
R2 |
|
|
|
R3 |
|
|
S |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
N |
NH |
+ NH2 |
CH |
C |
NH |
CH |
COOH |
|||
|
|
|
|
|
R2 |
|
|
|
R3 |
|
|
|
O |
R1 |
|
|
|
|
|
|
|
|
|
Дальнейшая обработка слабой кислотой без нагревания приводит к отщеплению от пептидной цепи N-концевой аминокислоты в виде фенилтиогидантоинового (ФТГ) производного, которое затем идентифицируется хроматографически. Последующее добавление к укороченному на одну аминокислоту пептиду фенилизотиоцианата в конечном итоге опять приводит к отщеплению аминокислоты с N-конца в виде ФТГ-производного. Таким образом можно определить аминокислотную последовательность, идентифицируя отщепляющиеся аминокислоты в виде их ФТГ-производных.
Реакции аминокислот по карбоксильной группе
Аминокислоты образуют сложные эфиры, реагируя с избытком спирта в присутствии HCl, как катализатора. Реакция протекает в спиртовой среде, а образующийся сложный эфир в виде соли выпадает
177

в осадок. Действуя более сильными основаниями на аммониевую соль сложного эфира, можно выделить сложный эфир в свободном виде:
NH2 |
|
|
CH |
|
COOH + C2H5OH |
HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NaOH |
|
|
|
|
|
|
|
|
|
|
NH3 |
|
CH |
|
COOC2H5 |
Cl |
|
NH |
|
CH |
|
COOC H |
|||||||||||||||
|
|
|
_ |
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
_ |
|
2 |
|
2 5 |
||||
|
|
R |
|
|
|
|
|
|
|
|
R |
|
NaCl,H2O |
R |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
Образование сложных эфиров используется для защиты карбоксильной группы при синтезе пептидов.
Карбоксильная группа аминокислот может быть превращена в ангидридную или галогенангидридную группу, но при проведении этих реакций необходимо предварительно защитить аминогруппу:
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
||||||
|
|
|
|
|
(CH3CO)2O |
|
|
|
|
|
|
|
|
|
|
SOCl2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
NH2 |
|
|
CH |
|
COOH _ CH3COOH H3C |
|
C |
|
NH |
|
|
CH |
|
COOH _ SO , HCl |
H3C |
|
C |
|
NH |
|
|
CH |
|
C |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
R |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
||||||||||
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
R |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
O |
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
O |
|
O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
C |
|
NH |
|
|
CH |
|
COOH + |
H5C2O |
|
C |
_ |
|
H C |
|
C |
|
NH |
|
CH |
|
C |
|
O |
|
C |
|
OC H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
HCl, |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 5 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
этиловый эфир |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
хлормуравьиной кислоты |
|
|
|
|
|
|
|
|
|
смешанный ангидрид |
|||||||||||||||||
Превращение карбоксильной группы в более реакционные ангидридную или галогенангидридную группы используют для активации карбоксильной группы при синтезе белков и пептидов.
Избыток аминокислот в организме уменьшается не только за счет реакций дезаминирования, но и в результате реакций декарбоксилирования. Декарбоксилирование -аминокислот протекает легко, что объясняется наличием у -углеродного атома двух электроноакцепторных заместителей (NH2- и СООН-группы). Вне организма (in vitro) декарбоксилирование происходит при нагревании аминокислот в присутствии щелочей, в организме (in vivo) – с участием ферментов – декарбоксилаз, приводя к образованию биогенных аминов:
178

|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
NH |
|
|
CH |
|
C |
|
OH |
NH |
|
CH |
|
CH OH |
+ CO |
||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
2 |
|
|
2 |
|
|
|
||||||||
|
|
|
|
|
СH2OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
N |
|
|
|
|
|
|
|
|
CH2 |
|
CH |
|
COOH |
|
N |
|
|
|
|
|
CH2 |
|
CH2 |
|
NH2 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
N |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Стратегия пептидного синтеза
Пептиды и белки часто представляют как результат реакции поликонденсации -аминокислот. В действительности же, на практике реакцию поликонденсации не используют, так как даже при синтезе дипептидов этим способом возникают проблемы с аминокислотной последовательностью и выходом нужного дипептида.
При взаимодействии двух разных аминокислот образуются семь дипептидов (без учета трипептидов, тетрапептидов и т.д.), разных по строению и аминокислотной последовательности, что существенно уменьшает количество нужного продукта.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|||||
NH2 |
|
|
|
|
CH |
|
|
|
|
COOH + NH2 |
|
|
|
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
CH |
|
|
|
C |
|
|
NH |
|
|
|
CH |
|
COOH + |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
R2 |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
CH |
|
|
|
C |
|
|
NH |
|
|
|
|
CH |
|
|
|
COOH + NH2 |
|
|
|
CH |
|
C |
|
NH |
|
|
|
|
CH |
|
|
COOH + |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
R2 |
|
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
R1 |
O |
|
|
|
|
|
O |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
R1 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
NH |
||||||||||||||||||
NH2 |
|
|
|
|
CH |
|
|
|
C |
|
|
NH |
|
|
|
CH |
|
|
|
COOH |
+ |
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
NH |
|||||||||||
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R1 |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|||||||||||||
Образование пептидной связи не представляет проблемы – пептидные связи легко образуются при взаимодействии амина или аминокислоты с активированной карбоксильной группой (ангидридной или галогенангидридной) другого соединения. Проблема в синтезе
179
белков и пептидов заключается в получении пептида или белка с нужной аминокислотной последовательностью. Чтобы преодолеть эти трудности, пептид синтезируют по стадиям, на каждой из которых приходится защищать (блокировать) одни функциональные группы и активировать другие. Активными должны быть функциональные группы, участвующие в образовании нужной амидной связи – карбоксильная группа одной молекулы с защищенной аминогруппой и аминогруппа другой молекулы с защищенной карбоксильной группой. Для защиты карбоксильной группы обычно используют ее перевод в сложный эфир, так как сложные эфиры легче гидролизуются, чем амиды, а удалить защитную группу можно, не затрагивая пептидную связь. Для защиты аминогруппы используют ее превращение в особые типы амидов, которые можно разрушать (снимать защиту) в условиях, в которых пептидные и амидные связи не затрагиваются. Для активации карбоксильной группы используют ее превращение в галогенангидридную группу или в смешанный ангидрид. Если боковые цепи аминокислот содержат реакционные функциональные группы, их также надо защищать.
Рассмотрим стратегию пептидного синтеза на примере образования аланилглицина.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
CH |
|
COOH |
NH2 |
|
CH2 |
|
COOH |
NH2 |
|
|
CH |
|
C |
|
NH |
|
CH2 |
|
COOH |
||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
||||||||||||||||||||||
|
|
CH3 |
|
Глицин |
|
|
CH3 |
|||||||||||||||||
|
Аланин |
|
|
|
|
|
Аланилглицин |
|||||||||||||||||
Для получения такой последовательности соединения аминокислот необходимо:
180
