
posobia2 / Лекции по биоорганической химии (2011 г
.).pdf
HO
HO
HO
HO
HO
HO
HO
HO
HO
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
CH |
|
|
|
|
COOH |
фенилаланин |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(незаменимая аминокислота) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гидроксилаза |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
CH |
|
|
|
|
COOH |
тирозин |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
гидроксилаза |
|
||||||||||||||||||
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
CH |
|
|
|
COOH |
3,4-дигидроксифенилаланин |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(3,4-ДОФА) |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
декарбоксилаза |
|||||||||||||||||
|
|
|
|
|
|
CH2 |
|
|
|
CH2 |
|
|
|
|
NH2 |
дофамин |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дофамин- -оксидаза |
|||||||||||||||||
|
|
* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
CH |
|
|
|
CH2 |
|
|
|
|
NH2 |
норадреналин |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N-метилтрансфераза |
|||||||||||||||||
|
|
* |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 адреналин |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
CH |
|
|
CH2 |
|
|
NH |
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Гидрокси- и аминокислоты, как гетерофункциональные соединения, проявляют типичные свойства как карбоновых кислот, так и свойства спиртов или аминов. Однако для них характерны и специфические реакции, обусловленные взаимным расположением функциональных групп.
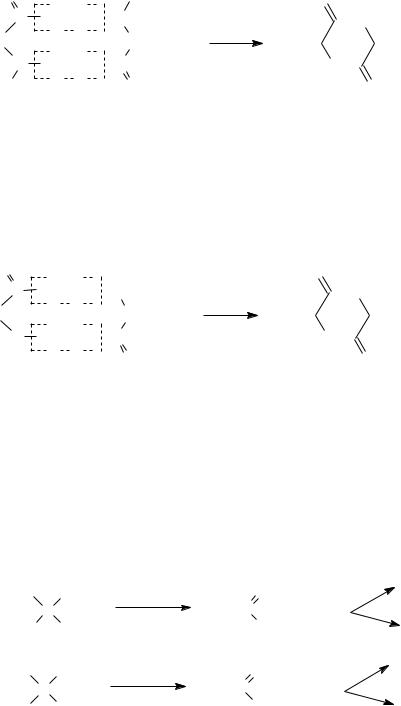
При нагревании -аминокислоты подвергаются межмолекулярной дегидратации с образованием устойчивых шестичленных гетероциклов – дикетопиперазинов :
121
|
|
O |
|
|
|
|
|
|
|
|
|
H |
|
|
O |
|
|||||||||
|
|
C |
OH |
|
H |
|
|
N |
T |
|
|
|
|
|
NH |
|
|||||||||
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
H3C |
|
CH |
|
|
+ |
|
|
|
|
|
CH |
|
CH3 |
H3C |
|
|
|
|
|
|
|
CH3 + |
2 H O |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
N |
H |
HO |
|
|
C |
|
|
|
HN |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
H |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
-аланин |
|
|
|
|
|
дикетопиперазин |
|
||||||||||||||||||
(2-аминопропановая кислота) |
|
|
(циклический диамид) |
|
|||||||||||||||||||||
При нагревании -гидроксикислоты образуют лактиды как результат межмолекулярного отщепления воды:
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|||||||
|
|
C |
OH |
|
|
H |
|
|
O |
T |
|
|
|
|
|
|
O |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
H3C |
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
CH3 |
H |
C |
|
|
|
|
|
|
|
CH |
|
|
2 H O |
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
3 |
2 |
|
|
|
O |
H |
HO |
|
|
C |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
молочная кислота |
|
|
|
|
|
лактид |
|
|
|
||||||||||||||||||||||
(2-гидроксипропановая кислота) |
(циклический сложный диэфир) |
|
При нагревании -гидроксикислот с серной кислотой происходит их превращение в карбонильное соединение и муравьиную кислоту, которая дальше разлагается на угарный газ и воду:
CH3 |
OH |
H SO , T |
|
|
|
|
|
O |
|
CO |
|
||
|
|
C |
2 |
4 |
CH3 |
|
|
C |
+ |
|
|
|
|
|
|
|
|
|
|
HCOOH |
|
|
|||||
|
|
|
|
|
|
|
|
||||||
|
H |
COOH |
|
|
|
|
|
|
H |
|
H2O |
|
|
CH3 |
OH |
H SO , T |
|
|
|
|
|
O |
CO |
|
|||
|
|
C |
2 |
4 |
CH3 |
|
|
C |
+ |
|
|
|
|
|
|
|
|
|
HCOOH |
|
|
||||||
|
|
|
|
|
|
|
|||||||
CH |
3 |
COOH |
|
|
|
|
|
|
CH3 |
|
H O |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
Нагревание |
-амино- |
и |
|
|
-гидроксикислот |
ведет |
к |
||||||
внутримолекулярному отщеплению аммиака или воды и образованию
, -непредельных кислот:
122

|
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
||||||
CH3 |
|
CH |
CH |
COOH |
CH |
|
CH |
|
|
CH |
|
|
COOH |
||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
- NH |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
NH2 |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3-аминобутановая кислота |
|
бутен-2-овая кислота |
|||||||||||||||||||||||
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
||||||||||
H3C |
|
CH2 |
|
CH |
CH |
COOH |
H3C |
|
|
|
CH2 |
|
CH |
|
CH |
|
COOH |
||||||||
|
|
- H O |
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3-гидроксипентановая кислота |
пентен-2-овая кислота |
||||||||||||||||||||||||
Легкость отщепления NH3 или H2O обусловлена возникновением в-положении С-Н кислотного центра из-за влияния двух электроноакцепторных заместителей.
Нагревание -амино и -гидроксикислот приводит к образованию пятичленных гетероциклов – лактамов и лактонов - в результате
внутримолекулярной дегидратации:
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
OH H |
|
|
T |
O |
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
H2C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
H |
|
|
|
|
|
|
|
|
|
|
+ H2O |
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
-аминомасляная кислота |
|
|
|
|
|
лактам |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
(4-аминобутановая кислота) |
(циклический амид) |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
T |
H3C |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
H2C |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
O + H2O |
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
гидроксивалерьяновая кислота |
|
|
|
|
|
|
|
|
лактон |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
(4-гидроксипентановая кислота) |
|
(циклический сложный эфир) |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
Оксокислоты часто встречаются в живых тканях, участвуют в |
||||||||||||||||||||||||||||||||||||||||||||||||||
процессах метаболизма. Наибольшее значение имеют - |
и |
- |
||||||||||||||||||||||||||||||||||||||||||||||||||||
оксокислоты. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
CH |
|
|
C |
|
COOH |
CH |
|
|
C |
|
|
CH |
|
|
|
|
COOH HOOC |
|
C |
|
CH |
|
|
|
COOH |
HOOC |
|
C |
|
CH |
|
|
CH |
|
COOH |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
3 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
2 |
|
|
2 |
|
||||||||
пировиноградная |
|
ацетоуксусная |
|
|
щавелевоуксусная |
-кетоглутаровая |
||||||||||||||||||||||||||||||||||||||||||||||||
2-оксопропановая |
3-оксобутановая |
|
|
2-оксобутандиовая |
2-оксопентандиовая |
|||||||||||||||||||||||||||||||||||||||||||||||||
123

Как гетерофункциональные соединения, они проявляют свойства как кислот, так и кетонов или альдегидов:
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH |
|
COOH |
+ |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2, |
t |
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
H |
CH3 |
|
C |
|
COOH |
|||||||||||||
|
|
|
||||||||||||||||||
|
|
|
|
NH |
N |
3 |
|
|
|
|
|
|
|
|||||||
|
|
|
|
O |
|
|
|
|
|
|||||||||||
|
|
|
|
+ |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
- |
2 |
|
|
|
|
|
|
|
|
CH3 |
|
C |
|
|
|
COOH |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
CH3 |
|
C |
|
|
|
|
COONa |
||
|
|
|
|
|
|
|
|
|
||||||
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
H2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3O |
|
|
|
|
|
O |
||||||
|
|
|
H, |
+ |
|
|
|
|||||||
- |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2O |
|
|
CH3 |
|
C |
|
|
COOCH3 |
||||
|
|
|
|
|
|
|
||||||||
Оксо-группа, содержащаяся в оксокислотах, являясь электроноакцепторным заместителем, усиливает их кислотные свойства за счет проявления отрицательных индуктивного и мезомерного (при наличии сопряженной системы) эффектов:
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
O |
||
+ I |
|
O |
|
+ I |
|
|
O |
|
+ I |
||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
CH3 C |
CH2 |
C |
|
|
CH3 |
C |
|||
CH3 CH2 |
C |
|
|
|
|
|
C |
||||||
|
|
|
|
|
|
|
O |
|
|
O H |
|||
|
|
O |
H |
|
|
|
H |
|
|
||||
|
|
|
|
_I |
|
|
|
|
_ I |
_M |
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
увеличение на атоме углерода карбоксильной группы, усиление кислотных свойств
При наличии двух карбоксильных групп в молекулах оксокислот более сильные кислотные свойства проявляет та карбоксильная группа, ближе к которой расположена оксогруппа. Из-за более близкого расположения электроноакцепторного заместителя на атоме углерода такой карбоксильной группы возникает больший частичный положительный заряд и связь О-Н поляризуется в большей степени, что приводит к усилению кислотности. Присутствие в молекулах двух сильных электроноакцепторных заместителей приводит к возникновению С-Н кислотного центра, благодаря которому для оксокислот характерна кето-енольная таутомерия.
124

|
|
O |
|
OH |
CH2 |
C COOH |
|
||
H |
CH2 C COOH |
|||
|
O |
|
|
OH |
CH3 |
C |
CH |
COOH |
CH3 C CH COOH |
|
O |
H |
|
OH |
HOOC C |
CH |
COOH |
HOOC C CH COOH |
|
|
|
H |
|
|
Обнаружить енольную форму кетокислот можно с помощью качественных реакций. При взаимодействии с FeCl3 енольный гидроксил (как и фенольный) дает характерное фиолетовое окрашивание, а при взаимодействии с бромной водой наблюдается ее обесцвечивание за счет протекания реакции по двойной связи.
Оксокислоты, в молекулах которых оксогруппа находится в - или-положениях, легко декарбоксилируются. -Оксокислоты подвергаются окислительному декарбоксилированию под действием мягких окислителей (Cu(OH)2, Ag2O и т.п.):
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH3 |
|
C |
|
|
COOH |
|
COOH |
+ CO |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
CH |
|||||||||||||||||||||
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
HOOC |
|
|
C |
|
CH2 |
|
|
CH2 |
|
|
COOH |
HOOC |
|
CH2 |
|
CH2 |
|
COOH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
-Оксокислоты |
неустойчивы |
и |
самопроизвольно |
||||||
декарбоксилируются при комнатной температуре. |
|
|
|
||||||
|
H |
|
O |
|
H |
|
|
O |
|
|
O |
O |
|
|
|
|
|||
|
|
|
O |
|
|
|
|||
|
|
|
C |
|
|
|
|
|
|
|
C |
C |
+ |
C |
|
CO2 + |
HOOC C |
CH3 |
|
|
|
|
|
||||||
HOOC |
CH2 |
O |
O |
|
|
|
|
|
|
HOOC |
CH2 |
|
|
|
|||||
|
|
|
|
|
|
||||
Легкость декарбоксилирования этих соединений обусловлена |
|||||||||
синхронным |
переносом |
|
протона |
от |
карбоксильной |
группы |
к |
||
125

карбонильной через образование внутримолекулярного переходного состояния.
|
|
|
OH |
|
|
|
|
|
O |
|
|
O |
H |
O |
|
|
|
OH |
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3 |
|
CH |
|
CH2 |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
- CO |
|
C |
|
C |
|||||||||||
|
|
|
|
C |
|
C |
|
H3C |
HOOC |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
2 |
|
CH2 |
|
|
CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
O |
|
|
|
|
|
|
|
|
||||
Ацетоуксусная кислота, образующаяся в организме в результате окисления -оксимасляной кислоты, декарбоксилируется аналогичным образом.
-Оксимасляная кислота, ацетоуксусная кислота и ацетон объединяются в клиническом анализе в группу «кетоновых тел». В моче здорового человека кетоновые тела содержатся в ничтожно малых количествах (не более 0,01г в сутки). В моче больных сахарным диабетом содержание кетоновых тел намного больше. Наряду с сахарным диабетом, кетоновые тела выделяются с мочой при голодании, исключении углеводов из пищи. Кетоновые тела можно обнаружить с помощью галоформной реакции. В эту реакцию вступают соединения, имеющие ацетогруппу СН3-С(О)-.
|
|
|
|
|
|
|
O |
|
|
|
3 I2, 3 NaOH |
|
|
|
|
O |
|
|
NaOH |
|
|
|
|
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
CH3 |
|
|
|
C |
|
|
|
R |
I3C |
|
|
|
C |
|
|
R |
CHI3 |
+ R |
|
C |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
- 3 NaI, 3 H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ONa |
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
3 I2, 3 NaOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NaOH CHI3 |
|
|
|
|
||||
CH3 |
|
C |
|
|
|
|
CH3 |
I3C |
|
|
C |
|
CH3 |
+ CH3 |
|
|
C |
|||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
- 3 NaI, 3 H2O |
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
йодоформ |
|
ONa |
|||||
Галоформную реакцию используют в аналитических целях, констатируя образование йодоформа по характерному запаху.
126

Биологически активные гетероциклические соединения
Из огромного числа гетероциклических соединений необходимо отметить гетероциклические соединения, имеющие в своем составе один или несколько атомов азота. Эти соединения широко распространены в природе и являются структурной основой многочисленных физиологически активных веществ и лекарственных препаратов.
Пятичленные гетероциклы с двумя атомами азота
Представителями пятичленных гетероциклов с двумя атомами азота являются пиразол и имидазол:
|
пиридиновый атом азота |
|
|
N |
|
пиразол |
N |
имидазол |
N |
N |
|
H |
H |
|
пиррольный атом азота
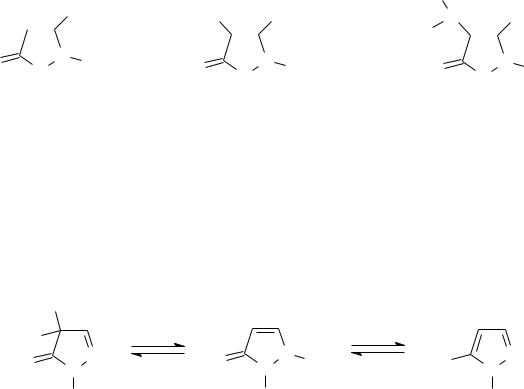
Оба соединения обладают ароматичностью, в единой сопряженной системе участвуют шесть электронов. Атомы углерода в сопряжение предоставляют по одному р-электрону, пиррольный атом азота в сопряжение отдает пару р-электронов, а пиридиновый атом азота – один р-электрон. Оба изомера обладают меньшей реакционной способностью в реакциях электрофильного замещения чем пиррол, что обусловлено электроноакцепторным характером пиридинового атома азота, уменьшающего электронную плотность в сопряженной системе. Оба гетероцикла проявляют амфотерные свойства, так как содержат
127

одновременно кислотный и основный центры. Пиридиновый атом азота проявляет основные свойства за счет неподеленной электронной пары, не участвующей в создании сопряженной системы, пиррольный атом выступает как N-Н кислотный центр. Для обоих соединений характерно образование межмолекулярных водородных связей и прототропная таутомерия:
|
|
|
|
|
|
4 |
3 |
|
4 |
5 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
1 2 N |
|
|
|
|
|
|
|
N |
N |
H3C |
5 |
|
3 |
1 |
|
|
N N |
H |
N |
H3C |
2 |
NH |
||||
H |
|
|
|
N |
|
|||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
4-метилпиразол |
3-метилпиразол |
||||
Из-за быстрого перехода протона практически невозможно выделить в индивидуальном виде изомеры замещенного пиразола и имидазола. Имидазольный цикл является структурным элементом разнообразных природных соединений, наиболее важными из которых являются аминокислота гистидин и продукт ее декарбоксилирования гистамин.
N |
|
|
|
|
CH2 |
|
|
CH |
|
COOH |
|
N |
|
|
|
|
CH2 |
|
CH2 |
|
NH2 |
N |
|
|
|
|
|
- CO2 |
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
N |
|||||||||||
|
|
|
|
|
NH2 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
H |
|
|
|
|
|
|
|
|
|
|
H |
|||||||||
|
|
|
|
|
гистидин |
|
гистамин |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Гистидин выступает как катализатор в ферментативных реакциях за счет наличия в молекуле кислотного и основного центров. Гистамин принимает участие в передаче нервного возбуждения, активирует секрецию соляной кислоты слизистой желудка, снижает кровяное давление, при освобождении из связанного сотяния или введении в
организм вызывает болевые ощущения и отеки. Гистидин также снижает
128
гормональную активность коркового слоя надпочечников, в связи с чем применяется для лечения шизофрении.
Пиразольный цикл в составе природных соединений не обнаружен, однако структура пиразола лежит в основе жаропонижающих, болеутоляющих препаратов – антипирина, амидопирина, анальгина (первые два препарата сняты с производства и заменены более эффективными).
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
(CH3)2N |
|
|
CH3 |
|
|
N |
|
|
CH3 |
|
O |
|
|
|
N |
CH3 |
O |
|
|
N CH3 |
NaO3S |
|
CH2 |
|
|
N CH |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
O |
|
|
||||||
|
N |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
N |
|
|
|
N |
3 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
C6H5 |
|
|
|
C6H5 |
|||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
антипирин |
амидопирин |
|
|
анальгин |
|
|||||||||
Структурной основой всех трех препаратов является пиразолон-5. Это соединение может существовать в виде трех таутомеров – двух кето-форм и енольной формы:
|
H |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
O |
N |
O |
N |
N |
H |
HO |
N |
N |
|
N |
|||||
|
|
|
|
|
|||
|
H |
|
H |
|
|
|
H |
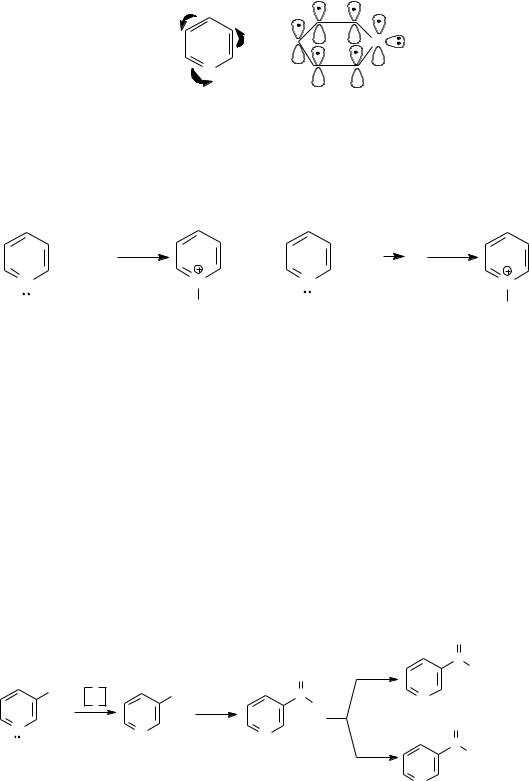
Шестичленные гетероциклы с одним и двумя атомами азота Пиридин является -дефицитным ароматическим соединением из-
за наличия в цикле атома азота, проявляющего электроноакцепторные свойства.
129
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
Неподеленная пара р-электронов атома азота не участвует в сопряжении и ответственна за проявление пиридином основных и нуклеофильных свойств:
|
|
|
|
|
+ H+Cl- |
|
|
|
|
- |
+ H C Cl |
- |
||
|
Cl |
3 |
|
Cl |
|
|
|
||
N |
N |
N |
|
N |
|
H |
|
|
CH3 |
При взаимодействии с кислотами неподеленная пара электронов атома азота предоставляется для образования связи с протоном, т.е. пиридин выступает как акцептор протона и проявляет основные свойства. Если пара электронов атома азота предоставляется для образования связи с любым другим электрофильным атомом, то пиридин в этом случае выступает как нуклеофил. Пиридиновый цикл содержится как в составе отдельных лекарственных препаратов, так и является структурной основой разнообразных природных соединений.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C NH2 |
|
|
|
|
|
|
|
|
|
CH3 |
|
COOH |
C |
|
N |
никотинамид |
|
|
Cl |
|||||
|
|
|
SOCl2 |
|
|
||
|
|
|
|
|
|
||
N |
|
- H2O |
-HCl,SO2 |
|
|
|
|
|
|
N |
N |
|
|
|
|
|
|
|
|
|
C |
||
|
|
|
|
хлорангидрид |
|
|
|
|
|
|
|
|
|
N(CH3)2 |
|
b-метилпиридин |
никотиновая |
никотиновой |
|
|
|||
|
|
диэтиламид |
|||||
|
|
|
кислота |
кислоты |
|
|
|
|
|
|
|
N |
никотиновой кислоты |
||
|
|
|
|
|
|
||
(кордиамин)
Никотиновая кислота и ее амид являются формами витамина РР, использующегося для лечения пеллагры. Кордиамин является стимулятором ЦНС. Производные изоникотиновой кислоты
130
