
- •Лекція №1. Предмет і завдання біохімії
- •Загальні уявлення про обмін речовин
- •Хімічний склад живого організму
- •Клітина – основа структури живих систем
- •Історія розвитку біохімії
- •Лекція № 2 Білкові речовини
- •Функції білків
- •Класифікація амінокислот
- •Властивості амінокислот
- •Кольорові реакції на амінокислоти
- •Методи визначення амінокислот
- •Будова білків
- •Фізико-хімічні властивості білків
- •Шляхи виділення та розділення білків
- •Методи визначення білка
- •Класифікація білків
- •Природні пептиди
- •Лекція № 3 Нуклеїнові кислоти
- •Властивості і будова днк
- •Будова і функції рнк
- •Нуклеозиди і нуклеотиди
- •Назви нуклеозидів та нуклеотидів
- •Лекція № 4 Вітаміни
- •Жиророзчинні вітаміни
- •1(138), 10(245) Вітаміни групи а (антиксерофтальмічний фактор).
- •Водорозчинні вітаміни
- •1(162), 10(277) Вітамін с (аскорбінова кислота)
- •Вітаміноподібні речовини
- •Антивітаміни, антиметаболіти, антибіотики
- •Лекція № 5 Вуглеводи
- •Моносахариди
- •10(216), 11Окремі представники моносахаридів
- •Дубильні речовини
- •Полісахариди
- •Лекція № 6 Ліпіди
- •Характеристика промислових жирів
- •Лекція № 7. Ферменти
- •Будова ферментів
- •Теорія ферментативного каталізу
- •Кінетика ферментативних реакцій
- •Властивості ферментів
- •Класифікація і номенклатура ферментів
- •Номенклатура ферментів
- •Класифікація ферментів
- •Характеристика окремих класів ферментів та їх промислове використання Оксидоредуктази
- •Трасферази
- •Гідролази
- •Ізомерази
- •Локалізація ферментів у клітині
- •Лекція № 8 Обмін речовин
- •Способи живлення організмів
- •Теорія біологічного окислення
- •Анаеробний розклад вуглеводів
- •Гліколіз
- •Види бродіння
- •2.Пропіоновокисле бродіння.
- •3.Маслянокисле бродіння
- •4.Ацетонобутилове бродіння.
- •5.Метановебродіння.
- •7.Спиртове бродіння.
- •Аеробний розклад вуглеводів
- •Енергетичний ефект повного розщеплення глюкози
- •Пентозний цикл (пентозофосфатний або гексозомонофосфатний шлях)
- •Гліоксилатний цикл
- •Фотосинтез
- •Біосинтез вуглеводів
- •Обмін ліпідів Розпад ліпідів
- •Окислення гліцерину
- •Окислення насичених жк
- •Енергетика -окислення жк
- •Α-окислення жк
- •Біосинтез ліпідів Біосинтез гліцерину
- •Біосинтез жк
- •Біосинтез тригліцеридів
- •Зміна жирів при зберіганні
- •Основні перетворення ліпідів
- •Обмін нуклеїнових кислот Розпад нк
- •Синтез нк
- •Обмін білків Розпад білків
- •Перетворення амінокислот
- •Нейтралізація і виведення аміаку з організму
- •Орнітиновий цикл
- •Біосинтез амінокислот
- •Біосинтез білків
- •Взаємозв’язок процесів обміну речовин у живому організмі
- •Література
Природні пептиди
1(63), 12(38) Деякі пептиди зустрічаються у вільному вигляді у рослинах, тканинах тварин та мікроорганізмах. Мають велике значення як проміжні продукти обміну речовин та фізіологічно досить активних сполук. Прикладом може слугувати трипептид глутатіон, який складається із залишків глікоколу, цистеїну та глютамінової кислоти.

Глутатіон міститься у всіх живих клітинах. Особливо багато його – у зародках пшеничного зерна та дріжджах. Є сильним відновником, дуже легко піддається окисленню. Бере участь у окисно-відновних реакціях.При цьому сульфгідрильна група окислюється (віднімається водень) і дві молекули глутатіону з’єднуються дисульфідним зв’язком, утворюючи молекулу окисленого глутатіону:

8(33) Глутатіон підвищує активність деяких ферментів (папаїну) Останній міститься у борошні і підвищення його активності призводить до розпаду білків борошна і дріжджів, що знижує якість харчових продуктів. Для запобігання руйнування клейковини під впливом папаїну відновлений глутатіон окислюють, наприклад дегідроаскорбіновою кислотою.
12(38) До пептидів належать антибіотики – граміцидин, гормони – окситоцин та вазопресин, циклопептиди блідої поганки.
Лекція № 3 Нуклеїнові кислоти
10(134) НК були відкриті швейцарським вченим Мішером у 1869 р. в ядрах лейкоцитів. У зв’язку з цим їх назвали нуклеїновими від nucleus – ядро.
5(38) Загальнобіологічна роль нуклеїнових кислот заключається в тому, що вони управляють всіма процесами, і, відповідно, всіма властивостями живого організму та передачею цих властивостей наступним поколінням.
Існує два типи нуклеїнових кислот: рибонуклеїнова (РНК) та дезоксирибонуклеїнова (ДНК) кислоти. Вони представляють собою полінуклеотиди, які побудовані з великої кількості структурних одиниць – нуклеотидів.
Нуклеотид - це сполука, що складається із залишків азотистої основи, цукру та фосфорної кислоти. Речовина, що складається лише з залишків азотистої основи та цукру, називається нуклеозидом.
1. Як цукор до складу РНК входить рибоза, до ДНК - дезоксирибоза. 1(78) Вуглеводи в молекулах НК знаходяться в -D-фуранозній формі.

2. З азотистих основ до складу нуклеїнових кислоти входять два похідних пурину - аденін та гуанін та три похідних піримідину - урацил, тимін та цитозин. Причому, до складу РНК входять АУГЦ, а до складу ДНК - АТГЦ, тобто кожен тип НК містить чотири основи.
П уринові
основи:
уринові
основи:

Піримідинові основи:
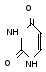


Урацил Тимін Цитозин
5(39) Всі азотисті основи мають таутомерні форми. Із-за наявності гідроксильної групи всі вони, окрім аденіну, можуть бути як в енольній, так і в кетонній формі. До складу НК всі азотистні основи, окрім аденіну, входять в кетонній формі.
1(79), 10(135) НК іноді містять інші похідні пурину та піримідину, їх називають мінорними основами (це метил-, оксіметил- та інші похідні основних азотистих основ). Лише до складу т-РНК входять близько 50 мінорних основ. В ДНК та РНК знайдені метиладенін, метилгуанін, метилурацил тощо.
3. Третім компонентом НК є фосфорна кислота.

5(39) Молекулярна маса НК дуже велика. Молекулярна маса РНК вірусу тютюнової мозаїки рівна 2000000, а молекулярна маса ДНК - 5-8 млн.
1(81), 10(1431) Для розуміння особливостей структури НК велике значення мають закономірності кількісного вмісту азотистих сполук, що встановлені вперше Чаргаффом (1949) і названі правилами Чаргаффа:
1. Сума пуринових основ рівна сумі піримідинових
А+Г=Ц+Т
2. Кількість аденіну та цитозину рівна кількості гуаніну та тиміну
А+Ц=Г+Т
3. Кількість аденіну рівна кількості тиміну, а кількість гуаніну рівна кількості цитозину
А=Т та Г=Ц
4. Співвідношення (Г+Ц)/(А+Т) називається коефіцієнтом специфічності. Для тварин та більшості рослин він складає 0,54 - 0,94, у мікроорганізмів 0,45 - 2,57.
