
- •Лекція №1. Предмет і завдання біохімії
- •Загальні уявлення про обмін речовин
- •Хімічний склад живого організму
- •Клітина – основа структури живих систем
- •Історія розвитку біохімії
- •Лекція № 2 Білкові речовини
- •Функції білків
- •Класифікація амінокислот
- •Властивості амінокислот
- •Кольорові реакції на амінокислоти
- •Методи визначення амінокислот
- •Будова білків
- •Фізико-хімічні властивості білків
- •Шляхи виділення та розділення білків
- •Методи визначення білка
- •Класифікація білків
- •Природні пептиди
- •Лекція № 3 Нуклеїнові кислоти
- •Властивості і будова днк
- •Будова і функції рнк
- •Нуклеозиди і нуклеотиди
- •Назви нуклеозидів та нуклеотидів
- •Лекція № 4 Вітаміни
- •Жиророзчинні вітаміни
- •1(138), 10(245) Вітаміни групи а (антиксерофтальмічний фактор).
- •Водорозчинні вітаміни
- •1(162), 10(277) Вітамін с (аскорбінова кислота)
- •Вітаміноподібні речовини
- •Антивітаміни, антиметаболіти, антибіотики
- •Лекція № 5 Вуглеводи
- •Моносахариди
- •10(216), 11Окремі представники моносахаридів
- •Дубильні речовини
- •Полісахариди
- •Лекція № 6 Ліпіди
- •Характеристика промислових жирів
- •Лекція № 7. Ферменти
- •Будова ферментів
- •Теорія ферментативного каталізу
- •Кінетика ферментативних реакцій
- •Властивості ферментів
- •Класифікація і номенклатура ферментів
- •Номенклатура ферментів
- •Класифікація ферментів
- •Характеристика окремих класів ферментів та їх промислове використання Оксидоредуктази
- •Трасферази
- •Гідролази
- •Ізомерази
- •Локалізація ферментів у клітині
- •Лекція № 8 Обмін речовин
- •Способи живлення організмів
- •Теорія біологічного окислення
- •Анаеробний розклад вуглеводів
- •Гліколіз
- •Види бродіння
- •2.Пропіоновокисле бродіння.
- •3.Маслянокисле бродіння
- •4.Ацетонобутилове бродіння.
- •5.Метановебродіння.
- •7.Спиртове бродіння.
- •Аеробний розклад вуглеводів
- •Енергетичний ефект повного розщеплення глюкози
- •Пентозний цикл (пентозофосфатний або гексозомонофосфатний шлях)
- •Гліоксилатний цикл
- •Фотосинтез
- •Біосинтез вуглеводів
- •Обмін ліпідів Розпад ліпідів
- •Окислення гліцерину
- •Окислення насичених жк
- •Енергетика -окислення жк
- •Α-окислення жк
- •Біосинтез ліпідів Біосинтез гліцерину
- •Біосинтез жк
- •Біосинтез тригліцеридів
- •Зміна жирів при зберіганні
- •Основні перетворення ліпідів
- •Обмін нуклеїнових кислот Розпад нк
- •Синтез нк
- •Обмін білків Розпад білків
- •Перетворення амінокислот
- •Нейтралізація і виведення аміаку з організму
- •Орнітиновий цикл
- •Біосинтез амінокислот
- •Біосинтез білків
- •Взаємозв’язок процесів обміну речовин у живому організмі
- •Література
Назви нуклеозидів та нуклеотидів
|
Азотисті основи |
Нуклео-зиди |
Нуклеотиди |
Скороче-на назва |
|
Аденін Гуанін Урацил Цитозин Тимін |
Аденозин Гуанозин Уридин Цитидин Тимідин |
Аденозинмонофосфат (аденілова к-та) Гуанозинмонофосфат (гуанілова к-та) Уридинмонофосфат (уридилова к-та) Цитидинмонофосфат (цитидилова к-а) Дезокситимідинмонофосфат |
АМФ ГМФ УМФ ЦМФ дТМФ |
10(137) Якщо азотиста основа з’єднується з дезоксирибозою – дезоксіаденозин, дезоксицитидин; нуклеотид – дезокситимідин-монофосфат.
В залежності від кількості залишків фосфорної кислоти, що приєднуються до нуклеозиду бувають МФ, ДФ, ТФ.
10(138), 5(41) Нуклеотиди не лише входять до складу нуклеїнових кислот, а можуть перебувати у вільному стані або бути складовими частинами ферментних систем.
Найважливішим з вільних нуклеотидів є аденозинтрифосфорна кислота (АТФ). Вона виконує роль акумулятора енергії бере участь в енергетичном обміні організму. За хімічною структурою АТФ є сполукою залишків аденіну, рибози та трьох залишків фосфорної кислоти:
Хімічний зв’язок, позначений кривою лінією, називається макроергічним зв’язком. В молекулі АТФ є два таких зв’язки. Вони містять значно більше енергії, ніж звичайні хімічні зв’язки. Фосфатні зв’язки таких сполук містять від 29 до 40 кДж/моль відщепленого фосфату. Звичайний зв’язок фосфорних ефірів, в тому числі перший зв’язок в молекулі АТФ, містить 8 - 12 кДж/моль енергії. При відщепленні від АТФ однієї або двох молекул фосфорної килоти, які зв’язані між собою макроергічним зв’язком, виділяється значна кількість енергії, яка використовується на побудову речовин.
5(42) Велику роль в організмі відіграють також три фосфати інших нуклеозидів – гуанозинтрифосфат (ГТФ), уридинтрифосфат (УТФ), тимідинтрифосфат (ТТФ), які беруть участь в окремих ланцюгах важливих ферментативних процесів обміну речовин.
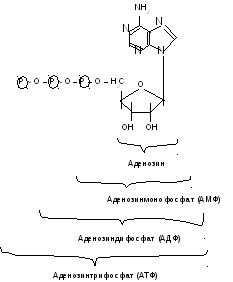
АМФ також має велике значення як складова частина ферментів. АМФ входить до складу коферментів всіх дегідрогеназ. Похідні аденілової кислоти (АМФ) є складовою частиною коферменту ацилювання.
Велике значення серед вільних нуклеотидів мають динуклеотиди НАД і ФАД.
НАД (нікотинамідаденіндинуклеотид)- входить до складу окисно-відновних ферментів дегідрогеназ, які окислюють органічні речовини шляхом віднімання водню, або відновлюють їх шляхом приєднання водню.
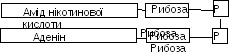
5(42) Коферментами інших дегідрогеназ (флавінових) є флавінмононуклеотид (ФМН) та флавінаденіндинуклеотид (ФАД) (містять вітамін В2).
Лекція № 4 Вітаміни
10 (240), 3(43), 1(134) Вітаміни - це низькомолекулярні органічні біологічно активні речовини різної хімічної природи, які синтезуються переважно в рослинних організмах і в невеликих кількостях потрібні для забезпечення нормальної життєдіяльності людин і тварин.
Визначний внесок у розвиток вчення про вітаміни вніс російський лікар Лунін М.І., який встановив, що для нормальної життєдіяльності організму крім основних поживних речовин (Б, Ж, В, мінеральних солей) потрібні ще якість невідомі на той час речовини. 7(274) Термін вітамін вперше був використаний для назви специфічного мікрокомпоненту їжі, що попереджав виникнення хвороби бері-бері. Оскільки ця речовина мала властивості аміну, Казимир Функ, польський біохімік, що першим отримав цю речовину в чистому вигляді, назвав його вітамін, що в перекладі означає “необхідний для життя амін”. В подальшому, коли були відкриті інші незамінні органічні мікрокомпоненти, виявилось, що не всі вони представляють собою аміни.
1(134) Вітаміни відрізняються від інших органічних харчових речовин двома характерними ознаками: 1) не включаються в структуру тканин; 2) не використовуються організмом як джерело енергії.
Порушення нормального обміну речовин часто пов’язані з недостатнім поступанням вітамінів в організм, повною їх відсутністю в їжі або порушенням їх всмоктування, транспорту. В результаті виникають авітамінози - хвороби, що спричинюються повною відсутністю в їжі або повного порушення засвоєння якогось вітаміну та гіповітамінози, що обумовлені недостатнім поступанням вітамінів з їжею чи поганим їх засвоєнням. Стани, пов’язані з поступанням в організм надмірних кількостей вітамінів називаються гіпервітамінозами.
5(239) Принципи хімічної будови вітамінів дуже різноманітні, тому їх класифікація будується на основі їх розчинності. Вітаміни поділяють на жирорзчинні - вітаміни А (ретинол), Д (кальцифероли), Е (токофероли), К (філохінони); водорозчинні - В1 (тіамін), В2 (рибофлавін), В6 (піридоксин), В12 (цианкобаламін), РР (нікотинамід), Вс (фолієва кислота), В3 (пантотенова кислота), Н (біотин), С (аскорбінова кислота), Р (біофлавоноїди).
7(275), 8(61), 1(245) Окрім цих, існують інші речовини, які необхідні певним видам, але зазвичай не вважаються вітамінами. Вони називаються вітаміноподібними речовинами. Ці сполуки або ж синтезуються в організмі в недостатній кількості або для них характерні не лише регуляторні, але й пластичні чи енергетичні функції. До них належать холін, ліпоєва кислота, пангамова кислота, оротова кислота тощо.
